解题方法
1 . 某溶液呈酸性,可能含有: 、
、 、
、 、
、 、
、 、
、 中的若干种。对其进行如下实验:
中的若干种。对其进行如下实验:
Ⅰ.取少量溶液,向其中加入过量 ,生成白色沉淀
,生成白色沉淀 和无色气体
和无色气体 ,该无色气体在空气中变为红棕色。
,该无色气体在空气中变为红棕色。
Ⅱ.将Ⅰ中所得溶液滤去沉淀后,加入过量浓 溶液,生成无色气体,最终得到红棕色沉淀
溶液,生成无色气体,最终得到红棕色沉淀 。
。
(1)上述6种离子中,该溶液肯定存在的为____________ ,肯定不存在 的为______ ,不能 确定是否存在的为______ 。
(2)请设计实验检验原溶液中是否存在 ,写出操作方法、现象及结论
,写出操作方法、现象及结论___________ 。
(3)生成无色气体 的离子方程式为
的离子方程式为____________ 。
(4)步骤Ⅱ中发生反应的离子方程式为___________________ 。
 、
、 、
、 、
、 、
、 、
、 中的若干种。对其进行如下实验:
中的若干种。对其进行如下实验:Ⅰ.取少量溶液,向其中加入过量
 ,生成白色沉淀
,生成白色沉淀 和无色气体
和无色气体 ,该无色气体在空气中变为红棕色。
,该无色气体在空气中变为红棕色。Ⅱ.将Ⅰ中所得溶液滤去沉淀后,加入过量浓
 溶液,生成无色气体,最终得到红棕色沉淀
溶液,生成无色气体,最终得到红棕色沉淀 。
。(1)上述6种离子中,该溶液肯定存在的为
(2)请设计实验检验原溶液中是否存在
 ,写出操作方法、现象及结论
,写出操作方法、现象及结论(3)生成无色气体
 的离子方程式为
的离子方程式为(4)步骤Ⅱ中发生反应的离子方程式为
您最近半年使用:0次
名校
解题方法
2 . 工业上,常用水蒸气通过炽热的焦炭制得水煤气(主要成分为 和
和 ),其反应的化学方程式为
),其反应的化学方程式为 ,请回答下列问题:
,请回答下列问题:
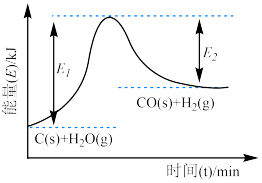
(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是__________。
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是__________。
(3)在体积均为 的甲、乙两个恒容密闭容器中,分别加入相同质量的一定量炭粉和
的甲、乙两个恒容密闭容器中,分别加入相同质量的一定量炭粉和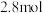 水蒸气,在不同温度下反应的过程如下图所示:
水蒸气,在不同温度下反应的过程如下图所示: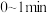 内的平均反应速率
内的平均反应速率
________ 。
②甲容器中,A点正反应速率__________ B点的逆反应速率(填“<”“>”或“=”)。
③反应过程中,两个容器温度:甲__________ 乙(填“<” “>”或“=”)。
④乙容器中C点时, 的物质的量百分数为
的物质的量百分数为__________ 。
(4)在 溶液条件下,以
溶液条件下,以 为原料,可制成一种燃料电池,写出该电池的负极反应式
为原料,可制成一种燃料电池,写出该电池的负极反应式____________________ ,当燃料电池消耗 (标况下)时,正极上有
(标况下)时,正极上有_________ 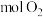 参与反应。
参与反应。
 和
和 ),其反应的化学方程式为
),其反应的化学方程式为 ,请回答下列问题:
,请回答下列问题:(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是__________。
| A.铝粉与氧化铁的反应 | B.氯化铵与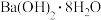 的反应 的反应 |
| C.锌片与稀硫酸的反应 | D.钠与冷水的反应 |
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是__________。
A.充入 使容器压强增大,提高反应速率 使容器压强增大,提高反应速率 |
B.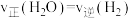 ,说明反应达到平衡状态 ,说明反应达到平衡状态 |
| C.容器中焦炭的质量不再变化,说明反应达到平衡状态 |
D.容器中水蒸气与氢气的体积比为 时,说明反应达到平衡状态 时,说明反应达到平衡状态 |
(3)在体积均为
 的甲、乙两个恒容密闭容器中,分别加入相同质量的一定量炭粉和
的甲、乙两个恒容密闭容器中,分别加入相同质量的一定量炭粉和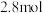 水蒸气,在不同温度下反应的过程如下图所示:
水蒸气,在不同温度下反应的过程如下图所示: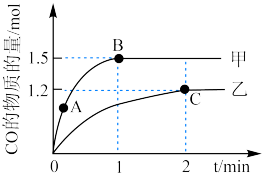
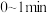 内的平均反应速率
内的平均反应速率
②甲容器中,A点正反应速率
③反应过程中,两个容器温度:甲
④乙容器中C点时,
 的物质的量百分数为
的物质的量百分数为(4)在
 溶液条件下,以
溶液条件下,以 为原料,可制成一种燃料电池,写出该电池的负极反应式
为原料,可制成一种燃料电池,写出该电池的负极反应式 (标况下)时,正极上有
(标况下)时,正极上有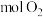 参与反应。
参与反应。
您最近半年使用:0次
2024-04-10更新
|
432次组卷
|
3卷引用:广东省深圳市宝安中学高中部2020-2021学年高一下学期期中考试化学试卷
3 . 研究氮及其化合物的性质具有极为重要的意义。
(1)NOx是汽车尾气中的主要污染物之一、NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:_______ ,此反应的氧化产物是_______ ,1molNO2反应转移电子_______ mol。
(2)工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,写出实验室用固体加热制取NH3的化学方程式为_______ ,用5.35g NH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积为_______ L。(NH4Cl的摩尔质量为53.5g·mol-1)
(3)实验室可以用铜与稀硝酸制取NO,写出该反应的离子方程式:_______ 。
(4)工业上采用氨氧化法制取硝酸,写出在催化剂作用下氨气与氧气反应的化学方程式:__ 。
(5)工业合成氨原料气氢气通过碳与水蒸气反应制取。已知1mol水蒸气和炽热的焦炭反应生成水煤气,反应吸热131.4 kJ 。写出该反应的热化学方程式______ 。
(1)NOx是汽车尾气中的主要污染物之一、NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:
(2)工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,写出实验室用固体加热制取NH3的化学方程式为
(3)实验室可以用铜与稀硝酸制取NO,写出该反应的离子方程式:
(4)工业上采用氨氧化法制取硝酸,写出在催化剂作用下氨气与氧气反应的化学方程式:
(5)工业合成氨原料气氢气通过碳与水蒸气反应制取。已知1mol水蒸气和炽热的焦炭反应生成水煤气,反应吸热131.4 kJ 。写出该反应的热化学方程式
您最近半年使用:0次
名校
4 . 氨能与 形成配合物
形成配合物 和
和 ,该反应在生产和生活中发挥着重要的作用。
,该反应在生产和生活中发挥着重要的作用。
(1)基态 原子价层电子的轨道表示式为
原子价层电子的轨道表示式为_______ , 中
中 与
与 间形成的化学键为
间形成的化学键为_______ 。
(2)将 置于
置于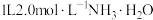 溶液中,通入
溶液中,通入 ,
, 转化为
转化为 的离子方程式为:
的离子方程式为:
_______ 
_______ 。反应1小时测得溶液中银的总浓度为 ,
, 的溶解速率为
的溶解速率为_______ 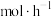 。
。
(3)氨与 形成配合物有助于
形成配合物有助于 溶解。常温下,向
溶解。常温下,向 饱和溶液(含足量
饱和溶液(含足量 固体)中滴加氨水,主要存在以下平衡:
固体)中滴加氨水,主要存在以下平衡:
(i)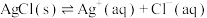
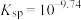
(ii)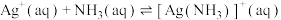
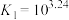
(iii)
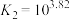
①下列有关说法中,正确的有_______ (填编号)。
A.加少量水稀释,平衡后溶液中 、
、 均减小
均减小
B.随 增大,反应ⅱ平衡正向移动,
增大,反应ⅱ平衡正向移动, 增大
增大
C.随 增大,
增大, 不变
不变
D.溶液中存在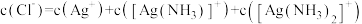
②反应

_______ (用 、
、 、
、 表示)。
表示)。
(4)向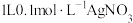 溶液中通入足量
溶液中通入足量 得到澄清溶液(设溶液体积不变),溶液中
得到澄清溶液(设溶液体积不变),溶液中 、
、 、
、 的物质的量分数
的物质的量分数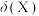 随
随 的变化如图所示。
的变化如图所示。
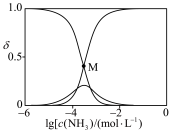
已知溶液中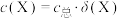 ,
, 。
。
① 点溶液中
点溶液中
_______  。
。
②计算 点溶液中
点溶液中 的转化率
的转化率________ (写出计算过程,已知 )。
)。
 形成配合物
形成配合物 和
和 ,该反应在生产和生活中发挥着重要的作用。
,该反应在生产和生活中发挥着重要的作用。(1)基态
 原子价层电子的轨道表示式为
原子价层电子的轨道表示式为 中
中 与
与 间形成的化学键为
间形成的化学键为(2)将
 置于
置于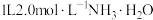 溶液中,通入
溶液中,通入 ,
, 转化为
转化为 的离子方程式为:
的离子方程式为:

 ,
, 的溶解速率为
的溶解速率为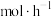 。
。(3)氨与
 形成配合物有助于
形成配合物有助于 溶解。常温下,向
溶解。常温下,向 饱和溶液(含足量
饱和溶液(含足量 固体)中滴加氨水,主要存在以下平衡:
固体)中滴加氨水,主要存在以下平衡:(i)
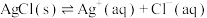
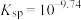
(ii)
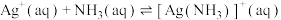
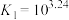
(iii)

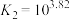
①下列有关说法中,正确的有
A.加少量水稀释,平衡后溶液中
 、
、 均减小
均减小B.随
 增大,反应ⅱ平衡正向移动,
增大,反应ⅱ平衡正向移动, 增大
增大C.随
 增大,
增大, 不变
不变D.溶液中存在
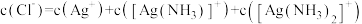
②反应


 、
、 、
、 表示)。
表示)。(4)向
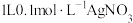 溶液中通入足量
溶液中通入足量 得到澄清溶液(设溶液体积不变),溶液中
得到澄清溶液(设溶液体积不变),溶液中 、
、 、
、 的物质的量分数
的物质的量分数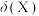 随
随 的变化如图所示。
的变化如图所示。
已知溶液中
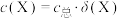 ,
, 。
。①
 点溶液中
点溶液中
 。
。②计算
 点溶液中
点溶液中 的转化率
的转化率 )。
)。
您最近半年使用:0次
2024-04-03更新
|
761次组卷
|
2卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期中测试化学试题
名校
解题方法
5 . 为研究二氧化硫的性质,某兴趣小组设计如图所示装置进行实验。将少量 溶液缓慢推入
溶液缓慢推入 粉末处,发生反应。下列说法不正确的是
粉末处,发生反应。下列说法不正确的是

 溶液缓慢推入
溶液缓慢推入 粉末处,发生反应。下列说法不正确的是
粉末处,发生反应。下列说法不正确的是
A.气球先变大后变小,体现了 的水溶性 的水溶性 |
B.石蕊试纸变红,说明 溶于水显酸性 溶于水显酸性 |
C.品红溶液褪色,体现了 的还原性 的还原性 |
D.加热褪色后的溶液又变红,说明 与品红生成不稳定的无色物质 与品红生成不稳定的无色物质 |
您最近半年使用:0次
2024-04-03更新
|
470次组卷
|
2卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期中测试化学试题
解题方法
6 . 下列有关实验操作正确的是
A.在待测液中加入NaOH溶液,加热试管,用玻璃棒粘住湿润的蓝色石蕊试纸放在试管口,试纸变红,说明溶液中含有NH |
| B.稀释浓H2SO4时,应将蒸馏水沿玻璃棒缓慢注入浓H2SO4中 |
C.向溶液中加入盐酸,将产生的气体通入澄清石灰水,石灰水变浑浊,说明溶液中含有CO 或HCO 或HCO |
| D.中和反应反应热的测定主要玻璃仪器有温度计、烧杯、环形玻璃搅拌器,玻璃搅拌器不能用金属制品代替 |
您最近半年使用:0次
7 . 下列叙述不正确的是
| A.电热水器用镁棒防止内胆腐蚀,原理是牺牲阳极的阴极保护法 |
| B.用稀硫酸和锌粒制取H2时,加几滴CuSO4溶液以加快反应速率 |
| C.化学与人体健康及环境保护息息相关,掩埋废旧电池会造成环境污染,因此要合理处理废旧电池有利于保护环境和资源再利用 |
D.研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如图所示),由图可知:雾和霾的分散剂相同,雾霾中含有硝酸铵和硫酸铵, NH3是形成无机颗粒物的催化剂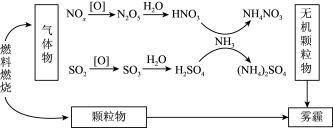 |
您最近半年使用:0次
名校
解题方法
8 . 有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。在101 kPa下,1 g氢气完全燃烧生成液态水放出142.9 kJ的热量。
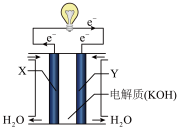
(1)请写出表示氢气燃烧热的热化学方程式__________________ 。
(2)将上述反应设计成下图所示的原电池,其中Y为________ 极(填“正”或“负”),该极电极反应式为___________________ 。

(1)请写出表示氢气燃烧热的热化学方程式
(2)将上述反应设计成下图所示的原电池,其中Y为
您最近半年使用:0次
名校
解题方法
9 . 凉山雷波等地盛产脐橙。从脐橙果皮中提取的橙油具有抗菌抑菌、抗氧化、祛痰平喘等多种作用,常用于医药、食品加工、日化等多个领域。橙油的主要成分是柠檬烯,其结构简式如下。下列有关柠檬烯的说法正确的是
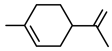
| A.分子式为C10H18 |
| B.可发生加成、取代、氧化反应 |
| C.一氯代物有7种(不考虑立体异构) |
| D.与1,3-丁二烯(CH2=CH-CH=CH2)互为同系物 |
您最近半年使用:0次
2024-03-26更新
|
817次组卷
|
3卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期中测试化学试题
名校
10 . 太空探索永无止境,探索浩瀚宇宙是全人类的共同梦想。回答下列问题:
(1)建造太空电梯的材料为单质碳。假设太空电梯重达
 ,则碳原子的物质的量为
,则碳原子的物质的量为(2)太阳阵闪是指当太阳内部温度升到
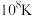 时,3个
时,3个 发生核聚变生成
发生核聚变生成 。
。 发生氦闪可生成
发生氦闪可生成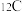 的质量为
的质量为(3)月球上有丰富的
 (摩尔质量为
(摩尔质量为 )气体核聚变发电燃料,我国每天用电量只需
)气体核聚变发电燃料,我国每天用电量只需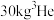 气体,则由
气体,则由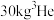 组成的气体在标准状况下所占的体积为
组成的气体在标准状况下所占的体积为(4)发射嫦娥四号用的是长征三号乙运载火箭,该火箭推进剂[燃料为
 和助燃剂为
和助燃剂为 ]共
]共 ,点燃时二者恰好反应,发生的反应为
,点燃时二者恰好反应,发生的反应为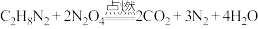 ,则其中燃料
,则其中燃料 的质量为
的质量为
您最近半年使用:0次



