解题方法
1 . 下列情况中反应速率不加快 的是
| A.将在空气中燃着的木条插入盛有纯氧的集气瓶中 |
| B.用煤粉代替煤块燃烧 |
C.增大合成氨反应(N2+3H2 2NH3)体系的压强 2NH3)体系的压强 |
| D.用0.01 mol·L-1的盐酸代替1 mol·L-1的盐酸与铁反应制取氢气 |
您最近一年使用:0次
名校
2 . 常温下,亚硝酸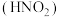 和连二次硝酸
和连二次硝酸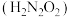 的电离常数数值如下表所示:
的电离常数数值如下表所示:
下列分析正确的是
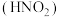 和连二次硝酸
和连二次硝酸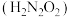 的电离常数数值如下表所示:
的电离常数数值如下表所示:| 化学式 | 电离平衡常数 |
 | 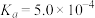 |
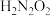 | 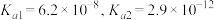 |
A.加水稀释亚硝酸,亚硝酸的电离程度增大, 也增大 也增大 |
B.常温下, 溶液中存在水解平衡,其 溶液中存在水解平衡,其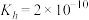 |
C.pH相等的 溶液和 溶液和 溶液中: 溶液中: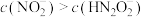 |
D.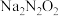 溶液中离子浓度大小顺序为 溶液中离子浓度大小顺序为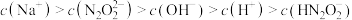 |
您最近一年使用:0次
2022-12-03更新
|
267次组卷
|
2卷引用:河北省卢龙县第二高级中学2021-2022学年高二上学期期中考试化学试题
名校
解题方法
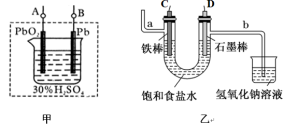
3 . 图甲为铅蓄电池,图乙为电解饱和食盐水装置图。某实验小组想用图甲作电源并利用图乙装置电解饱和食盐水制NaOH溶液。已知铅蓄电池的工作原理为:PbO2 + Pb + 2H2SO4 2PbSO4 + 2H2O
2PbSO4 + 2H2O
请回答下列问题:
(1)图甲铅蓄电的正极是_______ (填“A”或“B”),该极的电极反应式为_______ 。
(2)A电极应与乙图中_______ (填“C”或“D”)电极相连,该电极的电极反应式为_______ 。
(3)乙图中氢氧化钠溶液的作用是_______ ,反应的离子方程式为_______ 。
(4)该实验小组还利用实验过程中产生的a、b两种气体和NaOH溶液设计成图丙所示燃料电池,写出M电极的电极反应式_______ 。该燃料电池工作一段时间后溶液的pH_______ (填“减小”、“增大”或“不变”)。
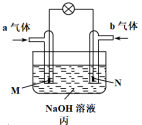
(5)铅蓄电池工作一段时间后,需要充电,充电时阴极反应的电极反应式为_______ 。
 2PbSO4 + 2H2O
2PbSO4 + 2H2O
请回答下列问题:
(1)图甲铅蓄电的正极是
(2)A电极应与乙图中
(3)乙图中氢氧化钠溶液的作用是
(4)该实验小组还利用实验过程中产生的a、b两种气体和NaOH溶液设计成图丙所示燃料电池,写出M电极的电极反应式

(5)铅蓄电池工作一段时间后,需要充电,充电时阴极反应的电极反应式为
您最近一年使用:0次
名校
解题方法
4 . 填空。
(1)写出相对分子质量为58的烃具有支链的同分异构体的结构简式为_______ ,其名称为_______ 。
(2)写出苯与液溴在铁粉作用下反应的化学方程式_______ ,该反应属于_______ (填反应类型)。实验室制得的溴苯中常含有杂质溴,可用NaOH稀溶液除去,其离子反应方程式为_______ 。
(3)乙烯是有机化工的一个重要原料,乙烯的结构式为_______ ,乙烯和HCl发生加成反应的化学方程式为_______ ,其加成产物1mol和足量的Cl2在光照下发生取代反应,最多消耗Cl2的物质的量是_______ 。
(1)写出相对分子质量为58的烃具有支链的同分异构体的结构简式为
(2)写出苯与液溴在铁粉作用下反应的化学方程式
(3)乙烯是有机化工的一个重要原料,乙烯的结构式为
您最近一年使用:0次
名校
5 . 可逆反应2SO2+O2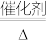 2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
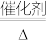 2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是| A.升高温度平衡向正反应方向移动 |
| B.增大压强SO2的转化率增大 |
| C.加入催化剂平衡不发生移动,但反应速率加快 |
| D.只增大SO2浓度平衡不移动 |
您最近一年使用:0次
名校
解题方法
6 . 关于下图装置的说法错误的是
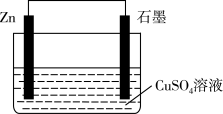
| A.电流由Zn电极经外线路流向石墨电极 |
| B.溶液中Cu2+由负极移向正极 |
| C.工作一段时间,溶液中离子数目减少 |
| D.负极电极反应式为:Zn-2e-=Zn2+ |
您最近一年使用:0次
2022-11-03更新
|
153次组卷
|
2卷引用:河北省唐山市滦南县第一中学2020-2021学年高一下学期期中考试化学试题
解题方法
7 . 生活处处有化学,制作馒头、面包等所用的发酵粉,主要成分是由Na2CO3、NaHCO3和固体有机酸混合而成的,晓露同学猜想:发酵粉加热或加水时都能产生CO2,并进行如下实验:
(1)将Na2CO3和NaHCO3分别加热,能产生CO2的物质是_______ (填化学式)。
(2)晓露同学用如图所示装置探究发酵粉加水能否产生CO2,并探究过氧化钠是否可作呼吸面具的供氧剂。请回答:

①A装置中仪器a的名称是_______ 。
②观察到B装置产生白色浑浊,写出反应的化学方程式_______ 。
③实验证实发酵粉加水也能产生CO2,主要原因是_______ 。
④C装置中浓硫酸的作用是_______ 。
⑤收集D装置产生的气体,要验证它是氧气,方法是_______ 。
(1)将Na2CO3和NaHCO3分别加热,能产生CO2的物质是
(2)晓露同学用如图所示装置探究发酵粉加水能否产生CO2,并探究过氧化钠是否可作呼吸面具的供氧剂。请回答:

①A装置中仪器a的名称是
②观察到B装置产生白色浑浊,写出反应的化学方程式
③实验证实发酵粉加水也能产生CO2,主要原因是
④C装置中浓硫酸的作用是
⑤收集D装置产生的气体,要验证它是氧气,方法是
您最近一年使用:0次
2022-09-16更新
|
222次组卷
|
2卷引用:河北省石家庄市元氏县第四中学2021-2022学年高一上学期期中考试化学试题
名校
解题方法
8 . 将磷肥生产中产生的副产物石膏( )转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用角度还是从环境保护角度看都具有重要意义。石膏转化为硫酸钾和氯化钙的工艺流程示意图如图。
)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用角度还是从环境保护角度看都具有重要意义。石膏转化为硫酸钾和氯化钙的工艺流程示意图如图。
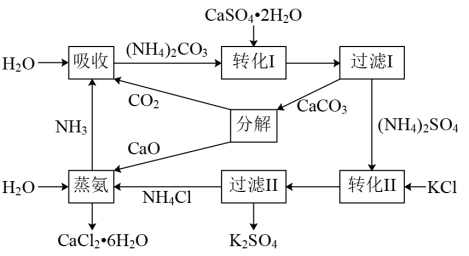
回答下列问题:
(1)该工艺流程中所用的原料除 、
、 外,还需要
外,还需要_______ (填化学式,不考虑损耗)。
(2)室温下, 溶液的
溶液的
_______ (填“>”、“<”或“=”)7,用离子方程式解释其原因:_______ 。
(3) 的
的 溶液中各离子浓度从大到小的顺序是
溶液中各离子浓度从大到小的顺序是_______ 。
(4)转化Ⅰ是将难溶的 转化为更难溶的
转化为更难溶的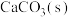 ,用离子方程式表示该沉淀转化过程:
,用离子方程式表示该沉淀转化过程:_______ ,该化学平衡的平衡常数
_______ 。将一定量的 加入过量的
加入过量的 悬浊液中,充分反应后,测得溶液中
悬浊液中,充分反应后,测得溶液中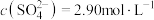 ,此时溶液中的
,此时溶液中的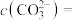
_______  。[已知:
。[已知: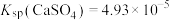 、
、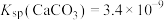 ]
]
(5)已知不同温度下 在100g水中达到饱和时溶解的量如下表:
在100g水中达到饱和时溶解的量如下表:
75℃的 饱和溶液482g冷却到20℃,可析出
饱和溶液482g冷却到20℃,可析出 晶体
晶体_______ g。
 )转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用角度还是从环境保护角度看都具有重要意义。石膏转化为硫酸钾和氯化钙的工艺流程示意图如图。
)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用角度还是从环境保护角度看都具有重要意义。石膏转化为硫酸钾和氯化钙的工艺流程示意图如图。
回答下列问题:
(1)该工艺流程中所用的原料除
 、
、 外,还需要
外,还需要(2)室温下,
 溶液的
溶液的
(3)
 的
的 溶液中各离子浓度从大到小的顺序是
溶液中各离子浓度从大到小的顺序是(4)转化Ⅰ是将难溶的
 转化为更难溶的
转化为更难溶的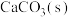 ,用离子方程式表示该沉淀转化过程:
,用离子方程式表示该沉淀转化过程:
 加入过量的
加入过量的 悬浊液中,充分反应后,测得溶液中
悬浊液中,充分反应后,测得溶液中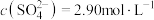 ,此时溶液中的
,此时溶液中的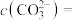
 。[已知:
。[已知: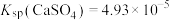 、
、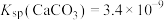 ]
](5)已知不同温度下
 在100g水中达到饱和时溶解的量如下表:
在100g水中达到饱和时溶解的量如下表:| 温度/℃ | 0 | 20 | 40 | 60 | 75 |
 溶解的量/g 溶解的量/g | 7.7 | 11.1 | 14.7 | 18.1 | 20.5 |
 饱和溶液482g冷却到20℃,可析出
饱和溶液482g冷却到20℃,可析出 晶体
晶体
您最近一年使用:0次
解题方法
9 .  重整技术是实现碳中和的一种
重整技术是实现碳中和的一种 的利用技术。该过程中发生的反应为
的利用技术。该过程中发生的反应为
 。回答下列问题:
。回答下列问题:
(1)_______ (填“高温”、“低温”或“任意温度”)有利于该反应自发进行,该反应的反应物键能总和_______ (填“大于”或“小于”)生成物键能总和。
(2)若向一容积可变的密闭容器中充入一定量的 和
和 进行反应,保持压强不变,反应后
进行反应,保持压强不变,反应后 的平衡转化率随温度(T)的变化如图1所示。若达到化学平衡状态a时,仅改变压强,反应又重新达到平衡状态b,则压强
的平衡转化率随温度(T)的变化如图1所示。若达到化学平衡状态a时,仅改变压强,反应又重新达到平衡状态b,则压强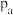
_______ (填“>”、“<”或“=”)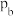 ,判断的理由是
,判断的理由是_______ 。

(3) ℃下,向体积为4L的恒容密闭容器中,充入0.2mol
℃下,向体积为4L的恒容密闭容器中,充入0.2mol 和0.5mol
和0.5mol 进行反应,反应达到平衡后,测得反应后混合气体的总压强为反应前的
进行反应,反应达到平衡后,测得反应后混合气体的总压强为反应前的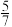 ,此时,
,此时, 的体积分数为
的体积分数为_______ , 的平衡转化率为
的平衡转化率为_______ ,平衡常数K=_______ 。
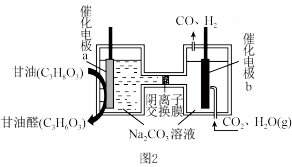
(4)我国科学家设计了一种电解装置如图2所示(电极均为惰性电极),能将二氧化碳、 转化成合成气CO和
转化成合成气CO和 ,同时获得甘油醛。则催化电极b为
,同时获得甘油醛。则催化电极b为_______ 极,催化电极a产生甘油醛的电极反应式为_______ 。
 重整技术是实现碳中和的一种
重整技术是实现碳中和的一种 的利用技术。该过程中发生的反应为
的利用技术。该过程中发生的反应为
 。回答下列问题:
。回答下列问题:(1)
(2)若向一容积可变的密闭容器中充入一定量的
 和
和 进行反应,保持压强不变,反应后
进行反应,保持压强不变,反应后 的平衡转化率随温度(T)的变化如图1所示。若达到化学平衡状态a时,仅改变压强,反应又重新达到平衡状态b,则压强
的平衡转化率随温度(T)的变化如图1所示。若达到化学平衡状态a时,仅改变压强,反应又重新达到平衡状态b,则压强
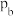 ,判断的理由是
,判断的理由是
(3)
 ℃下,向体积为4L的恒容密闭容器中,充入0.2mol
℃下,向体积为4L的恒容密闭容器中,充入0.2mol 和0.5mol
和0.5mol 进行反应,反应达到平衡后,测得反应后混合气体的总压强为反应前的
进行反应,反应达到平衡后,测得反应后混合气体的总压强为反应前的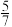 ,此时,
,此时, 的体积分数为
的体积分数为 的平衡转化率为
的平衡转化率为(4)我国科学家设计了一种电解装置如图2所示(电极均为惰性电极),能将二氧化碳、
 转化成合成气CO和
转化成合成气CO和 ,同时获得甘油醛。则催化电极b为
,同时获得甘油醛。则催化电极b为
您最近一年使用:0次
10 . 已知:25℃时,①亚硫酸( )的电离平衡常数为
)的电离平衡常数为 ,
, ;②次氯酸(HClO)的电离平衡常数为
;②次氯酸(HClO)的电离平衡常数为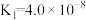 ;③碳酸(
;③碳酸( )的电离平衡常数为
)的电离平衡常数为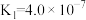 ,
, 。回答下列问题:
。回答下列问题:
(1)HClO的电离方程式为_______ 。
(2)上述三种酸由强到弱的顺序为_______ (填分子式)。
(3)向 溶液中加入
溶液中加入 溶液时,溶液中
溶液时,溶液中
_______ (填“增大”、“减小”或“不变”,下同),
_______ 。
(4)足量的 溶液和
溶液和 溶液发生反应的主要离子方程式为
溶液发生反应的主要离子方程式为_______ ;足量的 溶液中加入NaClO溶液发生反应的离子方程式为
溶液中加入NaClO溶液发生反应的离子方程式为_______ 。
(5)向 的HClO溶液中滴加等体积的一定浓度的稀硫酸,此时测得溶液中的
的HClO溶液中滴加等体积的一定浓度的稀硫酸,此时测得溶液中的 ,则溶液中
,则溶液中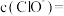
_______  。
。
 )的电离平衡常数为
)的电离平衡常数为 ,
, ;②次氯酸(HClO)的电离平衡常数为
;②次氯酸(HClO)的电离平衡常数为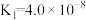 ;③碳酸(
;③碳酸( )的电离平衡常数为
)的电离平衡常数为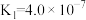 ,
, 。回答下列问题:
。回答下列问题:(1)HClO的电离方程式为
(2)上述三种酸由强到弱的顺序为
(3)向
 溶液中加入
溶液中加入 溶液时,溶液中
溶液时,溶液中

(4)足量的
 溶液和
溶液和 溶液发生反应的主要离子方程式为
溶液发生反应的主要离子方程式为 溶液中加入NaClO溶液发生反应的离子方程式为
溶液中加入NaClO溶液发生反应的离子方程式为(5)向
 的HClO溶液中滴加等体积的一定浓度的稀硫酸,此时测得溶液中的
的HClO溶液中滴加等体积的一定浓度的稀硫酸,此时测得溶液中的 ,则溶液中
,则溶液中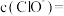
 。
。
您最近一年使用:0次



