名校
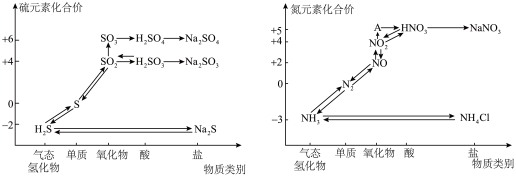
1 . 硫、氮的氧化物都会引起环境问题,越来越引起人们的重视.如图是硫、氮元素的各种价态与物质类别的对应关系:
(1)从硫元素的化合价变化的角度判断,图中只有还原性的含硫化合物为________ (填化学式);
(2)若将 通入紫色石蕊溶液中可观察到的现象为
通入紫色石蕊溶液中可观察到的现象为________________ ;
(3)根据A对应的化合价和物质类别,A为________ (写分子式);
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择________ ,反
应的离子方程式为________________ ;
(5)工业生产中利用氨水吸收 和
和 ,流程如图所示:
,流程如图所示: 被吸收过程的离子方程式是
被吸收过程的离子方程式是________________ ;
(6)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下: ;
; ;若用某
;若用某 溶液恰好完全吸收含
溶液恰好完全吸收含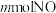 和
和 的大气污染物,则
的大气污染物,则 的物质的量为
的物质的量为________  .若所得溶液中
.若所得溶液中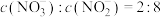 ,则原混合气体中
,则原混合气体中 和
和 物质的量之比
物质的量之比
________ 。
(1)从硫元素的化合价变化的角度判断,图中只有还原性的含硫化合物为
(2)若将
 通入紫色石蕊溶液中可观察到的现象为
通入紫色石蕊溶液中可观察到的现象为(3)根据A对应的化合价和物质类别,A为
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择
应的离子方程式为
(5)工业生产中利用氨水吸收
 和
和 ,流程如图所示:
,流程如图所示: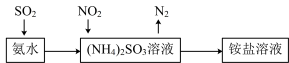
 被吸收过程的离子方程式是
被吸收过程的离子方程式是(6)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
 ;
; ;若用某
;若用某 溶液恰好完全吸收含
溶液恰好完全吸收含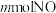 和
和 的大气污染物,则
的大气污染物,则 的物质的量为
的物质的量为 .若所得溶液中
.若所得溶液中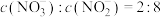 ,则原混合气体中
,则原混合气体中 和
和 物质的量之比
物质的量之比
您最近一年使用:0次
名校
解题方法
2 . I.有一块镀铜的铁制品,已严重锈蚀[铜锈成分视为 ],铁锈成分视为
],铁锈成分视为 ],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。
],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。
(1)气体甲的成分是___________ (填化学式),固体乙的成分是___________ (填名称)。
(2)铁发生的反应属于四种基本反应类型中的___________ 。
(3)滤液丙的颜色可能是___________(选填编号)。
(4)确认滤液丙中是否含有亚铁离子,适宜的试剂是___________(选填编号)。
Ⅱ.铁与不同浓度硝酸反应时主要还原产物不同。现将过量铁与一定浓度的硝酸充分反应,测得消耗的铁与被还原的硝酸的物质的量之比为 。
。
(5)假若反应生成的还原产物只有一种,则还原产物是___________ 。
(6)所得溶液与碳酸氢铵溶液混合可获得碳酸亚铁沉淀,同时有气体生成。写出反应生成碳酸亚铁的离子方程式___________ 。
 ],铁锈成分视为
],铁锈成分视为 ],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。
],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。(1)气体甲的成分是
(2)铁发生的反应属于四种基本反应类型中的
(3)滤液丙的颜色可能是___________(选填编号)。
| A.棕黄色 | B.蓝色 | C.浅绿色 | D.无色 |
A. 溶液 溶液 | B.NaOH溶液 |
C.KSCN溶液和 溶液 溶液 | D. 淀粉试纸 淀粉试纸 |
Ⅱ.铁与不同浓度硝酸反应时主要还原产物不同。现将过量铁与一定浓度的硝酸充分反应,测得消耗的铁与被还原的硝酸的物质的量之比为
 。
。(5)假若反应生成的还原产物只有一种,则还原产物是
(6)所得溶液与碳酸氢铵溶液混合可获得碳酸亚铁沉淀,同时有气体生成。写出反应生成碳酸亚铁的离子方程式
您最近一年使用:0次
名校
解题方法
3 . 化学电池的发明,改变了人们的生活。___________ 。
(2)电流的流动方向是___________ ;能证明化学能转化为电能的实验现象是___________ 。
(3)常见的锌锰干电池构造示意图如下。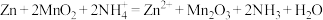 。
。
①该电池属于___________ (填“一次”、“二次”或“燃料”)电池。
②MnO2发生___________ (填“氧化”或“还原”)反应。
(2)电流的流动方向是
(3)常见的锌锰干电池构造示意图如下。
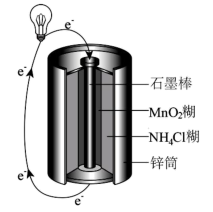
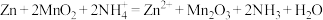 。
。①该电池属于
②MnO2发生
您最近一年使用:0次
名校
解题方法
4 . 连线题:___________
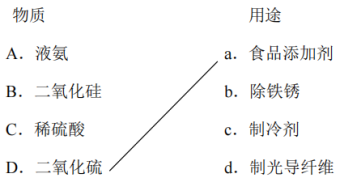
您最近一年使用:0次
5 . Ⅰ. 、
、 、
、 都是重要的能源物质,也是重要的化工原料。
都是重要的能源物质,也是重要的化工原料。
(1)下列事实能说明 分子呈正四面体结构的是_______(填字母)。
分子呈正四面体结构的是_______(填字母)。
(2)甲烷与下列烃的通式相同的是_______ (填字母)。_______ 。
②写出装置C中 与
与 反应生成氯仿(
反应生成氯仿( )的化学方程式
)的化学方程式_______ 。
③若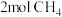 与
与 发生取代反应,测得生成4种有机取代产物的物质的量相等,则产物中最多的物质,其物质的量是
发生取代反应,测得生成4种有机取代产物的物质的量相等,则产物中最多的物质,其物质的量是_______ mol。
Ⅱ.用 还原
还原 能有效促进“碳中和”,反应的化学方程式为
能有效促进“碳中和”,反应的化学方程式为 。
。
(4)反应过程中的能量变化如下图所示。若生成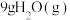 ,该反应会
,该反应会_____ (填“放出”或“吸收”)______ KJ热量。(用含有 、
、 的式子表示)
的式子表示) 和
和 ,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题: 的浓度随时间变化曲线为
的浓度随时间变化曲线为_______ (填“a”、“b”或“c”),在M点,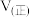
_______ 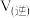 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
②2min时,反应速率改变的原因可能是_______ 。
A.升高温度 B.降低温度 C.充入一定量的 D.加入催化剂
D.加入催化剂
 、
、 、
、 都是重要的能源物质,也是重要的化工原料。
都是重要的能源物质,也是重要的化工原料。(1)下列事实能说明
 分子呈正四面体结构的是_______(填字母)。
分子呈正四面体结构的是_______(填字母)。A. 分子的4个C—H共价键键长相等 分子的4个C—H共价键键长相等 | B. 分子中每个键角都是109°28′ 分子中每个键角都是109°28′ |
C.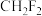 没有同分异构体 没有同分异构体 | D. 分子的沸点高于 分子的沸点高于 |
(2)甲烷与下列烃的通式相同的是
a. b.
b.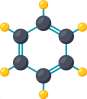 c.
c.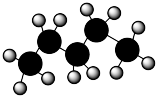 d.
d.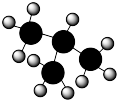
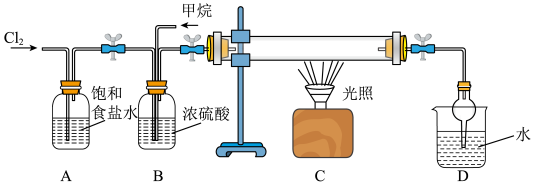
②写出装置C中
 与
与 反应生成氯仿(
反应生成氯仿( )的化学方程式
)的化学方程式③若
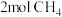 与
与 发生取代反应,测得生成4种有机取代产物的物质的量相等,则产物中最多的物质,其物质的量是
发生取代反应,测得生成4种有机取代产物的物质的量相等,则产物中最多的物质,其物质的量是Ⅱ.用
 还原
还原 能有效促进“碳中和”,反应的化学方程式为
能有效促进“碳中和”,反应的化学方程式为 。
。(4)反应过程中的能量变化如下图所示。若生成
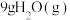 ,该反应会
,该反应会 、
、 的式子表示)
的式子表示)
 和
和 ,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题: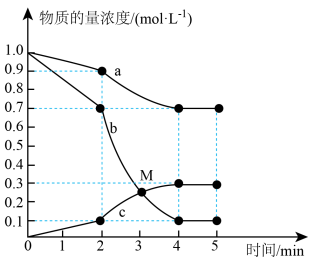
 的浓度随时间变化曲线为
的浓度随时间变化曲线为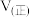
 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。②2min时,反应速率改变的原因可能是
A.升高温度 B.降低温度 C.充入一定量的
 D.加入催化剂
D.加入催化剂
您最近一年使用:0次
名校
6 . 按要求回答下列问题:
(1)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是_______。
(2)下图是一氧化碳和氧在钌催化剂的表面形成化学键的过程。下列说法正确的是_______。
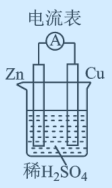
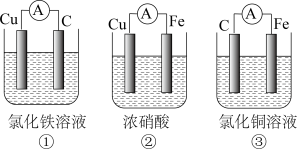
(3)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是_______ (填序号)。_______ 。
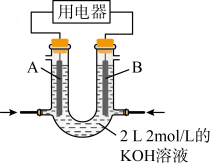
(4)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。_______ (填“A”或“B”)处电极入口通甲烷,其电极反应式为_______ 。当消耗甲烷的体积为33.6 L(标准状况)时,假设电池的能量转化率为80%,导线中转移电子的物质的量为_______ 。
(1)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是_______。
A.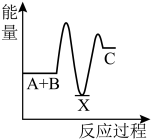 | B.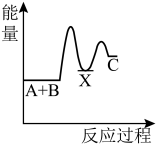 | C.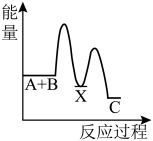 | D.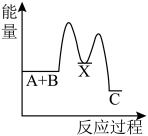 |
(2)下图是一氧化碳和氧在钌催化剂的表面形成化学键的过程。下列说法正确的是_______。
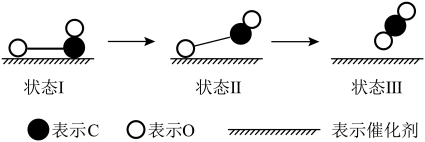
A. 和 和 均为酸性氧化物 均为酸性氧化物 | B.该过程中, 先断键成C和O 先断键成C和O |
| C.状态I到状态Ⅲ为放热过程 | D.图示表示 和 和 反应生成 反应生成 的过程 的过程 |
(3)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是
(4)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
您最近一年使用:0次
名校
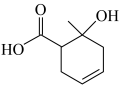
7 . I.某有机物的结构简式如图所示___________ 。
Ⅱ.某烷烃1mol完全燃烧消耗氧气为179.2L(标况)
(2)该烷烃的分子式为___________ 。
(3)该烷烃的结构简式有____________ ,它们中一氯代物只有一种的名称是__________ 。
(4)与该烷烃同系物且比该烷烃多一个碳,主链有4个碳的同分异构体有(写结构简式)_________ 。
(5)与该烷烃同系物且比该烷烃少一个碳,它二氯代物共有___________ 种。
Ⅱ.某烷烃1mol完全燃烧消耗氧气为179.2L(标况)
(2)该烷烃的分子式为
(3)该烷烃的结构简式有
(4)与该烷烃同系物且比该烷烃多一个碳,主链有4个碳的同分异构体有(写结构简式)
(5)与该烷烃同系物且比该烷烃少一个碳,它二氯代物共有
您最近一年使用:0次
名校
8 . 有下列几种物质:① 晶体;②
晶体;② ;③
;③ 溶液;④
溶液;④ ;⑤
;⑤ 溶液;⑥
溶液;⑥ (酒精);⑦
(酒精);⑦ ;⑧氨水;⑨饱和
;⑧氨水;⑨饱和 溶液。根据要求回答下列问题:
溶液。根据要求回答下列问题:
1.上述各物质属于强电解质的是___________ (填物质编号,下同);属于非电解质的是___________ 。
2.写出少量④通入⑤中反应的离子方程式:___________ ;③和⑧在水溶液中反应的离子方程式:___________ 。
3.将⑨加入到沸水中,继续加热溶液呈红褐色,制得 胶体,该反应的离子方程式:
胶体,该反应的离子方程式:___________ 。
4.向③中加入⑤至溶液中恰好呈中性,写出该反应的离子方程式:___________ 。
 晶体;②
晶体;② ;③
;③ 溶液;④
溶液;④ ;⑤
;⑤ 溶液;⑥
溶液;⑥ (酒精);⑦
(酒精);⑦ ;⑧氨水;⑨饱和
;⑧氨水;⑨饱和 溶液。根据要求回答下列问题:
溶液。根据要求回答下列问题:1.上述各物质属于强电解质的是
2.写出少量④通入⑤中反应的离子方程式:
3.将⑨加入到沸水中,继续加热溶液呈红褐色,制得
 胶体,该反应的离子方程式:
胶体,该反应的离子方程式:4.向③中加入⑤至溶液中恰好呈中性,写出该反应的离子方程式:
您最近一年使用:0次
名校
9 . 按照要求,回答下列问题:
(1)硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是___________ (填序号)。
①玻璃 ②陶瓷 ③水晶 ④硅芯片 ⑤水泥 ⑥光导纤维 ⑦钻石
(2)下列变化中属于吸热反应的是___________ 。
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③甲烷在氧气中的燃烧反应 ④Ba(OH)2·8H2O与NH4Cl反应 ⑤煅烧石灰石 ⑥NH4NO3固体溶于水
(3)已知部分共价键的键能如下:E(N≡N)=946 kJ/mol,E(H-H)=436 kJ/mol,E(N-H)=391kJ/mol。根据以上数据写出工业合成氨的热化学反应方程式:___________ 。
(4)在25℃、101 kPa下,液态甲醇(CH3OH))的燃烧热为726.5 kJ/mol,已知:H2O (l)=H2O(g) △H=+44 kJ/mol,写出甲醇燃烧生成水蒸气的热化学方程式___________ 。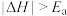 。在右图中补充该反应过程的能量变化示意图
。在右图中补充该反应过程的能量变化示意图___________ 。
(1)硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是
①玻璃 ②陶瓷 ③水晶 ④硅芯片 ⑤水泥 ⑥光导纤维 ⑦钻石
(2)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③甲烷在氧气中的燃烧反应 ④Ba(OH)2·8H2O与NH4Cl反应 ⑤煅烧石灰石 ⑥NH4NO3固体溶于水
(3)已知部分共价键的键能如下:E(N≡N)=946 kJ/mol,E(H-H)=436 kJ/mol,E(N-H)=391kJ/mol。根据以上数据写出工业合成氨的热化学反应方程式:
(4)在25℃、101 kPa下,液态甲醇(CH3OH))的燃烧热为726.5 kJ/mol,已知:H2O (l)=H2O(g) △H=+44 kJ/mol,写出甲醇燃烧生成水蒸气的热化学方程式
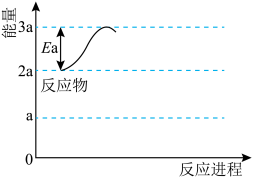
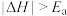 。在右图中补充该反应过程的能量变化示意图
。在右图中补充该反应过程的能量变化示意图
您最近一年使用:0次
名校
10 . 回答下列问题:
(1)一定量的乙醇和O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物分别经过浓硫酸和碱石灰,浓硫酸增重5.4g,碱石灰增重6.6g。求乙醇和氧气物质的量分别是___________ 、___________ 。
(2)若将0.6mol乙醇与11.5g金属钠充分反应,则标况下生成气体的体积是___________ 。
(1)一定量的乙醇和O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物分别经过浓硫酸和碱石灰,浓硫酸增重5.4g,碱石灰增重6.6g。求乙醇和氧气物质的量分别是
(2)若将0.6mol乙醇与11.5g金属钠充分反应,则标况下生成气体的体积是
您最近一年使用:0次



