名校
1 . 回答下列问题:
(1)0.5 molNH3的质量是___________ ,在标准状况下的体积为___________ ,将此气体溶于100 mL水中得到溶液,且溶液密度为a g/mL,则该溶液的物质的量浓度为___________ ;(已知水的密度为1 g/mL)
(2)7.8g Na2X中含有Na+ 0.2 mol,则Na2X的摩尔质量为___________ ;
(3)实验室需要1.0 mol/L NaOH溶液240 mL,根据配制溶液的过程,回答下列问题:
①为完成此溶液配制实验需要的仪器除托盘天平(带砝码)、药匙、烧杯、玻璃棒、量筒、胶头滴管这六种仪器外,还缺少的必要玻璃仪器为___________ (填名称)。
②根据计算用托盘天平称取NaOH的质量为___________ g。
③若取5 mL该溶液用水稀释到100 mL,所得溶液中Na+的物质的量浓度为___________ mol/L。
(1)0.5 molNH3的质量是
(2)7.8g Na2X中含有Na+ 0.2 mol,则Na2X的摩尔质量为
(3)实验室需要1.0 mol/L NaOH溶液240 mL,根据配制溶液的过程,回答下列问题:
①为完成此溶液配制实验需要的仪器除托盘天平(带砝码)、药匙、烧杯、玻璃棒、量筒、胶头滴管这六种仪器外,还缺少的必要玻璃仪器为
②根据计算用托盘天平称取NaOH的质量为
③若取5 mL该溶液用水稀释到100 mL,所得溶液中Na+的物质的量浓度为
您最近一年使用:0次
2 . 酸、碱、盐都是电解质,常温下,有以下电解质溶液:
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
已知: 的电离常数
的电离常数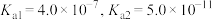
(1)用化学用语解释④呈酸性的原因:_______
(2) 的溶液①中由水电离出的
的溶液①中由水电离出的 为
为_______
(3)浓度均为 的上述7种溶液,
的上述7种溶液,  由大到小为
由大到小为_______
(4)在⑥溶液中下列关系成立的是_______
(5)若某浓度的⑥和⑦的混合溶液中 ,该溶液的
,该溶液的
_______
(6)将 的①溶液与
的①溶液与 的③溶液混合,若所得混合溶液的
的③溶液混合,若所得混合溶液的 ,则①和②溶液的体积比为
,则①和②溶液的体积比为_______
①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
已知:
 的电离常数
的电离常数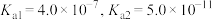
(1)用化学用语解释④呈酸性的原因:
(2)
 的溶液①中由水电离出的
的溶液①中由水电离出的 为
为(3)浓度均为
 的上述7种溶液,
的上述7种溶液,  由大到小为
由大到小为(4)在⑥溶液中下列关系成立的是
A.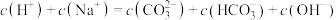 |
B.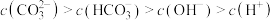 |
C. |
D.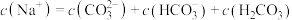 |
 ,该溶液的
,该溶液的
(6)将
 的①溶液与
的①溶液与 的③溶液混合,若所得混合溶液的
的③溶液混合,若所得混合溶液的 ,则①和②溶液的体积比为
,则①和②溶液的体积比为
您最近一年使用:0次
名校
解题方法
3 . 弱电解质的电离
(1)写出碳酸氢钠的电离方程式_______ 。
(2)写出氢氧化铝的电离方程式_______ 。
(3)已知硼酸与足量氢氧化钠溶液反应的离子方程式为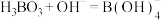 ,则硼酸的电离方程式为
,则硼酸的电离方程式为_______ 。
(4)已知酸性: ,写出下列反应的离子方程式
,写出下列反应的离子方程式
①足量 通入
通入 溶液
溶液_______ 。
②足量 与
与 溶液混合
溶液混合_______ 。
(1)写出碳酸氢钠的电离方程式
(2)写出氢氧化铝的电离方程式
(3)已知硼酸与足量氢氧化钠溶液反应的离子方程式为
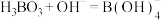 ,则硼酸的电离方程式为
,则硼酸的电离方程式为(4)已知酸性:
 ,写出下列反应的离子方程式
,写出下列反应的离子方程式①足量
 通入
通入 溶液
溶液②足量
 与
与 溶液混合
溶液混合
您最近一年使用:0次
名校
解题方法
4 . 化学平衡图像分析
(1)对于反应
 ,
,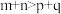
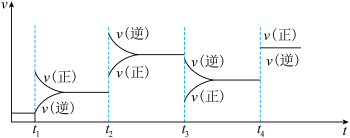
上图中各时间点改变的条件是
_______ ;
_______ ;
_______ 。
(2)可逆反应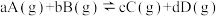
 ,同时符合下列两图中各曲线,
,同时符合下列两图中各曲线,

则
_______ 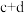

_______ 

_______ 0(填“>”、“<”或“=”)
(3)某化学科研小组研究在其他条件不变时,改变某一条件对反应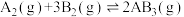 的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)
的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)

根据图像得出的结论,若正反应吸热,则
_______  (填“>”、“<”或“=”),对于a、b、c三点:
(填“>”、“<”或“=”),对于a、b、c三点: 的平衡体积分数由大到小为
的平衡体积分数由大到小为_______ , 的平衡转化率由大到小为
的平衡转化率由大到小为_______ , 的平衡转化率由大到小为
的平衡转化率由大到小为_______ 。
(4)对于化学反应 ,L线上所有的点都是平衡点。
,L线上所有的点都是平衡点。

则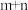
_______ 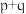 ,E点
,E点
_______  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
(1)对于反应

 ,
,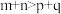

上图中各时间点改变的条件是



(2)可逆反应
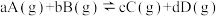
 ,同时符合下列两图中各曲线,
,同时符合下列两图中各曲线,
则

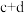



(3)某化学科研小组研究在其他条件不变时,改变某一条件对反应
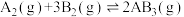 的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)
的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)
根据图像得出的结论,若正反应吸热,则

 (填“>”、“<”或“=”),对于a、b、c三点:
(填“>”、“<”或“=”),对于a、b、c三点: 的平衡体积分数由大到小为
的平衡体积分数由大到小为 的平衡转化率由大到小为
的平衡转化率由大到小为 的平衡转化率由大到小为
的平衡转化率由大到小为(4)对于化学反应
 ,L线上所有的点都是平衡点。
,L线上所有的点都是平衡点。
则
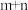
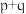 ,E点
,E点
 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
您最近一年使用:0次
2022-11-17更新
|
488次组卷
|
2卷引用:内蒙古第一机械制造(集团)有限公司第一中学2022-2023学年高二上学期11月线上期中考试化学试题
名校
解题方法
5 . 运用分类的方法研究物质及其变化的规律是化学学习的有效途径。回答下列问题:
(1)将①Fe ②CO ③硫酸铜溶液 ④液态氯化氢 ⑤熔融氯化钠 ⑥固态烧碱 ⑦ 固体 ⑧CuO固体 ⑨氨气 ⑩
固体 ⑧CuO固体 ⑨氨气 ⑩ 晶体
晶体
按不同的分类标准填空:
a.碱性氧化物:_______ (填序号,下同);
b.电解质:_______ ;
c.上述状态下能导电的是_______ 。
(2)用上述物质,按要求填空。
a.⑩在熔融状态下的电离方程式为_______ ;
b.④和⑥在溶液中反应的离子方程式为_______ ;
c.将少量⑦投入③中的现象为_______ ;
d.用②还原⑧的化学方程式为_______ 。
(1)将①Fe ②CO ③硫酸铜溶液 ④液态氯化氢 ⑤熔融氯化钠 ⑥固态烧碱 ⑦
 固体 ⑧CuO固体 ⑨氨气 ⑩
固体 ⑧CuO固体 ⑨氨气 ⑩ 晶体
晶体按不同的分类标准填空:
a.碱性氧化物:
b.电解质:
c.上述状态下能导电的是
(2)用上述物质,按要求填空。
a.⑩在熔融状态下的电离方程式为
b.④和⑥在溶液中反应的离子方程式为
c.将少量⑦投入③中的现象为
d.用②还原⑧的化学方程式为
您最近一年使用:0次
2022-11-04更新
|
180次组卷
|
2卷引用:内蒙古乌兰浩特第一中学2022-2023学年高一上学期期中考试化学试题
6 . 自然界中的水中含有多种杂质与病原微生物,在利用之前必须进行净化。
I. 自来水处理需要经过絮凝沉淀、投药消毒等步骤才能输送到住户。
(1)明矾作为一种传统的净水剂,其溶于水后形成的_______ 可以吸附水中的杂质。由于人体过量摄入 会产生健康问题,现在明矾的使用量已大幅度减少。
会产生健康问题,现在明矾的使用量已大幅度减少。
(2) 是一种新型的消毒剂,可杀灭绝大多数的微生物。已知在中性溶液中,
是一种新型的消毒剂,可杀灭绝大多数的微生物。已知在中性溶液中, 可将剧毒的
可将剧毒的 氧化为两种无毒的气体,则发生反应的离子方程式为
氧化为两种无毒的气体,则发生反应的离子方程式为_______ ;“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是“分别在氧化还原反应中得到1 mol电子时, 与该种含氯消毒剂的质量比”,则
与该种含氯消毒剂的质量比”,则 的有效氯含量为
的有效氯含量为_______ (结果保留两位小数)。
II.为配制100 mL 0.1 mol/L的 溶液,实验室中要制取少量蒸馏水,其装置如下图所示:
溶液,实验室中要制取少量蒸馏水,其装置如下图所示:

(3)仪器a的名称为_______ ,冷凝水应从_______ (选填“p”或“q”)口进入冷凝管。
(4)请指出图中装置的一处明显错误:_______ 。
(5)配制 溶液所需的玻璃仪器有100 mL容量瓶、烧杯、胶头滴管、
溶液所需的玻璃仪器有100 mL容量瓶、烧杯、胶头滴管、_______ ;在配制过程中,需要用托盘天平称取 固体的质量为
固体的质量为_______ g;若使用自来水进行溶液的配制,可能产生的后果为_______ (用离子方程式表示)。
I. 自来水处理需要经过絮凝沉淀、投药消毒等步骤才能输送到住户。
(1)明矾作为一种传统的净水剂,其溶于水后形成的
 会产生健康问题,现在明矾的使用量已大幅度减少。
会产生健康问题,现在明矾的使用量已大幅度减少。(2)
 是一种新型的消毒剂,可杀灭绝大多数的微生物。已知在中性溶液中,
是一种新型的消毒剂,可杀灭绝大多数的微生物。已知在中性溶液中, 可将剧毒的
可将剧毒的 氧化为两种无毒的气体,则发生反应的离子方程式为
氧化为两种无毒的气体,则发生反应的离子方程式为 与该种含氯消毒剂的质量比”,则
与该种含氯消毒剂的质量比”,则 的有效氯含量为
的有效氯含量为II.为配制100 mL 0.1 mol/L的
 溶液,实验室中要制取少量蒸馏水,其装置如下图所示:
溶液,实验室中要制取少量蒸馏水,其装置如下图所示:
(3)仪器a的名称为
(4)请指出图中装置的一处明显错误:
(5)配制
 溶液所需的玻璃仪器有100 mL容量瓶、烧杯、胶头滴管、
溶液所需的玻璃仪器有100 mL容量瓶、烧杯、胶头滴管、 固体的质量为
固体的质量为
您最近一年使用:0次
名校
解题方法
7 . 阅读下段语句,“我国海水制盐具有悠久的历史。从海水中制得的氯化钠除食用外,还用作工业原料,如生产①烧碱、②纯碱、③金属钠、④氯气、⑤漂白液(主要成分:NaCl和NaClO)、⑥次氯酸(化学式:HClO)等含氯化工产品”。
(1)语句中的化学物质中,属于电解质的是_______ (填序号),可以导电的是_______ (填序号)。
(2)语句中漂白液在酸性条件下发生归中反应生成氯气,反应的离子方程式为_______ 。
(3)从海水获得较纯净的氯化钠的简要流程如下:

①流程图中试剂1、试剂2和试剂3,可行的组合是_______ 。
A.NaOH溶液 溶液
溶液 溶液
溶液
B. 溶液NaOH溶液
溶液NaOH溶液 溶液
溶液
C. 溶液
溶液 溶液NaOH溶液
溶液NaOH溶液
D.NaOH溶液 溶液
溶液 溶液
溶液
②试剂4的化学式为_______ 。
③操作的名称:_______ 。
(4)若纯碱溶液中 与盐酸溶液中的HCl按4∶7反应的离子方程式为
与盐酸溶液中的HCl按4∶7反应的离子方程式为_______ 。
(1)语句中的化学物质中,属于电解质的是
(2)语句中漂白液在酸性条件下发生归中反应生成氯气,反应的离子方程式为
(3)从海水获得较纯净的氯化钠的简要流程如下:

①流程图中试剂1、试剂2和试剂3,可行的组合是
A.NaOH溶液
 溶液
溶液 溶液
溶液B.
 溶液NaOH溶液
溶液NaOH溶液 溶液
溶液C.
 溶液
溶液 溶液NaOH溶液
溶液NaOH溶液D.NaOH溶液
 溶液
溶液 溶液
溶液②试剂4的化学式为
③操作的名称:
(4)若纯碱溶液中
 与盐酸溶液中的HCl按4∶7反应的离子方程式为
与盐酸溶液中的HCl按4∶7反应的离子方程式为
您最近一年使用:0次
2022-10-09更新
|
178次组卷
|
3卷引用:内蒙古赤峰红旗中学2022-2023学年高一上学期11月期中考试化学试题
名校
8 . 化学计量在化学中占有重要地位。请回答下列问题:
(1)2019年1月21日13时42分,我国在酒泉卫星发射中心用长征十一号运载火箭成功发射了三颗卫星。长征系列运载火箭的燃料之一是肼( )。回答下列问题:
)。回答下列问题:
①肼的摩尔质量是_______ 。
②16g肼中含有氮原子的数目为_______ 。
③肼在氧气中燃烧生成 和
和 ,一定质量的肼燃烧后生成
,一定质量的肼燃烧后生成 和
和 的物质的量之比是
的物质的量之比是_______ 。每生成标准状况下44.8L的氮气,需要消耗肼的质量为_______ 。
(2)22.2g某二价金属氯化物(ACl2)中含有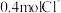 ,则A的相对原子质量是
,则A的相对原子质量是_______ ;ACl2的化学式是_______ 。
(3)在0.2L由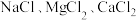 组成的混合液中,部分离子浓度大小如图所示。
组成的混合液中,部分离子浓度大小如图所示。
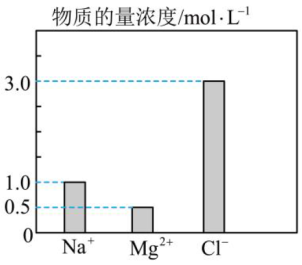
①该混合液中 的物质的量为
的物质的量为_______ mol,将该混合液加水稀释至体积为1L,稀释后溶液中 的物质的量浓度为
的物质的量浓度为_______ mol/L。
②向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀_______ mol。
(4)如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。0℃时向Ⅰ中充入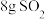 ,Ⅱ中充入
,Ⅱ中充入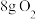 ,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为
,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为_______ 。

(1)2019年1月21日13时42分,我国在酒泉卫星发射中心用长征十一号运载火箭成功发射了三颗卫星。长征系列运载火箭的燃料之一是肼(
 )。回答下列问题:
)。回答下列问题:①肼的摩尔质量是
②16g肼中含有氮原子的数目为
③肼在氧气中燃烧生成
 和
和 ,一定质量的肼燃烧后生成
,一定质量的肼燃烧后生成 和
和 的物质的量之比是
的物质的量之比是(2)22.2g某二价金属氯化物(ACl2)中含有
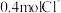 ,则A的相对原子质量是
,则A的相对原子质量是(3)在0.2L由
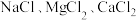 组成的混合液中,部分离子浓度大小如图所示。
组成的混合液中,部分离子浓度大小如图所示。
①该混合液中
 的物质的量为
的物质的量为 的物质的量浓度为
的物质的量浓度为②向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀
(4)如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。0℃时向Ⅰ中充入
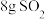 ,Ⅱ中充入
,Ⅱ中充入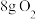 ,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为
,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为
您最近一年使用:0次
2022-10-08更新
|
306次组卷
|
2卷引用:内蒙古赤峰红旗中学2022-2023学年高一上学期11月期中考试化学试题
名校
9 . 低浓度SO2废气的处理是工业难题,目前常用的方法如下:
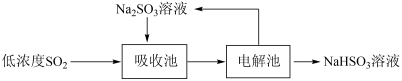
(1) 溶液吸收SO2的化学方程式是
溶液吸收SO2的化学方程式是_______ 。
(2)如果用含等物质的量溶质的下列各溶液分别吸收SO2,则理论吸收量最多的是_______ 。
a. b.
b. c.溴水 d.酸性
c.溴水 d.酸性
氧化剂与还原剂的物质的量之比为_______ 。
(3)研究大气中含硫化合物(主要是 和
和 )的转化具有重要意义。
)的转化具有重要意义。 资源化利用途径之一是回收能量并得到单质硫,如图为质子膜(该膜的作用就是只容许固体电解质中的H+自由通过)H2S燃料电池的示意图。
资源化利用途径之一是回收能量并得到单质硫,如图为质子膜(该膜的作用就是只容许固体电解质中的H+自由通过)H2S燃料电池的示意图。
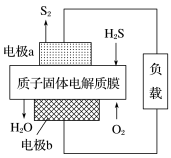
①电极b为电池的_______ 极,电极a上发生的电极反应为:_______ 。
②硫元素在元素周期表中的位置_______ ,其气态氢化物的电子式_______ 。
③每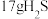 参与反应,正极消耗的
参与反应,正极消耗的 为
为_______ mol。
(4)汽车的启动电源常用铅蓄电池。放电时其电池反应为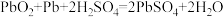 。当外电路转移1mol电子时,会消耗
。当外电路转移1mol电子时,会消耗_______ mol ,此时正极质量增加
,此时正极质量增加_______ g。

(1)
 溶液吸收SO2的化学方程式是
溶液吸收SO2的化学方程式是(2)如果用含等物质的量溶质的下列各溶液分别吸收SO2,则理论吸收量最多的是
a.
 b.
b. c.溴水 d.酸性
c.溴水 d.酸性
氧化剂与还原剂的物质的量之比为
(3)研究大气中含硫化合物(主要是
 和
和 )的转化具有重要意义。
)的转化具有重要意义。 资源化利用途径之一是回收能量并得到单质硫,如图为质子膜(该膜的作用就是只容许固体电解质中的H+自由通过)H2S燃料电池的示意图。
资源化利用途径之一是回收能量并得到单质硫,如图为质子膜(该膜的作用就是只容许固体电解质中的H+自由通过)H2S燃料电池的示意图。
①电极b为电池的
②硫元素在元素周期表中的位置
③每
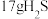 参与反应,正极消耗的
参与反应,正极消耗的 为
为(4)汽车的启动电源常用铅蓄电池。放电时其电池反应为
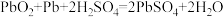 。当外电路转移1mol电子时,会消耗
。当外电路转移1mol电子时,会消耗 ,此时正极质量增加
,此时正极质量增加
您最近一年使用:0次
名校
10 . Ⅰ.黑火药爆炸的化学方程式为: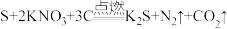 。回答下列问题:
。回答下列问题:
(1)硫元素在周期表的位置是_______ 。氨气的电子式_______ 。
(2)用电子式表示化合物 的形成过程为
的形成过程为_______ 。
(3)上述氧化产物结构式为_______ 。
(4)硫、氮及其化合物中,下列比较正确的是_______(选填编号)。
Ⅱ.如图列出了①~⑩十种元素在周期表中的位置:
请回答下列问题:
(5)上述元素中,M层电子数最多的是_______ (填元素名称)。
(6)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是_______ (用离子符号表示)。
(7)下列可以比较⑤、⑥两元素金属性强弱的实验是_______(填字母)。
(8)元素⑦的最高价氧化物对应的水化物与元素⑨的最简单氢化物的水溶液反应的离子方程式_______ 。
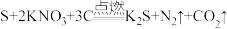 。回答下列问题:
。回答下列问题:(1)硫元素在周期表的位置是
(2)用电子式表示化合物
 的形成过程为
的形成过程为(3)上述氧化产物结构式为
(4)硫、氮及其化合物中,下列比较正确的是_______(选填编号)。
A.原子半径: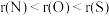 | B.热稳定性: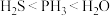 |
C.溶解度: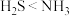 | D.微粒种类:氢硫酸<氨水 |
Ⅱ.如图列出了①~⑩十种元素在周期表中的位置:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ |
请回答下列问题:
(5)上述元素中,M层电子数最多的是
(6)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是
(7)下列可以比较⑤、⑥两元素金属性强弱的实验是_______(填字母)。
| A.比较这两种元素最高价氧化物对应的水化物的碱性 |
| B.将⑤的单质投入到⑥的盐溶液中 |
| C.将形状、大小相同的这两种元素的单质分别与等体积20℃的水反应 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
您最近一年使用:0次



