名校
1 . 回答下列问题:
(1)0.5 molNH3的质量是___________ ,在标准状况下的体积为___________ ,将此气体溶于100 mL水中得到溶液,且溶液密度为a g/mL,则该溶液的物质的量浓度为___________ ;(已知水的密度为1 g/mL)
(2)7.8g Na2X中含有Na+ 0.2 mol,则Na2X的摩尔质量为___________ ;
(3)实验室需要1.0 mol/L NaOH溶液240 mL,根据配制溶液的过程,回答下列问题:
①为完成此溶液配制实验需要的仪器除托盘天平(带砝码)、药匙、烧杯、玻璃棒、量筒、胶头滴管这六种仪器外,还缺少的必要玻璃仪器为___________ (填名称)。
②根据计算用托盘天平称取NaOH的质量为___________ g。
③若取5 mL该溶液用水稀释到100 mL,所得溶液中Na+的物质的量浓度为___________ mol/L。
(1)0.5 molNH3的质量是
(2)7.8g Na2X中含有Na+ 0.2 mol,则Na2X的摩尔质量为
(3)实验室需要1.0 mol/L NaOH溶液240 mL,根据配制溶液的过程,回答下列问题:
①为完成此溶液配制实验需要的仪器除托盘天平(带砝码)、药匙、烧杯、玻璃棒、量筒、胶头滴管这六种仪器外,还缺少的必要玻璃仪器为
②根据计算用托盘天平称取NaOH的质量为
③若取5 mL该溶液用水稀释到100 mL,所得溶液中Na+的物质的量浓度为
您最近一年使用:0次
解题方法
2 . 下列关于钠和钠的化合物的说法中错误的是
| A.金属钠着火时,用干沙子灭火 |
| B.从生活常识考虑,钠元素在自然界的主要存在形式NaCl |
| C.银白色的金属钠暴露在空气中,最终变成碳酸钠粉末 |
| D.纯碱、烧碱和小苏打都是碱类物质 |
您最近一年使用:0次
解题方法
3 . 镁在空气里点燃可以燃烧,放出大量的热并发出耀眼的白光,生成白色的氧化镁,同时,镁在这样的高温条件下,还可与空气中的另一种主要成分反应,生成少量的物质A,已知A可发生如图的一系列变化:
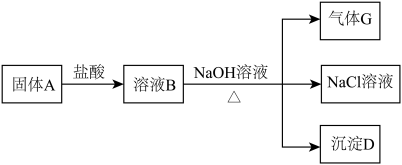
(1)写出A、C、D的化学式:A_____ 、C_____ 、D______ 。
(2)写出下列变化的化学方程式:
①固体A+盐酸:______ 。
②溶液B+NaOH溶液:______ 。

(1)写出A、C、D的化学式:A
(2)写出下列变化的化学方程式:
①固体A+盐酸:
②溶液B+NaOH溶液:
您最近一年使用:0次
解题方法
4 . 铁、铝、铜是制造潜艇必不可少的重要金属材料。下列说法正确的是
| A.三种金属形成的氧化物均为碱性氧化物 |
| B.Cu不能与AlCl3溶液、FeCl3溶液发生反应 |
| C.任何情况下,三种金属都不能与水反应 |
| D.用惰性电极电解含有Fe3+、Al3+、Cu2+的混合溶液时Fe3+优先放电 |
您最近一年使用:0次
5 . 已知R﹣CH2OH R﹣COOH(R为H原子或烃基),A(C6H14O)、B、C三种有机物之间具有如图所示的转化关系,若A、B的碳骨架相同,则C的结构最多有
R﹣COOH(R为H原子或烃基),A(C6H14O)、B、C三种有机物之间具有如图所示的转化关系,若A、B的碳骨架相同,则C的结构最多有

 R﹣COOH(R为H原子或烃基),A(C6H14O)、B、C三种有机物之间具有如图所示的转化关系,若A、B的碳骨架相同,则C的结构最多有
R﹣COOH(R为H原子或烃基),A(C6H14O)、B、C三种有机物之间具有如图所示的转化关系,若A、B的碳骨架相同,则C的结构最多有
| A.4种 | B.5种 | C.6种 | D.8种 |
您最近一年使用:0次
6 . 酸、碱、盐都是电解质,常温下,有以下电解质溶液:
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
已知: 的电离常数
的电离常数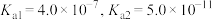
(1)用化学用语解释④呈酸性的原因:_______
(2) 的溶液①中由水电离出的
的溶液①中由水电离出的 为
为_______
(3)浓度均为 的上述7种溶液,
的上述7种溶液,  由大到小为
由大到小为_______
(4)在⑥溶液中下列关系成立的是_______
(5)若某浓度的⑥和⑦的混合溶液中 ,该溶液的
,该溶液的
_______
(6)将 的①溶液与
的①溶液与 的③溶液混合,若所得混合溶液的
的③溶液混合,若所得混合溶液的 ,则①和②溶液的体积比为
,则①和②溶液的体积比为_______
①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
已知:
 的电离常数
的电离常数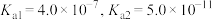
(1)用化学用语解释④呈酸性的原因:
(2)
 的溶液①中由水电离出的
的溶液①中由水电离出的 为
为(3)浓度均为
 的上述7种溶液,
的上述7种溶液,  由大到小为
由大到小为(4)在⑥溶液中下列关系成立的是
A.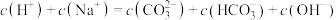 |
B.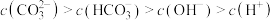 |
C. |
D.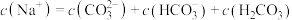 |
 ,该溶液的
,该溶液的
(6)将
 的①溶液与
的①溶液与 的③溶液混合,若所得混合溶液的
的③溶液混合,若所得混合溶液的 ,则①和②溶液的体积比为
,则①和②溶液的体积比为
您最近一年使用:0次
7 . 化学与社会生活密切相关。下列叙述中,不能用勒夏特列原理解释的是
| A.食品包装中加抗氧化剂利于延长保质期 | B.用排饱和食盐水法收集氯气 |
| C.用浓氨水和氧化钙固体快速制取氨气 | D.用热的纯碱溶液洗去油污效果更好 |
您最近一年使用:0次
名校
8 . Haber-Bosch法合成氨存在能耗高、污染严重等缺点。实现常温、常压下固氮是近年来研究的热点。回答下列问题:
(1)合成氨反应速率较慢,与反应的活化能高有很大关系,降低反应的活化能最有效的措施是_______ 。
(2)Haber-Bosch法合成氨发生的反应为 ,一定温度下,在恒压密闭容器中加入
,一定温度下,在恒压密闭容器中加入 和
和 ,达到平衡时,
,达到平衡时, 的转化率为50%,且容器体积变为
的转化率为50%,且容器体积变为 。
。
①初始时 和
和 的体积之和为
的体积之和为_______ 。
②该条件下的平衡常数为_______ 。
(3)在催化剂表面,反应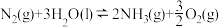 在常温、常压、光照条件下即可顺利进行,反应过程与能量关系如图所示:
在常温、常压、光照条件下即可顺利进行,反应过程与能量关系如图所示:
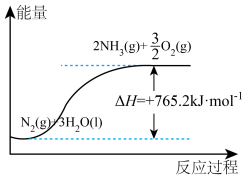
①该反应每生成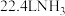 (已折算为标准状况下的体积),反应体系的能量变化为
(已折算为标准状况下的体积),反应体系的能量变化为_______  。
。
② 平衡量与温度的关系如下表所示:
平衡量与温度的关系如下表所示:
表中所涉及温度从高到低的顺序为_______ , 温度下反应
温度下反应 达到平衡,以
达到平衡,以 物质的量变化表示的平均反应速率为
物质的量变化表示的平均反应速率为_______ 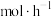 。
。
(1)合成氨反应速率较慢,与反应的活化能高有很大关系,降低反应的活化能最有效的措施是
(2)Haber-Bosch法合成氨发生的反应为
 ,一定温度下,在恒压密闭容器中加入
,一定温度下,在恒压密闭容器中加入 和
和 ,达到平衡时,
,达到平衡时, 的转化率为50%,且容器体积变为
的转化率为50%,且容器体积变为 。
。①初始时
 和
和 的体积之和为
的体积之和为②该条件下的平衡常数为
(3)在催化剂表面,反应
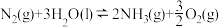 在常温、常压、光照条件下即可顺利进行,反应过程与能量关系如图所示:
在常温、常压、光照条件下即可顺利进行,反应过程与能量关系如图所示:
①该反应每生成
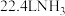 (已折算为标准状况下的体积),反应体系的能量变化为
(已折算为标准状况下的体积),反应体系的能量变化为 。
。②
 平衡量与温度的关系如下表所示:
平衡量与温度的关系如下表所示: |  |  |  |
 平衡量/( 平衡量/(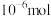 ) ) | 6.0 | 5.9 | 4.8 |
 温度下反应
温度下反应 达到平衡,以
达到平衡,以 物质的量变化表示的平均反应速率为
物质的量变化表示的平均反应速率为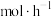 。
。
您最近一年使用:0次
2023-02-14更新
|
46次组卷
|
2卷引用:内蒙古乌兰浩特市第四中学2022-2023学年高二上学期期中考试化学试题
名校
9 . 弱酸型指示剂( )在溶液中存在如下平衡:
)在溶液中存在如下平衡: ,下列有关
,下列有关 溶液说法中正确的是[已知:
溶液说法中正确的是[已知: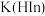 为
为 的电离平衡常数,
的电离平衡常数,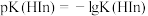 ]
]
 )在溶液中存在如下平衡:
)在溶液中存在如下平衡: ,下列有关
,下列有关 溶液说法中正确的是[已知:
溶液说法中正确的是[已知: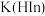 为
为 的电离平衡常数,
的电离平衡常数,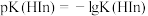 ]
]A.常温下,向 溶液中滴加 溶液中滴加 ,溶液变红 ,溶液变红 |
B.常温下,溶液 减小过程中,上述平衡向右移动 减小过程中,上述平衡向右移动 |
C. 可能是甲基橙指示剂 可能是甲基橙指示剂 |
D.当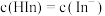 时, 时, 溶液中 溶液中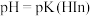 |
您最近一年使用:0次
名校
解题方法
10 . 一氯化碘(ICl)是一种卤素互化物。卤素互化物具有强氧化性稀溶液,可与金属直接反应,也可用作有机合成中的碘化剂,一般可由卤素单质直接化合制得。有关一氯化碘制备及性质验证,请回答下列问题:
I.海藻提碘可得到I2的CCl4溶液,从其中回收I2的流程如下:
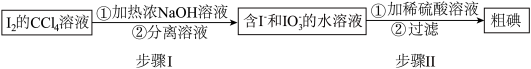
(1)步骤I的分离溶液操作中,主要用到的玻璃仪器有烧杯和_______ ,步骤Ⅱ的反应中氧化剂与还原剂的物质的量之比为_______ 。
(2)回收获得的粗碘可采用如图所示的简易装置分离提纯。将粉状物放入蒸发皿中并小火加热,碘晶体在扎有小孔的滤纸上凝结,该分离提纯方法的名称是_______ 。

Ⅱ.某学习小组在实验室中拟用下图装置制取纯净、干燥的氯气,并利用氯气与碘反应制备一氯化碘。
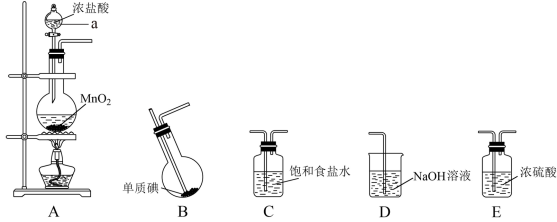
查阅资料了解到以下内容:
①碘与氯气的反应为放热反应
②ICl是一种红棕色液体,沸点97.4℃,不溶于水
③ICl能与KI反应生成I2
请回答下列问题:
(3)各装置连接顺序为A→_______→_______→_______→_______;_______
(4)B装置烧瓶需放在冷水中,其目的是:_______ ,B装置得到的液态产物进一步提纯可得到较纯净的ICl,采取的方法是_______ 。
(5)ICl与稀NaOH溶液可发生非氧化还原反应,请写出该反应的离子方程式_______ 。
(6)请设计简单的实验证明ICl的氧化性比I2强:_______ 。
I.海藻提碘可得到I2的CCl4溶液,从其中回收I2的流程如下:

(1)步骤I的分离溶液操作中,主要用到的玻璃仪器有烧杯和
(2)回收获得的粗碘可采用如图所示的简易装置分离提纯。将粉状物放入蒸发皿中并小火加热,碘晶体在扎有小孔的滤纸上凝结,该分离提纯方法的名称是

Ⅱ.某学习小组在实验室中拟用下图装置制取纯净、干燥的氯气,并利用氯气与碘反应制备一氯化碘。

查阅资料了解到以下内容:
①碘与氯气的反应为放热反应
②ICl是一种红棕色液体,沸点97.4℃,不溶于水
③ICl能与KI反应生成I2
请回答下列问题:
(3)各装置连接顺序为A→_______→_______→_______→_______;
(4)B装置烧瓶需放在冷水中,其目的是:
(5)ICl与稀NaOH溶液可发生非氧化还原反应,请写出该反应的离子方程式
(6)请设计简单的实验证明ICl的氧化性比I2强:
您最近一年使用:0次
2023-01-19更新
|
406次组卷
|
2卷引用:内蒙古自治区呼和浩特市2022-2023学年高三上学期质量普查调研考试化学试题



