1 . 酸、碱、盐都是电解质,常温下,有以下电解质溶液:
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
已知: 的电离常数
的电离常数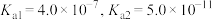
(1)用化学用语解释④呈酸性的原因:_______
(2) 的溶液①中由水电离出的
的溶液①中由水电离出的 为
为_______
(3)浓度均为 的上述7种溶液,
的上述7种溶液,  由大到小为
由大到小为_______
(4)在⑥溶液中下列关系成立的是_______
(5)若某浓度的⑥和⑦的混合溶液中 ,该溶液的
,该溶液的
_______
(6)将 的①溶液与
的①溶液与 的③溶液混合,若所得混合溶液的
的③溶液混合,若所得混合溶液的 ,则①和②溶液的体积比为
,则①和②溶液的体积比为_______
①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
已知:
 的电离常数
的电离常数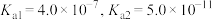
(1)用化学用语解释④呈酸性的原因:
(2)
 的溶液①中由水电离出的
的溶液①中由水电离出的 为
为(3)浓度均为
 的上述7种溶液,
的上述7种溶液,  由大到小为
由大到小为(4)在⑥溶液中下列关系成立的是
A.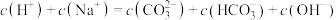 |
B.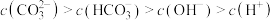 |
C. |
D.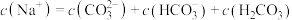 |
 ,该溶液的
,该溶液的
(6)将
 的①溶液与
的①溶液与 的③溶液混合,若所得混合溶液的
的③溶液混合,若所得混合溶液的 ,则①和②溶液的体积比为
,则①和②溶液的体积比为
您最近一年使用:0次
2 . 化学与社会生活密切相关。下列叙述中,不能用勒夏特列原理解释的是
| A.食品包装中加抗氧化剂利于延长保质期 | B.用排饱和食盐水法收集氯气 |
| C.用浓氨水和氧化钙固体快速制取氨气 | D.用热的纯碱溶液洗去油污效果更好 |
您最近一年使用:0次
解题方法
3 . 在实验室里用乙醇、冰醋酸和浓硫酸来制备一种有香味的物质,实验装置如图所示,请根据要求作答。

(1)写出该反应的化学方程式。_______ ,反应类型:_______ 。
(2)往甲试管中加入_____ 可防止暴沸。乙中所盛的试剂为_____ ,该溶液的主要作用是:_____ 、____ 。
(3)实验室怎样鉴别乙酸和乙醇?_______ 。
(4)该装置图中有一个明显的错误是_______ 。

(1)写出该反应的化学方程式。
(2)往甲试管中加入
(3)实验室怎样鉴别乙酸和乙醇?
(4)该装置图中有一个明显的错误是
您最近一年使用:0次
名校
解题方法
4 . 用如图所示的甲、乙两个装置做导电实验,下列叙述正确的是


| A.石墨、金刚石及C60都是单质 |
| B.甲装置中石墨和NaOH溶液均能导电,所以均为电解质 |
| C.甲装置中NaOH溶液能导电的原因是NaOH电离出自由移动的离子. |
| D.乙装置中纯醋酸液体不能导电,所以纯醋酸不是电解质 |
您最近一年使用:0次
2022-10-28更新
|
278次组卷
|
2卷引用:内蒙古集宁一中2022-2023学年高一上学期期末考试化学试题
解题方法
5 . 下图是实验室用乙醇、硫酸、溴化钠混合反应来制备溴乙烷的装置(省去了加热装置),回答下列问题:
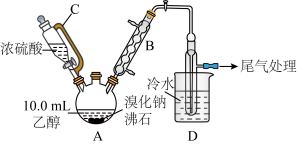
已知:浓硫酸与溴化钠共热时发生反应:
(1)仪器A、C的名称分别为_______ 、_______ ;B的作用为_______ 。
(2)装置A中生成溴乙烷的化学方程式为_______ 。
(3)若选用的硫酸浓度过大,D中得到的产品则会因混入少量溴而呈棕黄色,生成这一副产物的原因为_______ (用化学方程式表示);为纯化产物,最好选择下列的_______ 溶液来洗涤产品。
A.四氯化碳 B.硫酸钠 C.碘化钠 D.亚硫酸钠
(4)若实验中使用了10g乙醇、20.6g溴化钠,且浓硫酸足量,经过分离、提纯、干燥后,最终得到10.9g溴乙烷,则本实验中溴乙烷的产率为_______ (保留3位有效数字)。
(5)检验溴乙烷中溴元素的方法为:取样,_______ ,若产生淡黄色沉淀,则该物质中存在溴元素。

已知:浓硫酸与溴化钠共热时发生反应:

(1)仪器A、C的名称分别为
(2)装置A中生成溴乙烷的化学方程式为
(3)若选用的硫酸浓度过大,D中得到的产品则会因混入少量溴而呈棕黄色,生成这一副产物的原因为
A.四氯化碳 B.硫酸钠 C.碘化钠 D.亚硫酸钠
(4)若实验中使用了10g乙醇、20.6g溴化钠,且浓硫酸足量,经过分离、提纯、干燥后,最终得到10.9g溴乙烷,则本实验中溴乙烷的产率为
(5)检验溴乙烷中溴元素的方法为:取样,
您最近一年使用:0次
2022-10-25更新
|
333次组卷
|
2卷引用:内蒙古自治区鄂尔多斯市达拉特旗第一中学2021-2022学年高二下学期期末考试化学试题
6 . 苯是一种重要的化工原料,回答下列问题:
(1)1865年,德国化学家凯库勒提出了苯分子的单双键交替环状结构式,解释了苯的部分性质,但还有些问题尚未解决,它不能解释的事实是_______ 。
a.邻二溴苯只有一种 b.苯可发生加成反应
c.溴苯没有同分异构体 d.苯不能使溴的四氯化碳溶液褪色
(2)以苯的同系物中分子量最小的物质为原料能生产一种烈性炸药,该过程中发生的化学方程式为_______ 。
(3)苯有多种生产途径,将煤炭隔绝空气加强热使其分解的过程称为煤的_______ ,其产品煤焦油中便含有一定量的苯;另一方面,乙炔在催化剂作用下可合成苯,已知苯与乙炔在氧气中燃烧的热化学方程式如下,则3C2H2(g)=C6H6(l) △H=_______ 。C6H6(l)+7.5O2(g)=6CO2(g)+3H2O(l) △H=-3260.4kJ/mol
C2H2(g)+2.5O2(g)=2CO2(g)+H2O(l) △H=-1299.6kJ/mol
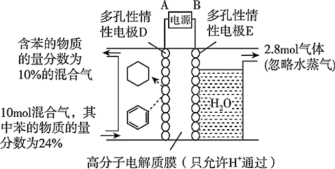
(4)一定条件下,如图所示装置可实现苯到环己烷的转化,若阴极产物只有环己烷和氢气,则阴极上苯生成环己烷的电极反应式为____ ;按图中所给数据计算可得阴极产生H2的物质的量为____ mol。
(1)1865年,德国化学家凯库勒提出了苯分子的单双键交替环状结构式,解释了苯的部分性质,但还有些问题尚未解决,它不能解释的事实是
a.邻二溴苯只有一种 b.苯可发生加成反应
c.溴苯没有同分异构体 d.苯不能使溴的四氯化碳溶液褪色
(2)以苯的同系物中分子量最小的物质为原料能生产一种烈性炸药,该过程中发生的化学方程式为
(3)苯有多种生产途径,将煤炭隔绝空气加强热使其分解的过程称为煤的
C2H2(g)+2.5O2(g)=2CO2(g)+H2O(l) △H=-1299.6kJ/mol
(4)一定条件下,如图所示装置可实现苯到环己烷的转化,若阴极产物只有环己烷和氢气,则阴极上苯生成环己烷的电极反应式为

您最近一年使用:0次
解题方法
7 . 下列每组中的物质能用所给的试剂进行鉴别的是
| A.苯、苯酚、1-戊烯、辛烷(溴水) |
| B.乙醇、乙醛、乙酸、乙酸乙酯(新制氢氧化铜悬浊液) |
| C.甲烷、乙烯、乙炔、甲醛(品红溶液) |
| D.苯、甲苯、溴苯、硝基苯(酸性高锰酸钾溶液) |
您最近一年使用:0次
解题方法
8 . 实验室对某有机物有如下实验记录:①在氧气中完全燃烧,只生成 、
、 ;②1mol该有机物完全燃烧需消耗氧气112L(标准状况下),其分子式可能为
;②1mol该有机物完全燃烧需消耗氧气112L(标准状况下),其分子式可能为
 、
、 ;②1mol该有机物完全燃烧需消耗氧气112L(标准状况下),其分子式可能为
;②1mol该有机物完全燃烧需消耗氧气112L(标准状况下),其分子式可能为A.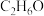 | B. | C. | D. |
您最近一年使用:0次
9 . 下列关于高聚物的说法错误的是
| A.聚乙炔可以用于制作导电部件 |
| B.网状结构的酚醛树脂可以加热重塑 |
| C.聚丙烯酸钠是一种高吸水性树脂 |
| D.顺丁橡胶弹性好,可用于轮胎制造 |
您最近一年使用:0次
10 . 取少量鸡蛋清溶液于试管中,向其中滴加少量饱和溶液X,发现蛋白质析出,再加适量水发现蛋白质溶解,则X中的溶质可能为
A. | B. | C. | D. |
您最近一年使用:0次



