名校
1 . 回答下列问题:
(1)0.5 molNH3的质量是___________ ,在标准状况下的体积为___________ ,将此气体溶于100 mL水中得到溶液,且溶液密度为a g/mL,则该溶液的物质的量浓度为___________ ;(已知水的密度为1 g/mL)
(2)7.8g Na2X中含有Na+ 0.2 mol,则Na2X的摩尔质量为___________ ;
(3)实验室需要1.0 mol/L NaOH溶液240 mL,根据配制溶液的过程,回答下列问题:
①为完成此溶液配制实验需要的仪器除托盘天平(带砝码)、药匙、烧杯、玻璃棒、量筒、胶头滴管这六种仪器外,还缺少的必要玻璃仪器为___________ (填名称)。
②根据计算用托盘天平称取NaOH的质量为___________ g。
③若取5 mL该溶液用水稀释到100 mL,所得溶液中Na+的物质的量浓度为___________ mol/L。
(1)0.5 molNH3的质量是
(2)7.8g Na2X中含有Na+ 0.2 mol,则Na2X的摩尔质量为
(3)实验室需要1.0 mol/L NaOH溶液240 mL,根据配制溶液的过程,回答下列问题:
①为完成此溶液配制实验需要的仪器除托盘天平(带砝码)、药匙、烧杯、玻璃棒、量筒、胶头滴管这六种仪器外,还缺少的必要玻璃仪器为
②根据计算用托盘天平称取NaOH的质量为
③若取5 mL该溶液用水稀释到100 mL,所得溶液中Na+的物质的量浓度为
您最近一年使用:0次
解题方法
2 . 下列关于钠和钠的化合物的说法中错误的是
| A.金属钠着火时,用干沙子灭火 |
| B.从生活常识考虑,钠元素在自然界的主要存在形式NaCl |
| C.银白色的金属钠暴露在空气中,最终变成碳酸钠粉末 |
| D.纯碱、烧碱和小苏打都是碱类物质 |
您最近一年使用:0次
解题方法
3 . 镁在空气里点燃可以燃烧,放出大量的热并发出耀眼的白光,生成白色的氧化镁,同时,镁在这样的高温条件下,还可与空气中的另一种主要成分反应,生成少量的物质A,已知A可发生如图的一系列变化:
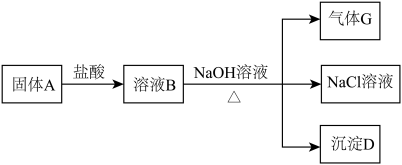
(1)写出A、C、D的化学式:A_____ 、C_____ 、D______ 。
(2)写出下列变化的化学方程式:
①固体A+盐酸:______ 。
②溶液B+NaOH溶液:______ 。

(1)写出A、C、D的化学式:A
(2)写出下列变化的化学方程式:
①固体A+盐酸:
②溶液B+NaOH溶液:
您最近一年使用:0次
解题方法
4 . 铁、铝、铜是制造潜艇必不可少的重要金属材料。下列说法正确的是
| A.三种金属形成的氧化物均为碱性氧化物 |
| B.Cu不能与AlCl3溶液、FeCl3溶液发生反应 |
| C.任何情况下,三种金属都不能与水反应 |
| D.用惰性电极电解含有Fe3+、Al3+、Cu2+的混合溶液时Fe3+优先放电 |
您最近一年使用:0次
名校
解题方法
5 . 某绿色溶液A含有H+、Na+、Mg2+、Fe2+、Cu2+、 、Cl-、
、Cl-、 、
、 离子中的种若干种。取该溶液进行如下实验:
离子中的种若干种。取该溶液进行如下实验:
①向溶液中滴加Ba(OH)2溶液,过滤,得到不溶于酸的白色沉淀和绿色滤液B;
②取滤液B,先用硝酸酸化,再滴加AgNO3溶液,有白色沉淀生成。
已知:①CuCl2·2H2O是绿色固体,溶于水浓溶液呈绿色,稀溶液呈蓝色;
②Ag2SO4微溶于水,可溶于硝酸;
③Fe2+(aq)呈浅绿色;Fe(OH)2是白色沉淀,在空气中与氧气和水反应迅速变成灰绿色,最终变成红褐色的Fe(OH)3沉淀。
根据上述信息,回答下列问题:
(1)导致溶液A呈现绿色的原因是_______ ;
(2)通过实验①可以得出_______ 离子存在、_______ 离子不存在的结论;
(3)通过实验②可以得出的结论是_______ ;
(4)结合实验①和②和题干信息,仍不能判断A溶液中是否存在的离子是_______ ;
(5)在绿色滤液B中加入_______ 溶液,依据不同的现象,可以推断出导致溶液呈现绿色的离子的具体存在情况。写出Fe(OH)2在空气中与氧气和水反应生成红褐色的Fe(OH)3的化学方程式_______ 。
 、Cl-、
、Cl-、 、
、 离子中的种若干种。取该溶液进行如下实验:
离子中的种若干种。取该溶液进行如下实验:①向溶液中滴加Ba(OH)2溶液,过滤,得到不溶于酸的白色沉淀和绿色滤液B;
②取滤液B,先用硝酸酸化,再滴加AgNO3溶液,有白色沉淀生成。
已知:①CuCl2·2H2O是绿色固体,溶于水浓溶液呈绿色,稀溶液呈蓝色;
②Ag2SO4微溶于水,可溶于硝酸;
③Fe2+(aq)呈浅绿色;Fe(OH)2是白色沉淀,在空气中与氧气和水反应迅速变成灰绿色,最终变成红褐色的Fe(OH)3沉淀。
根据上述信息,回答下列问题:
(1)导致溶液A呈现绿色的原因是
(2)通过实验①可以得出
(3)通过实验②可以得出的结论是
(4)结合实验①和②和题干信息,仍不能判断A溶液中是否存在的离子是
(5)在绿色滤液B中加入
您最近一年使用:0次
2022-12-07更新
|
187次组卷
|
2卷引用:内蒙古包头市第九中学2022-2023学年高一上学期10月月考化学试题
23-24高一上·全国·假期作业
名校
解题方法
6 . 某小组同学在加热NH4HCO3固体时,闻到了刺激性气味,决定对其进一步探究:
(1)如图所示,
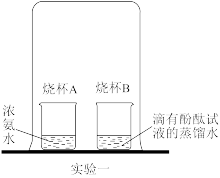
实验一中观察到的现象是_______ ,宏观上说明浓氨水有_______ ,微观上说明_______ 。写出NH4HCO3受热分解的化学方程式_______ 。
(2)实验二装置连接好之后首先要做的是_______ ,然后再通入氨气排尽装置A中的空气,最后点燃酒精灯,持续加热,发现氧化铜逐渐由黑变红,依据题中信息,写出装置A中发生反应的化学方程式_______ ,该反应中氨气是_______ 剂,实验证明了氨气具有_______ 性。
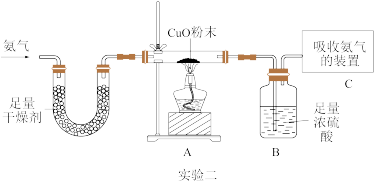
(3)实验二加热一段时间后,A、B、C三个装置的质量变化是:
该实验小组的同学按照实验数据计算出氮、氢元素的质量之比明显与理论上氨气中氮、氢的质量比不符,分析产生该误差的原因是_______ ,写出装置B中发生反应的化学方程式_______ 。
(1)如图所示,

实验一中观察到的现象是
(2)实验二装置连接好之后首先要做的是

(3)实验二加热一段时间后,A、B、C三个装置的质量变化是:
| 装置 | A | B | C |
| 数据 | 减少了4.8g | 增加了7.2g | 增加了2.8g |
您最近一年使用:0次
名校
解题方法
7 . 海水通过蒸发结晶得到的粗盐经溶解过滤,除去少量泥沙及悬浮物后,溶液中主要含有Na+、Cl-,还有杂质离子Ca2+、Mg2+、SO ,现要对其进一步提纯,得到较纯净的NaCl溶液,可用试剂和操作步骤如下:试剂:①盐酸、②Na2CO3(aq)、③NaOH(aq)、④BaCl2(aq)
,现要对其进一步提纯,得到较纯净的NaCl溶液,可用试剂和操作步骤如下:试剂:①盐酸、②Na2CO3(aq)、③NaOH(aq)、④BaCl2(aq)
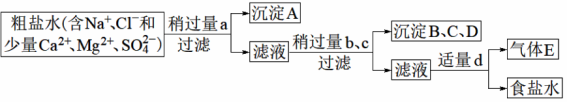
图中a、b、c、d分别表示上述试剂中的一种,回答下列问题:
(1)沉淀A可能是_______ 或_______ (填化学式)
(2)判断试剂a稍过量的实验操作是_______
(3)Na2CO3(aq)的作用是_______
(4)第一次过滤是否可以省略_______ (填“是”或“否”)
(5)写出加入适量d所发生反应的离子方程式_______ ;写出少量气体E通入澄清石灰水反应的离子方程式_______ 。
 ,现要对其进一步提纯,得到较纯净的NaCl溶液,可用试剂和操作步骤如下:试剂:①盐酸、②Na2CO3(aq)、③NaOH(aq)、④BaCl2(aq)
,现要对其进一步提纯,得到较纯净的NaCl溶液,可用试剂和操作步骤如下:试剂:①盐酸、②Na2CO3(aq)、③NaOH(aq)、④BaCl2(aq)
图中a、b、c、d分别表示上述试剂中的一种,回答下列问题:
(1)沉淀A可能是
(2)判断试剂a稍过量的实验操作是
(3)Na2CO3(aq)的作用是
(4)第一次过滤是否可以省略
(5)写出加入适量d所发生反应的离子方程式
您最近一年使用:0次
8 . 下列物质的应用不是利用了氧化还原反应的是
| A.用生石灰脱去燃煤产生的SO2并且最终转化为稳定的CaSO4 |
| B.火箭发射时火箭燃料剧烈的反应 |
| C.用煮沸的豆浆和石膏稀溶液可制作豆腐脑或豆腐 |
| D.绿色植物进行光合作用将CO2和H2O转化成葡萄糖和氧气 |
您最近一年使用:0次
名校
解题方法
9 . 在制备Fe(OH)3胶体的实验中,下列操作正确的是
| A.使用自来水 | B.使用饱和FeCl3溶液 | C.长时间煮沸 | D.用玻璃棒搅拌 |
您最近一年使用:0次
名校
解题方法
10 . 关于胶体和溶液的区别,下列叙述中正确的是
| A.溶液中溶质粒子有规律的运动,而胶体粒子无规律的运动 |
| B.溶液和胶体粒子均能透过滤纸,胶体粒子还可以透过半透膜 |
| C.溶液中溶质粒子一定带电,且通电后溶质粒子向两极移动 |
| D.一束光通过胶体时有光亮的“通路”,通过溶液时无此现象 |
您最近一年使用:0次



