解题方法
1 . 化学与人体健康及生产、生活息息相关。下列叙述正确的是
| A.常用的食品添加剂有蔗糖、醋、二氧化硫、苯甲酸等 |
| B.直馏汽油、裂化汽油、植物油均能使溴的四氯化碳溶液褪色 |
| C.“井水不犯河水”说明井水与河水中含有两种完全不同的水 |
| D.古代造纸工艺中使用草木灰会导致纸张发生酸性腐蚀 |
您最近半年使用:0次
名校
2 . 下列说法正确的是
| A.烷基是推电子基团,故甲酸的酸性强于乙酸 |
| B.水分子在较高温度下也很稳定与氢键有关 |
C.白磷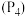 空间结构呈正四面体形,1mol白磷含 空间结构呈正四面体形,1mol白磷含 个P-P 个P-P |
D.邻羟基苯甲醛分子内氢键示意图: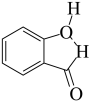 |
您最近半年使用:0次
名校
3 . 下列说法正确的是
A.电子排布不同的两种氮原子:①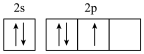 ② ②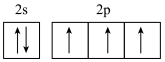 ,能量 ,能量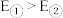 |
| B.焰火、霓虹灯光、激光、苂光、LED灯光等,都与原子核外电子跃迁吸收能量有关 |
C.若以 表示某能级的能量,则 表示某能级的能量,则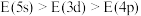 |
| D.三氯乙酸的酸性强于三氟乙酸 |
您最近半年使用:0次
4 . 回答下列问题。
(1)双氧水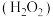 和水都是极弱电解质,若把
和水都是极弱电解质,若把 看成是二元弱酸,请写出在水中的电离方程式:
看成是二元弱酸,请写出在水中的电离方程式:___________ 。鉴于 显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出
显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出 与
与 作用形成盐的两个化学方程式:
作用形成盐的两个化学方程式:___________ 。
(2)如图是向 的盐酸中逐渐加入
的盐酸中逐渐加入 溶液时,溶液的
溶液时,溶液的 变化图像。
变化图像。___________  。
。
②X的值为___________ 。
(3)已知 的高碘酸
的高碘酸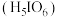 溶液与
溶液与 的
的 溶液等体积混合,所得混合溶液呈酸性,
溶液等体积混合,所得混合溶液呈酸性, 的碘酸
的碘酸 或高锰酸
或高锰酸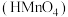 溶液与
溶液与 的
的 溶液等体积混合,所得溶液呈中性,高碘酸是
溶液等体积混合,所得溶液呈中性,高碘酸是___________ (填“强酸”或“弱酸”),理由是___________ 。
(4) 时,在一定体积
时,在一定体积 的
的 溶液中,逐滴加入一定物质的量浓度的
溶液中,逐滴加入一定物质的量浓度的 溶液,当溶液中的
溶液,当溶液中的 恰好完全沉淀时,溶液
恰好完全沉淀时,溶液 ,忽略溶液体积变化,则
,忽略溶液体积变化,则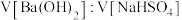 为
为___________ 。
(1)双氧水
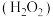 和水都是极弱电解质,若把
和水都是极弱电解质,若把 看成是二元弱酸,请写出在水中的电离方程式:
看成是二元弱酸,请写出在水中的电离方程式: 显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出
显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出 与
与 作用形成盐的两个化学方程式:
作用形成盐的两个化学方程式:(2)如图是向
 的盐酸中逐渐加入
的盐酸中逐渐加入 溶液时,溶液的
溶液时,溶液的 变化图像。
变化图像。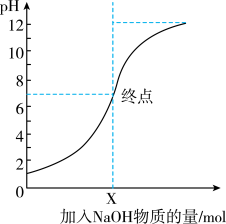
 。
。②X的值为
(3)已知
 的高碘酸
的高碘酸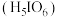 溶液与
溶液与 的
的 溶液等体积混合,所得混合溶液呈酸性,
溶液等体积混合,所得混合溶液呈酸性, 的碘酸
的碘酸 或高锰酸
或高锰酸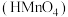 溶液与
溶液与 的
的 溶液等体积混合,所得溶液呈中性,高碘酸是
溶液等体积混合,所得溶液呈中性,高碘酸是(4)
 时,在一定体积
时,在一定体积 的
的 溶液中,逐滴加入一定物质的量浓度的
溶液中,逐滴加入一定物质的量浓度的 溶液,当溶液中的
溶液,当溶液中的 恰好完全沉淀时,溶液
恰好完全沉淀时,溶液 ,忽略溶液体积变化,则
,忽略溶液体积变化,则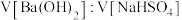 为
为
您最近半年使用:0次
5 . 试回答下列有关热化学问题。
(1)根据键能数据计算 的反应热
的反应热
___________ 。
(2) 催化重整反应为
催化重整反应为 。
。
已知:
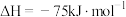

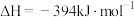

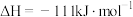
该催化重整反应的
___________  。
。
(3)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如图: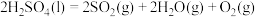

反应Ⅲ:
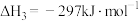
反应Ⅱ的热化学方程式:___________ 。
(4)工业上常用磷精矿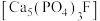 和硫酸反应制备磷酸。已知
和硫酸反应制备磷酸。已知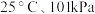 时:
时:

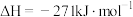
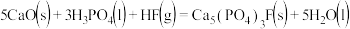
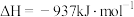
则 和硫酸反应生成磷酸的热化学方程式是
和硫酸反应生成磷酸的热化学方程式是___________ 。
(5)已知: 钒催化剂参与反应的能量变化如图所示,
钒催化剂参与反应的能量变化如图所示,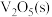 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。
(1)根据键能数据计算
 的反应热
的反应热
| 化学键 |  |  |  |  |
键能 | 414 | 489 | 565 | 155 |
(2)
 催化重整反应为
催化重整反应为 。
。已知:

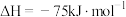

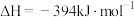

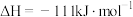
该催化重整反应的

 。
。(3)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如图:
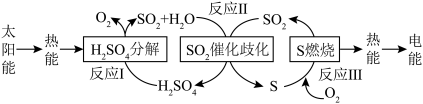
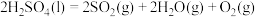

反应Ⅲ:

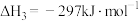
反应Ⅱ的热化学方程式:
(4)工业上常用磷精矿
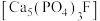 和硫酸反应制备磷酸。已知
和硫酸反应制备磷酸。已知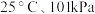 时:
时:
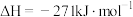
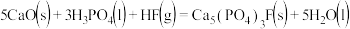
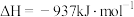
则
 和硫酸反应生成磷酸的热化学方程式是
和硫酸反应生成磷酸的热化学方程式是(5)已知:
 钒催化剂参与反应的能量变化如图所示,
钒催化剂参与反应的能量变化如图所示,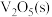 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为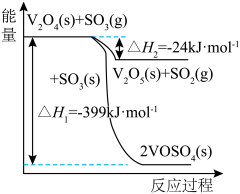
您最近半年使用:0次
名校
解题方法
6 . 五水硫酸铜在化工、农业、医药、食品等方面均有广泛的用途,实验室制备方法如下:
(1)制备硫酸铜溶液
称取3.0g铜粉放入双颈烧瓶中,加入11.0mL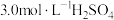 ,再分批缓慢加入5.0mL
,再分批缓慢加入5.0mL 浓
浓 ,待反应缓和后水浴加热。在加热过程中补加6.0mL
,待反应缓和后水浴加热。在加热过程中补加6.0mL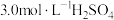 和1.0mL浓硝酸。
和1.0mL浓硝酸。
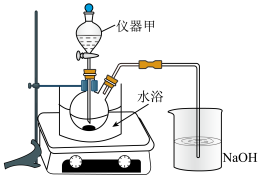
①仪器甲的名称是______ ,硝酸的主要作用是______ 。
②分批加入硝酸的主要原因是______ 。
③实验过程中,观察到有气体生成,NaOH溶液的作用是吸收______ 和______ 。
(2)制得五水硫酸铜粗品
待Cu接近于全部溶解后,趁热用倾析法将溶液转至小烧杯中,然后通过“相关操作”得到粗五水硫酸铜晶体。
①趁热用倾析法转液的目的是______ 、______ 。
②通过“相关操作”得到粗五水硫酸铜晶体,其“相关操作”是指将溶液转至蒸发皿中,水浴加热,______ 。
③如果蒸发水时温度过高,得到的晶体会偏白色,则原因是______ 。(用化学反应方程式表示)
(1)制备硫酸铜溶液
称取3.0g铜粉放入双颈烧瓶中,加入11.0mL
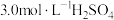 ,再分批缓慢加入5.0mL
,再分批缓慢加入5.0mL 浓
浓 ,待反应缓和后水浴加热。在加热过程中补加6.0mL
,待反应缓和后水浴加热。在加热过程中补加6.0mL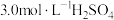 和1.0mL浓硝酸。
和1.0mL浓硝酸。
①仪器甲的名称是
②分批加入硝酸的主要原因是
③实验过程中,观察到有气体生成,NaOH溶液的作用是吸收
(2)制得五水硫酸铜粗品
待Cu接近于全部溶解后,趁热用倾析法将溶液转至小烧杯中,然后通过“相关操作”得到粗五水硫酸铜晶体。
①趁热用倾析法转液的目的是
②通过“相关操作”得到粗五水硫酸铜晶体,其“相关操作”是指将溶液转至蒸发皿中,水浴加热,
③如果蒸发水时温度过高,得到的晶体会偏白色,则原因是
您最近半年使用:0次
2024-04-04更新
|
200次组卷
|
3卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期末测试化学试题
名校
解题方法
7 . 某化学小组利用装置A制取 并探究
并探究 的相关性质(部分仪器已略去)。
的相关性质(部分仪器已略去)。
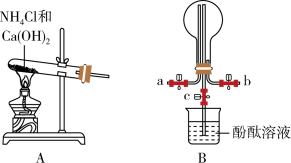
(1)B中圆底烧瓶收集氨气时,氨气的进气口________ (填“a”或“b”)。
(2)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是________ ;引发喷泉的操作应是________ 。
(3)查阅资料:氮的氧化物( )是大气污染物之一,工业上在一定温度和催化剂条件下用
)是大气污染物之一,工业上在一定温度和催化剂条件下用 将
将 还原生成无污染的物质。该小组将收集到的
还原生成无污染的物质。该小组将收集到的 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入
充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入 (两端用夹子
(两端用夹子 、
、 夹好)。
夹好)。
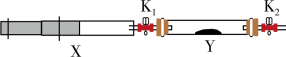
在一定温度下按图示装置进行实验,打开 ,推动注射器活塞,使X中的气体缓慢通入Y管中,反应的化学方程式为
,推动注射器活塞,使X中的气体缓慢通入Y管中,反应的化学方程式为________ 。
Ⅱ.下图是探究铜与浓硫酸反应生成硫酸铜的实验装置图:

(4)写出装置B中发生反应的离子方程式________ ,写出图中虚线框内装置的作用________ 。
Ⅲ. 如图所示, 分子呈正四面体结构。
分子呈正四面体结构。
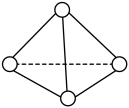
(5)已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则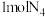 气体转化为
气体转化为 时要
时要________ (填“吸收”或“放出”)热量________ kJ。
 并探究
并探究 的相关性质(部分仪器已略去)。
的相关性质(部分仪器已略去)。
(1)B中圆底烧瓶收集氨气时,氨气的进气口
(2)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是
(3)查阅资料:氮的氧化物(
 )是大气污染物之一,工业上在一定温度和催化剂条件下用
)是大气污染物之一,工业上在一定温度和催化剂条件下用 将
将 还原生成无污染的物质。该小组将收集到的
还原生成无污染的物质。该小组将收集到的 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入
充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入 (两端用夹子
(两端用夹子 、
、 夹好)。
夹好)。
在一定温度下按图示装置进行实验,打开
 ,推动注射器活塞,使X中的气体缓慢通入Y管中,反应的化学方程式为
,推动注射器活塞,使X中的气体缓慢通入Y管中,反应的化学方程式为Ⅱ.下图是探究铜与浓硫酸反应生成硫酸铜的实验装置图:

(4)写出装置B中发生反应的离子方程式
Ⅲ. 如图所示,
 分子呈正四面体结构。
分子呈正四面体结构。
(5)已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则
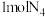 气体转化为
气体转化为 时要
时要
您最近半年使用:0次
名校
8 . 化学就在身边,下列说法中正确的是
| A.开启啤酒瓶后,瓶中马上泛起大量泡沫,此现象无法用勒夏特列原理解释 |
| B.将水坝中的钢闸门连通电源的负极对其进行保护,其原理为牺牲阳极的阴极保护法 |
| C.银锡子佩戴时间长了会发黑,将其放在盛有食盐水的铝制易拉罐(打磨后)中,可使其光亮如新 |
D.钢铁发生吸氧腐蚀时负极发生的反应为 |
您最近半年使用:0次
名校
9 . 填空
(1) 的名称为
的名称为_______ 。
(2)乙醚(C4H10O)的同分异构体有多种,请写出符合下列条件的同分异构体的结构简式_______ 。
a.属于醇类; b.不能发生催化氧化。
(3)模拟“人工树叶”电化学实验装置如下图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。

a电极的反应式为_______ ;每生成1molO2,转移_______ mol电子。
(4)高能火箭燃料肼(H2N—NH2)在燃烧过程的能量变化如下图所示。
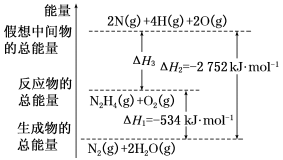
N2H4在O2中燃烧的热化学方程式为_______ 。
(1)
 的名称为
的名称为(2)乙醚(C4H10O)的同分异构体有多种,请写出符合下列条件的同分异构体的结构简式
a.属于醇类; b.不能发生催化氧化。
(3)模拟“人工树叶”电化学实验装置如下图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。

a电极的反应式为
(4)高能火箭燃料肼(H2N—NH2)在燃烧过程的能量变化如下图所示。

N2H4在O2中燃烧的热化学方程式为
您最近半年使用:0次
解题方法
10 . 铅(Pb)元素的主要化合价有+2价和+4价,溶液中铅为+2价(Pb2+或 ,铅单质及其化合物在日常生活和工业生产中具有非常广泛的用途。
,铅单质及其化合物在日常生活和工业生产中具有非常广泛的用途。
(1)Pb3O4 俗名红丹,在涂料工业中用作防锈颜料,Pb3O4中+2价铅和+4价铅的原子个数之比为
(2)Pb、PbO2可用于制造铅蓄电池,铅蓄电池工作时的反应方程式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,该反应中还原产物为
(3)工业上利用铅渣(主要成分是PbO、Pb,以及少量不溶于硝酸的杂质)生产PbSO4的流程如图:
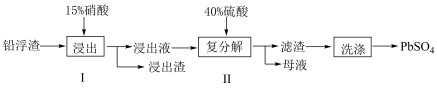
已知步骤1有NO产生,试写出Pb与硝酸反应的化学方程式
(4)血铅是指血液中铅元素的含量。血铅超标会引起机体的神经系统、血液系统、消化系统的一系列异常表现。某人血液中铅的浓度为0.4μg/mL,若转化为物质的量浓度为
您最近半年使用:0次



