解题方法
1 . 若CH4、C2H6、C3H8、C4H10四种烃各为1 mol,在足量O2中燃烧,消耗O2最多的是______ (填化学式,下同);上述四种烃各为1 g,在足量O2中燃烧,消耗O2最多的是_______ ;1 mol C3H8在足量O2中燃烧,消耗O2_______ mol。(相对分子质量:C:12,H:1)
您最近一年使用:0次
解题方法
2 . 顺1,2二甲基环丙烷和反1,2二甲基环丙烷可发生如下转化:

该反应的速率方程可表示为:v(正)=k(正)·c(顺)和v(逆)=k(逆)·c(反),k(正)和k(逆)在一定温度时为常数,分别称作正、逆反应速率常数。已知:t1温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数值K=_______ 。

该反应的速率方程可表示为:v(正)=k(正)·c(顺)和v(逆)=k(逆)·c(反),k(正)和k(逆)在一定温度时为常数,分别称作正、逆反应速率常数。已知:t1温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数值K=
您最近一年使用:0次
解题方法
3 . 某些化学键的键能(kJ·mol-1)如下表:
(1)1 mol H2在2 mol Cl2中燃烧,生成2 mol HCl放出的热量为_______ kJ。
(2)在一定条件下,1 mol H2分别与足量的Cl2、Br2、I2完全反应,放出热量由多到少的顺序是_______ 。
| 键 | H—H | Br—Br | I—I | Cl—Cl | H—Cl | H—I | H—Br |
| 键能 | 436 | 193 | 151 | 247 | 431 | 299 | 366 |
(2)在一定条件下,1 mol H2分别与足量的Cl2、Br2、I2完全反应,放出热量由多到少的顺序是
您最近一年使用:0次
解题方法
4 . 以甲烷为原料制取氢气是工业上常用的制氢方法。已知有关化学反应的能量变化如图所示:
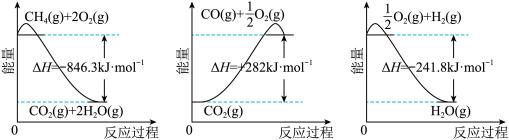
(1)下列说法正确的是___________(填字母)。
(2)CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为___________ 。

(1)下列说法正确的是___________(填字母)。
| A.CH4的摩尔燃烧焓为846.3 kJ·mol-1 |
| B.CO的摩尔燃烧焓为282 kJ·mol-1 |
| C.H2的摩尔燃烧焓为241.8 kJ·mol-1 |
| D.CO(g)+H2O(g)=CO2(g)+H2(g)为放热反应 |
您最近一年使用:0次
5 . 二甲醚(CH3OCH3)重整制取氢气,具有无毒性、无刺激性等优点,发生反应:CH3OCH3(g)=CO(g)+H2(g)+CH4(g) ΔH。已知部分化学键的键能如下表所示:
计算该反应的ΔH值。_________
| 化学键 | C-H | C-O | H-H | C≡O(CO) |
| 键能/(kJ·mol-1) | 413 | 356 | 436 | 1 075 |
您最近一年使用:0次
6 . 已知丙烷的摩尔燃烧焓ΔH=-2215kJ·mol-1。试计算丙烷完全燃烧生成1.8g水时放出的热量。_____
您最近一年使用:0次
7 . 已知1 g丁烷(C4H10)完全燃烧生成二氧化碳和液态水时,放出50 kJ的热量。
(1)请写出丁烷燃烧的热化学方程式_______ 。
(2)计算10 kg丁烷完全燃烧生成二氧化碳和液态水时放出的热量_______ 。
(1)请写出丁烷燃烧的热化学方程式
(2)计算10 kg丁烷完全燃烧生成二氧化碳和液态水时放出的热量
您最近一年使用:0次
解题方法
8 . 25 ℃、101kPa时,1 mol FeS2(s)完全燃烧生成Fe2O3(s)和SO2(g),放出853 kJ热量。
(1)请写出FeS2(s)燃烧的热化学方程式________ 。
(2)计算理论上180 g FeS2(s)完全燃烧放出的热量________ 。
(1)请写出FeS2(s)燃烧的热化学方程式
(2)计算理论上180 g FeS2(s)完全燃烧放出的热量
您最近一年使用:0次
解题方法
9 . 无色气体N2O4是一种强氧化剂,为重要的火箭推进剂之一。N2O4与NO2转换的热化学方程式为N2O4(g)⇌2NO2(g) ΔH=+24.4 kJ·mol-1。上述反应中,正反应速率v正=k正·p(N2O4),逆反应速率v逆=k逆·p2(NO2),其中k正、k逆为速率常数,则Kp为_______ (以k正、k逆表示)。若将一定量N2O4投入真空容器中恒温恒压分解(温度298 K、压强100 kPa),已知该条件下k正=4.8×104 s-1,当N2O4分解10%时,v正=_______ kPa·s-1。
您最近一年使用:0次
解题方法
10 . 已知2N2O5(g)=2N2O4(g)+O2(g),起始时N2O5(g)为35.8 kPa,分解的反应速率v=2×10-3×pN2O5(kPa·min-1)。t=62 min时,测得体系中pO2=2.9 kPa,则此时的pN2O5=_______ kPa,v=_______ kPa·min-1。
您最近一年使用:0次



