1 . A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
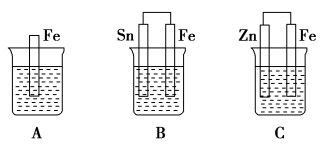
(1)A中反应的离子方程式为___________ 。
(2)B中锡极为________ 极,电极反应式为_________ ,锡极附近溶液的酸性_________ (填“增强”“减弱”或“不变”)。B中Fe极为________ 极,电极反应式为_________ 。
(3)C中被氧化的金属是___________ ,总反应的化学方程式为___________ 。
(4)A、B、C中铁被氧化由快到慢的顺序是___________ 。

(1)A中反应的离子方程式为
(2)B中锡极为
(3)C中被氧化的金属是
(4)A、B、C中铁被氧化由快到慢的顺序是
您最近一年使用:0次
2 . 如图所示是某同学利用注射器设计的简易实验装置。加热分离出可燃冰中的甲烷,将10mL甲烷注入甲注射器中,在同温、同压下向乙注射器中注入50mLCl2,将乙注射器中气体推入甲注射器中,用日光照射甲注射器一段时间,气体在甲注射器中发生反应。
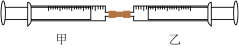
(1)下列是某同学预测的实验现象,其中正确的是___________(填字母)。
(2)甲注射器中发生的化学反应类型为___________ 。
(3)反应后,甲注射器中剩余气体最好用___________(填字母)吸收。

(1)下列是某同学预测的实验现象,其中正确的是___________(填字母)。
| A.气体最终变为无色 |
| B.实验过程中,甲注射器活塞向右移动 |
| C.甲注射器内壁有油状液滴产生 |
| D.产生火花 |
(2)甲注射器中发生的化学反应类型为
(3)反应后,甲注射器中剩余气体最好用___________(填字母)吸收。
| A.水 | B.氢氧化钠溶液 |
| C.硝酸银溶液 | D.饱和食盐水 |
您最近一年使用:0次
3 . 化学反应的速率与限度在社会生产、生活和科学研究中具有广泛的应用,对人类文明的进步和现代化建设具有重大的价值,与我们每个人息息相关。恒温条件下,在5L恒容密闭容器内充入1.5molX(g)与2.0molY(g),反应10min后达到平衡,此时X的物质的量减少1mol,Y的物质的量浓度为0.2mol·L-1,0~10min内,生成Z的平均反应速率为0.04mol·L-1·min-1。请回答下列问题:
(1)该反应的化学方程式为___________ 。
(2)0~10min内,v(Y)=___________ mol·L-1·min-1。
(3)反应达到平衡状态时,X、Y的转化率分别为___________ 、___________ (保留三位有效数字)。
(4)298K时,将一定物质的量浓度的Na3AsO3、I2和NaOH三种溶液混合,发生反应:AsO (aq)+I2(aq)+2OH-(aq)⇌AsO
(aq)+I2(aq)+2OH-(aq)⇌AsO (aq)+2I-(aq)+H2O(l)。溶液中c(AsO
(aq)+2I-(aq)+H2O(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
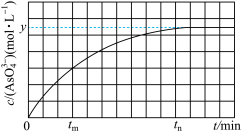
①tm时,v(正)___________ v(逆)(填“>”“<”或“=”)。
②从0到tn时,v(OH-)=___________ 。
③下列可判断反应达到平衡的是___________ (填标号)。
a.溶液的pH不再变化 b.v(I-)=2v(AsO ) c.
) c.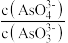 不再变化
不再变化
(1)该反应的化学方程式为
(2)0~10min内,v(Y)=
(3)反应达到平衡状态时,X、Y的转化率分别为
(4)298K时,将一定物质的量浓度的Na3AsO3、I2和NaOH三种溶液混合,发生反应:AsO
 (aq)+I2(aq)+2OH-(aq)⇌AsO
(aq)+I2(aq)+2OH-(aq)⇌AsO (aq)+2I-(aq)+H2O(l)。溶液中c(AsO
(aq)+2I-(aq)+H2O(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
①tm时,v(正)
②从0到tn时,v(OH-)=
③下列可判断反应达到平衡的是
a.溶液的pH不再变化 b.v(I-)=2v(AsO
 ) c.
) c.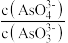 不再变化
不再变化
您最近一年使用:0次
4 . 海洋资源的利用具有广阔前景。
(1)不需要经过化学变化就能从海水中获得的物质是___________(填字母)。
(2)下图是从海水中提取镁的简单流程。
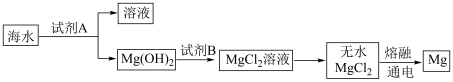
①工业上常用于沉淀Mg2+的试剂A是___________ ,Mg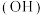 2转化为MgCl2的离子方程式是
2转化为MgCl2的离子方程式是___________ 。
②由无水MgCl2制取Mg的化学方程式是___________ 。
(1)不需要经过化学变化就能从海水中获得的物质是___________(填字母)。
| A.Cl2 | B.淡水 | C.烧碱 | D.粗盐 |
(2)下图是从海水中提取镁的简单流程。

①工业上常用于沉淀Mg2+的试剂A是
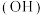 2转化为MgCl2的离子方程式是
2转化为MgCl2的离子方程式是②由无水MgCl2制取Mg的化学方程式是
您最近一年使用:0次
5 . I.在一定条件下,向VL密闭容器中充入amolSO2和bmolO2,发生反应:2SO2(g)+O2(g) 2SO3(g)。
2SO3(g)。
(1)当反应进行到v正与v逆___________ 时,此时可逆反应达到最大限度,若保持外界条件不变时,混合物中各组分的物质的量、浓度、质量分数、体积分数及总压强都___________ 。
II.NO2与SO2混合可发生放热反应:NO2+SO2⇌SO3+NO。在100℃下将1molNO2与1molSO2的混合气体置于绝热(不与外界进行热交换)恒容密闭容器中发生上述反应。
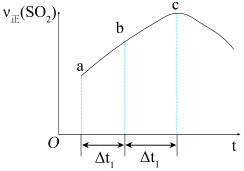
(2)SO2的正反应速率随时间变化的趋势如图所示,则下列说法正确的是_________(填字母,下同)。
(3)判断此反应达到平衡状态的标志是___________ 。
A.体系的压强不再发生变化
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.各组分的物质的量浓度不再改变
E.体系的温度不再发生变化
F.v正(NO2)=v逆(NO)
 2SO3(g)。
2SO3(g)。(1)当反应进行到v正与v逆
II.NO2与SO2混合可发生放热反应:NO2+SO2⇌SO3+NO。在100℃下将1molNO2与1molSO2的混合气体置于绝热(不与外界进行热交换)恒容密闭容器中发生上述反应。
(2)SO2的正反应速率随时间变化的趋势如图所示,则下列说法正确的是_________(填字母,下同)。

| A.反应在c点达到平衡状态 |
| B.反应物浓度:a点小于b点 |
| C.当Δt1=Δt2时,SO2的平均反应速率:ab段小于bc段 |
| D.当Δt1=Δt2时,SO2的消耗量:ab段大于bc段 |
(3)判断此反应达到平衡状态的标志是
A.体系的压强不再发生变化
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.各组分的物质的量浓度不再改变
E.体系的温度不再发生变化
F.v正(NO2)=v逆(NO)
您最近一年使用:0次
6 . 为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如下图:
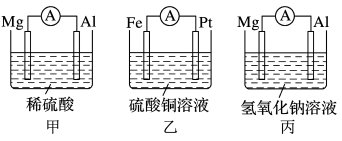
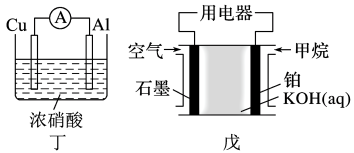
回答下列问题:
(1)根据原电池原理填写下表:
(2)电极类型除与电极材料的性质有关外,还与___________ 有关。
(3)根据上述电池分析,负极材料是否一定参加电极反应?___________ (填“是”“否”或“不一定”),请举例说明:___________ 。
(4)指出下列电池的放电过程中,电解质溶液酸碱性的变化:甲酸性___________ ,丙碱性___________ 。


回答下列问题:
(1)根据原电池原理填写下表:
| 装置序号 | 正极 | 负极反应式 | 阳离子移动方向 |
| 甲 | |||
| 乙 | |||
| 丙 | |||
| 丁 | |||
| 戊 |
(2)电极类型除与电极材料的性质有关外,还与
(3)根据上述电池分析,负极材料是否一定参加电极反应?
(4)指出下列电池的放电过程中,电解质溶液酸碱性的变化:甲酸性
您最近一年使用:0次
7 . 如果将燃料燃烧设计成燃料电池就可避免NOx的生成,某种燃料电池的工作原理如图所示,a、b均为惰性电极。
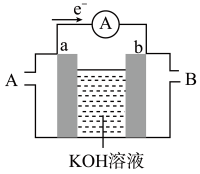
(1)使用时,空气从___________ 口通入(填“A”或“B”);当外电路通过0.4mol的电子时,消耗O2的体积___________ L(标况下)。
(2)假设使用的燃料是甲烷(CH4),a极的电极反应式为___________ 。

(1)使用时,空气从
(2)假设使用的燃料是甲烷(CH4),a极的电极反应式为
您最近一年使用:0次
8 . 有一种有机物的结构简式为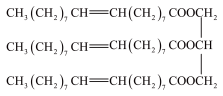 ,试回答下列问题:
,试回答下列问题:
(1)该化合物是___________(填字母,下同)。
(2)该化合物的密度________ 。
A.比水大 B.比水小 C.与水相同
(3)常温下该化合物是________ 。
A.液态 B.固态 C.气态
(4)下列物质中,能与该物质反应的有________ 。
A.NaOH溶液 B.溴水 C.乙醇 D.乙酸 E.H2
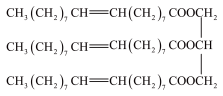 ,试回答下列问题:
,试回答下列问题:(1)该化合物是___________(填字母,下同)。
| A.烯烃 | B.油脂 | C.蛋白质 | D.糖类 |
(2)该化合物的密度
A.比水大 B.比水小 C.与水相同
(3)常温下该化合物是
A.液态 B.固态 C.气态
(4)下列物质中,能与该物质反应的有
A.NaOH溶液 B.溴水 C.乙醇 D.乙酸 E.H2
您最近一年使用:0次
9 . 已知丁酸跟乙酸具有相似的化学性质,丁醇跟乙醇具有相似的化学性质。丁醇和丁酸的结构简式如下:
丁醇:CH3CH2CH2CH2OH、
丁酸:CH3CH2CH2COOH。
试回答下列问题:
(1)分别写出丁醇、丁酸与Na反应的化学方程式:
丁醇+钠:___________ ,
丁酸+钠:___________ 。
预测上述化学反应的速率:v(丁醇)___________ (填“>”或“<”)v(丁酸)。
(2)写出丁酸与丁醇发生酯化反应的化学方程式:____________ (说明反应条件)。
丁醇:CH3CH2CH2CH2OH、
丁酸:CH3CH2CH2COOH。
试回答下列问题:
(1)分别写出丁醇、丁酸与Na反应的化学方程式:
丁醇+钠:
丁酸+钠:
预测上述化学反应的速率:v(丁醇)
(2)写出丁酸与丁醇发生酯化反应的化学方程式:
您最近一年使用:0次
解题方法
10 . 按要求回答下列问题:
(1)某烃的结构简式为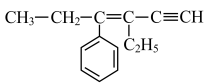 ,该分子中可能共面的碳原子数最多有
,该分子中可能共面的碳原子数最多有___________ 个,一定在同一个平面上的原子至少有___________ 个。
(2)常温下,某气态烃与氧气混合装入密闭容器中,点燃爆炸后回到原温度,此时容器内气体的压强为反应前的一半,经氢氧化钠溶液吸收后,容器内几乎成真空,此烃可能是___________ (写出结构简式)。
(1)某烃的结构简式为
 ,该分子中可能共面的碳原子数最多有
,该分子中可能共面的碳原子数最多有(2)常温下,某气态烃与氧气混合装入密闭容器中,点燃爆炸后回到原温度,此时容器内气体的压强为反应前的一半,经氢氧化钠溶液吸收后,容器内几乎成真空,此烃可能是
您最近一年使用:0次



