1 . 已知 ,如果要合成
,如果要合成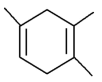 ,所用的起始原料可以是
,所用的起始原料可以是
| A.1,3—戊二烯和2—丁炔 |
| B.2,3—二甲基—1,3—丁二烯和丙烯 |
| C.2,3—二甲基—1,3—戊二烯和乙炔 |
| D.2—甲基—1,3—丁二烯和2—丁炔 |
您最近一年使用:0次
2023-05-06更新
|
833次组卷
|
8卷引用:黑龙江省哈尔滨师范大学附属中学2019-2020学年高二下学期期中考试化学试题
黑龙江省哈尔滨师范大学附属中学2019-2020学年高二下学期期中考试化学试题山东省实验中学2023届高三下学期5月第一次模拟考试化学试题江西省赣州市第一中学2021-2022学年高二下学期中期质量检测(1)化学试题江苏省南京市燕子矶中学2022-2023学年高二下学期3月月考化学试题(已下线)专题10 有机物结构与性质-2023年高考化学真题题源解密(新高考专用)黑龙江省鸡西实验中学2022-2023学年高二下学期7月期末考试化学试题吉林省长春市第十七中学2022-2023学年高二下学期7月期末考试化学试题(已下线)第1讲 有机化合物的结构特点与研究方法
2 . 以下是有关胶体性质的实验探究,回答相关的问题。
Fe(OH)3胶体的制备:
(1)实验室制取Fe(OH)3胶体的方法是_______ ;该反应的离子方程式是:_______ 。制备Fe(OH)3胶体用到的FeCl3溶解在盐酸溶液中制备得到,需要用盐酸溶液的理由是:_______ 。
(2)制备得到的Fe(OH)3胶体体系具有的性质是_______ (填写序号字母)。
a.光束通过该液体的形成光亮的“通路”
b.静止一段时间后,该红褐色液体仍然澄清透明
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(3)在分离和提纯Fe(OH)3胶体时用到的方法是:_______ (填分离操作的名称)。
Fe(OH)3胶体的制备:
(1)实验室制取Fe(OH)3胶体的方法是
(2)制备得到的Fe(OH)3胶体体系具有的性质是
a.光束通过该液体的形成光亮的“通路”
b.静止一段时间后,该红褐色液体仍然澄清透明
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(3)在分离和提纯Fe(OH)3胶体时用到的方法是:
您最近一年使用:0次
名校
3 . 孔雀石的主要成分为xCuCO3•yCu(OH)2•zH2O,为测定其中CuCO3的质量分数,称取a g样品进行实验。下列实验方案可行的是
| A.充分加热样品,用碱石灰吸收逸出气体,增重b g |
| B.加热至样品质量不再发生变化,称得其质量为b g |
| C.向样品中加入足量的稀盐酸,用排水法收集逸出气体,得b mL气体 |
| D.向样品中加入足量的稀盐酸,充分反应,将生成的气体全部通入到足量Ba(OH)2溶液中,过滤、洗涤、烘干,得b g固体 |
您最近一年使用:0次
2023-04-26更新
|
301次组卷
|
3卷引用:北京市中国人民大学附属中学2020届高三化学质检试题
名校
解题方法
4 . 将标准状况下的22.4L SO2通入4mol NaOH溶液中,下列用来解释事实的方程式中不合理的是(已知室温下饱和Na2SO3溶液的pH约为8.3)
A.标准状况下的22.4L SO2通入含4mol NaOH的溶液:2OH-+SO2=SO +H2O +H2O |
B.上述反应后所得溶液的pH约为12:SO +H2O +H2O HSO HSO +OH- +OH- |
C.向上述反应后所得溶液中,通入氯气,pH下降:SO +Cl2+2OH-=SO +Cl2+2OH-=SO +2Cl-+H2O +2Cl-+H2O |
D.向上述反应后所得溶液中,滴加少量H2O2和BaCl2溶液的混合液,产生白色沉淀:SO +Ba2++H2O2=BaSO4↓+H2O +Ba2++H2O2=BaSO4↓+H2O |
您最近一年使用:0次
2023-04-21更新
|
251次组卷
|
2卷引用:北京市中国人民大学附属中学2017-2018学年高三上学期12月月考化学试题
名校
解题方法
5 . 某学习小组拟对KMnO4与Na2S的反应进行了探究。所有探究实验中所使用的KMnO4溶液均为浓酸酸化的0.1mol/LKMnO4溶液[c(H+)=1.5mol/L]。
资料显示:
Ⅰ.Na2SX可溶于水,Na2SX在酸性条件下不稳定。
П.MnS为肉红色固体,难溶于水。
(1)请写出实验a中Na2S与KMnO4发生的化学反应方程式___________ 。
(2)针对实验b中,静置后淡黄色沉淀溶解的原因,小组同学提出两种假设:
假设i:淡黄色沉淀溶于水中;
假设ii:淡黄色沉淀与Na2S反应得到Na2SX并溶解。
①小组同学仔细分析实验过程后,认为假设i不成立,其依据为:___________ 。
②小组同学通过进一步实验证实溶液中存在Na2SX。请用化学用语说明设计该实验所依据的化学原理:___________
(3)请结合平衡移动原理,解释实验abc中,仅c得到肉红色固体的原因:___________ 。
(4)为探究实验d中所得棕褐色固体的组成,小组同学继续进行了实验e.某同学分析后,认为黑色固体为纯净的某种物质,并设计实验证实了他的猜想。其实验操作为:___________ 。
(5)实验d中,两溶液混合后立即发生的复分解反应可能干扰氧化还原反应的进行,请设计实验,在排除上述干扰的前提下探究等体积的KMnO4溶液与0.1mol/LNa2S溶液反应的可能的还原产物。(已知:该条件KMnO4可反应完全)。(请将实验装置补充完整,标出所用试剂,并描述实验操作)___________ 。

(6)综合以上实验,KMnO4酸性溶液与Na2S溶液反应的复杂性,与___________ 有关。
| 实验 | 操作 | 现象 |
| a | 向2mL0.1mol/LNa2S溶液中滴加3滴KMnO4溶液,振荡,静置 | 溶液中出现黄色浑浊,得到淡黄色沉淀、无色溶液 |
| b | 向2mL1.0mol/LNa2S溶液中滴加3滴KMnO4溶液,振荡,静置 | 溶液中出现黄色浑浊,浑浊消失,得到浅黄色溶液 |
| c | 向2mL2.4mol/LNa2S溶液中滴加3滴KMnO4溶液,振荡,静置 | 有肉红色固体生成,上清液为 浅黄色 |
| d | 向2mLKMnO4溶液中滴加0.1mol/LNa2S溶液 | 立即有臭鸡蛋气味气体生成,稍后,有棕褐色固体生成 |
| e | 取少量d中所得固体,滴加1.0mol/LNa2S溶液,振荡,静置 | 得到黑色固体,浅黄色溶液 |
Ⅰ.Na2SX可溶于水,Na2SX在酸性条件下不稳定。
П.MnS为肉红色固体,难溶于水。
(1)请写出实验a中Na2S与KMnO4发生的化学反应方程式
(2)针对实验b中,静置后淡黄色沉淀溶解的原因,小组同学提出两种假设:
假设i:淡黄色沉淀溶于水中;
假设ii:淡黄色沉淀与Na2S反应得到Na2SX并溶解。
①小组同学仔细分析实验过程后,认为假设i不成立,其依据为:
②小组同学通过进一步实验证实溶液中存在Na2SX。请用化学用语说明设计该实验所依据的化学原理:
(3)请结合平衡移动原理,解释实验abc中,仅c得到肉红色固体的原因:
(4)为探究实验d中所得棕褐色固体的组成,小组同学继续进行了实验e.某同学分析后,认为黑色固体为纯净的某种物质,并设计实验证实了他的猜想。其实验操作为:
(5)实验d中,两溶液混合后立即发生的复分解反应可能干扰氧化还原反应的进行,请设计实验,在排除上述干扰的前提下探究等体积的KMnO4溶液与0.1mol/LNa2S溶液反应的可能的还原产物。(已知:该条件KMnO4可反应完全)。(请将实验装置补充完整,标出所用试剂,并描述实验操作)

(6)综合以上实验,KMnO4酸性溶液与Na2S溶液反应的复杂性,与
您最近一年使用:0次
名校
解题方法
6 . NaClO2是重要漂白剂和消毒剂,主要用于水、砂糖、油脂的漂白杀菌。
已知:i.NaClO2在溶液中过饱和时,若溶液温度低于38℃,析出NaClO2•3H2O;若溶液温度高于38℃,则析出NaClO2;若溶液温度高于60℃,NaClO2分解为NaClO3和NaCl。
ii.ClO2气体浓度超过10%时,长期存放易发生嫌炸性分解。通常需现用现制。
iii.ClO2气体在中性和碱性溶液中不能稳定存在。
【实验室制备】实验室设计如下实验制备如图亚氯酸钠(NaClO2)晶体。
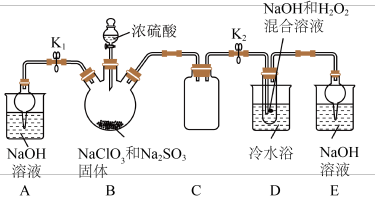
已知:装置B中发生的主要反应:2NaClO3+Na2SO3+H2SO4(浓)=2ClO2↑+2Na2SO4+H2O
(1)ClO2气体与装置D中混合溶液反应生成NaClO2,每转移1mol电子,生成NaClO2的质量为___________
(2)反应结束后,为从D试管中溶液获得NaClO2晶体,需进行以下操作。请补充完整:
①55℃蒸发结晶;
②趁热过滤;
③用___________ ℃热水洗涤晶体;
④低温干燥,得到成品。
(3)实验须使B中NaClO3稍微过量,原因是____________ :如NaClO3不足,则装置D中可能产生 ,检验装置D中是否含有
,检验装置D中是否含有 的方法是:取少量D中反应后的溶液于试管中,
的方法是:取少量D中反应后的溶液于试管中,___________ ,证明溶液中存在 。
。
(4)实验结束后,关闭K2,打开K1。在一段时间后断开K2左侧橡胶管与玻璃管的连接,并从接口处向C中鼓入一定量空气。以上操作的目的是___________ 。
【工业制备】
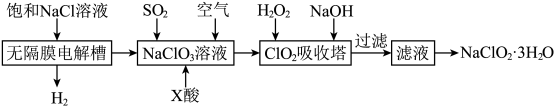
(5)在无隔膜电解槽中阳极的电极反应式:___________ 。
(6)吸收塔内的温度不能过高的原因为___________ 。
(7)吸收塔内ClO2随着还原剂的不同和溶液酸碱性的变化可被还原为 或Cl-。ClO2被S2-还原为
或Cl-。ClO2被S2-还原为 、Cl-的转化率与溶液pH的关系如图所示。请写出pH≤2时ClO2与S2-反应的离子方程式:
、Cl-的转化率与溶液pH的关系如图所示。请写出pH≤2时ClO2与S2-反应的离子方程式:___________ 。

已知:i.NaClO2在溶液中过饱和时,若溶液温度低于38℃,析出NaClO2•3H2O;若溶液温度高于38℃,则析出NaClO2;若溶液温度高于60℃,NaClO2分解为NaClO3和NaCl。
ii.ClO2气体浓度超过10%时,长期存放易发生嫌炸性分解。通常需现用现制。
iii.ClO2气体在中性和碱性溶液中不能稳定存在。
【实验室制备】实验室设计如下实验制备如图亚氯酸钠(NaClO2)晶体。

已知:装置B中发生的主要反应:2NaClO3+Na2SO3+H2SO4(浓)=2ClO2↑+2Na2SO4+H2O
(1)ClO2气体与装置D中混合溶液反应生成NaClO2,每转移1mol电子,生成NaClO2的质量为
(2)反应结束后,为从D试管中溶液获得NaClO2晶体,需进行以下操作。请补充完整:
①55℃蒸发结晶;
②趁热过滤;
③用
④低温干燥,得到成品。
(3)实验须使B中NaClO3稍微过量,原因是
 ,检验装置D中是否含有
,检验装置D中是否含有 的方法是:取少量D中反应后的溶液于试管中,
的方法是:取少量D中反应后的溶液于试管中, 。
。(4)实验结束后,关闭K2,打开K1。在一段时间后断开K2左侧橡胶管与玻璃管的连接,并从接口处向C中鼓入一定量空气。以上操作的目的是
【工业制备】

(5)在无隔膜电解槽中阳极的电极反应式:
(6)吸收塔内的温度不能过高的原因为
(7)吸收塔内ClO2随着还原剂的不同和溶液酸碱性的变化可被还原为
 或Cl-。ClO2被S2-还原为
或Cl-。ClO2被S2-还原为 、Cl-的转化率与溶液pH的关系如图所示。请写出pH≤2时ClO2与S2-反应的离子方程式:
、Cl-的转化率与溶液pH的关系如图所示。请写出pH≤2时ClO2与S2-反应的离子方程式:
您最近一年使用:0次
2023-04-21更新
|
406次组卷
|
3卷引用:北京市中国人民大学附属中学2017届高三下学期三模化学试题
名校
解题方法
7 . 化合物H是一种香料,存在于金橘中,可用如下路线合成:
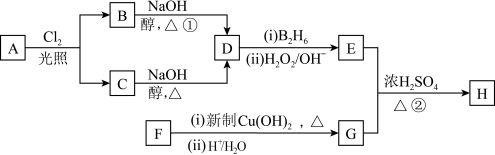
已知:R-CH=CH2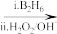 R-CH2CH2OH(B2H4为乙硼烧)
R-CH2CH2OH(B2H4为乙硼烧)
回答下列问题:
(1)质谱仪测定显示,烃A的相对分子质量为58。A的分子式是___________ 。
(2)B和C均为一氯代烃。其中,C的核磁共振氧谱只有1个信号峰。请写出B的名称___________ ,反应①的反应类型为___________ 。
(3)在催化剂存在条件下,1molF与2molH2反应,生成3-苯基-1-丙醇。F的结构简式为___________ 。
(4)新制Cu(OH)2悬浊液的配制方法为(填序号)___________ 。
a.在试管中加入2mL10%的NaOH溶液,滴入4~6滴2%的CuSO4溶液,振荡
b.在试管中加入2mLl%的NaOH溶液,滴入2mL2%的CuSO4溶液,振荡
c.在试管中加入4~6滴2%的NaOH溶液,滴入2mLl%的CuSO4溶液,振荡
(5)反应②的化学方程式为___________ 。
(6)在一定条件下,H可以形成一种高分子化合物,其结构简式为___________ 。
(7)写出所有与G具有相同官能团的G的芳香族同分异构体的结构简式:___________ 。
(8)已知:i.H2C=CH-CH3+HBr CH3CHBrCH3+BrCH2CH2CH3,两种产物的物质的量分数:95%,5%
CH3CHBrCH3+BrCH2CH2CH3,两种产物的物质的量分数:95%,5%
ii.RCH2Br RCH2COOH
RCH2COOH
请以丙烯为唯一有机原料,选用必要的无机试剂合成1-丁酸___________ 。

已知:R-CH=CH2
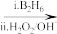 R-CH2CH2OH(B2H4为乙硼烧)
R-CH2CH2OH(B2H4为乙硼烧)回答下列问题:
(1)质谱仪测定显示,烃A的相对分子质量为58。A的分子式是
(2)B和C均为一氯代烃。其中,C的核磁共振氧谱只有1个信号峰。请写出B的名称
(3)在催化剂存在条件下,1molF与2molH2反应,生成3-苯基-1-丙醇。F的结构简式为
(4)新制Cu(OH)2悬浊液的配制方法为(填序号)
a.在试管中加入2mL10%的NaOH溶液,滴入4~6滴2%的CuSO4溶液,振荡
b.在试管中加入2mLl%的NaOH溶液,滴入2mL2%的CuSO4溶液,振荡
c.在试管中加入4~6滴2%的NaOH溶液,滴入2mLl%的CuSO4溶液,振荡
(5)反应②的化学方程式为
(6)在一定条件下,H可以形成一种高分子化合物,其结构简式为
(7)写出所有与G具有相同官能团的G的芳香族同分异构体的结构简式:
(8)已知:i.H2C=CH-CH3+HBr
 CH3CHBrCH3+BrCH2CH2CH3,两种产物的物质的量分数:95%,5%
CH3CHBrCH3+BrCH2CH2CH3,两种产物的物质的量分数:95%,5%ii.RCH2Br
 RCH2COOH
RCH2COOH请以丙烯为唯一有机原料,选用必要的无机试剂合成1-丁酸
您最近一年使用:0次
名校
解题方法
8 . 科学家尝试用微生物电池除去废水中的有害的有机物,其原理如图所示。下列有关说法正确的是
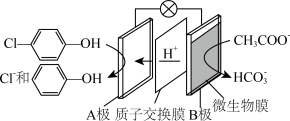

A.若1mol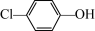 转化为1mol苯酚转移2mole-,则同时生成的X为氯气 转化为1mol苯酚转移2mole-,则同时生成的X为氯气 |
B.用该电池电解饱和食盐水(使用情性电极的电解槽)每产生22.4L的氢气,B极上生成0.5mol |
| C.A极为正极,B极为负极 |
| D.电池工作过程中A极周围溶液pH不断增大 |
您最近一年使用:0次
9 . 化学镀的原理是利用化学反应生成金属单质沉淀在镀件表面形成的镀层。某化学镀铜的反应速率随镀液pH变化如图所示。(已知:该镀铜过程中,镀液pH控制在12.5左右)。根据图中信息,下列说法正确的是


| A.若采用电镀的方法,镀件应与电源正极连接 |
| B.若用铜盐进行化学镀铜,镀件做氧化剂 |
| C.可以调节溶液的pH至8-9之间使反应停止 |
| D.同等条件下,使用化学镀比电镀反应速率更快 |
您最近一年使用:0次
解题方法
10 . 学好化学让生活更美好。下列说法错误 的是
| A.高锰酸钾溶液、84消毒液、双氧水能杀菌消毒,都利用了其强氧化性 |
| B.电热水器用镁棒防止内胆腐蚀,原理是牺牲阳极的阴极保护法 |
| C.海洋中含有丰富的资源,仅利用物理方法就可以获得NaCl、Br2和Mg |
| D.港珠澳大桥采用的超高分子量聚乙烯纤维吊绳,是有机高分子化合物 |
您最近一年使用:0次



