1 . Ⅰ.有两个试管分别装有等浓度的Na2CO3和NaHCO3溶液,
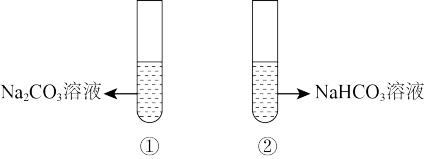
(1)分别加入澄清石灰水,产生沉淀的是_______ ,(填写试管序号,下同。)
(2)逐滴加入等浓度的盐酸,立即产生气泡者的是_______ 。
Ⅱ.铁及其化合物在生产、生活中存在广泛用途。回答下列问题。
(3)可以通过_______ 来鉴别FeCl3溶液和Fe(OH)3胶体;
(4)绿矾(FeSO4·7H2O)可用于治疗缺铁性贫血,其水溶液露置于空气中会变质。实验室中检验绿矾晶体是否变质的操作是:_______ 。写出该反应的离子方程式:_______ 。
(5)写铁与水蒸气反应的化学方程式:_______ 。
(6)现将一包铜铁的混合粉末放入盛有FeCl3溶液的烧杯中,充分反应后烧杯中仍有少量固体,该固体不和盐酸反应。关于烧杯中物质组成的说法正确的是_______。(填序号)。

(1)分别加入澄清石灰水,产生沉淀的是
(2)逐滴加入等浓度的盐酸,立即产生气泡者的是
Ⅱ.铁及其化合物在生产、生活中存在广泛用途。回答下列问题。
(3)可以通过
(4)绿矾(FeSO4·7H2O)可用于治疗缺铁性贫血,其水溶液露置于空气中会变质。实验室中检验绿矾晶体是否变质的操作是:
(5)写铁与水蒸气反应的化学方程式:
(6)现将一包铜铁的混合粉末放入盛有FeCl3溶液的烧杯中,充分反应后烧杯中仍有少量固体,该固体不和盐酸反应。关于烧杯中物质组成的说法正确的是_______。(填序号)。
| A.溶液中有FeCl2 | B.溶液中含有FeCl2、FeCl3 |
| C.固体中含有铜和铁 | D.溶液中只含FeCl3 |
您最近一年使用:0次
2 . 锂是最轻的活泼金属,其单质及其化合物有广泛的用途。回答下列问题:
(1)用碳酸锂和盐酸反应可制备氯化锂。实验室用密度为1.20 g/mL,质量分数为36.5%的浓盐酸配制240 mL 0.1 mol/L的盐酸,该浓盐酸的物质的量浓度为___________ ;配制240 mL 0.1 mol/L的盐酸需要的玻璃仪器为:烧杯、玻璃棒、量筒、胶头滴管和___________ 。
(2)锂在空气中受热燃烧生成物的化学式是___________ ;不可使用二氧化碳灭火器扑灭因金属锂引起的火灾,原因是(用化学方程式表示)___________ 。
(3)以废旧的 电池正极材料(含
电池正极材料(含 、Al等)为原料,通过浸出、除铝和沉淀处理后可制备
、Al等)为原料,通过浸出、除铝和沉淀处理后可制备 。
。
①浸出:用 溶液浸取正极材料中的铁元素。正极材料中的
溶液浸取正极材料中的铁元素。正极材料中的 与
与 反应的微观过程如图1所示。
反应的微观过程如图1所示。

 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
②除铝:30℃时,向浸出液中加入氢氟酸,生成 沉淀。生成
沉淀。生成 沉淀的离子方程式为
沉淀的离子方程式为___________ 。研究发现,铝元素去除率随溶液初始pH变化如图2所示,则溶液初始pH为___________ 时,铝元素去除率最高。

③沉淀:向除铝后溶液中加入一定量 溶液,生成
溶液,生成 沉淀。选用
沉淀。选用 的理由是
的理由是___________ 。
(1)用碳酸锂和盐酸反应可制备氯化锂。实验室用密度为1.20 g/mL,质量分数为36.5%的浓盐酸配制240 mL 0.1 mol/L的盐酸,该浓盐酸的物质的量浓度为
(2)锂在空气中受热燃烧生成物的化学式是
(3)以废旧的
 电池正极材料(含
电池正极材料(含 、Al等)为原料,通过浸出、除铝和沉淀处理后可制备
、Al等)为原料,通过浸出、除铝和沉淀处理后可制备 。
。①浸出:用
 溶液浸取正极材料中的铁元素。正极材料中的
溶液浸取正极材料中的铁元素。正极材料中的 与
与 反应的微观过程如图1所示。
反应的微观过程如图1所示。
 与
与 反应的化学方程式为
反应的化学方程式为②除铝:30℃时,向浸出液中加入氢氟酸,生成
 沉淀。生成
沉淀。生成 沉淀的离子方程式为
沉淀的离子方程式为
③沉淀:向除铝后溶液中加入一定量
 溶液,生成
溶液,生成 沉淀。选用
沉淀。选用 的理由是
的理由是
您最近一年使用:0次
解题方法
3 . 前香港中文大学校长高锟和George A· Hockham首先提出光纤可用于通信传输的设想,高锟因此获得2009年诺贝尔物理学奖。石英光纤是以二氧化硅为主要原料制备的光纤,下列有关SiO2性质和用途的说法不正确的是
| A.SiO2是酸性氧化物,能和烧碱溶液反应 |
| B.工业上利用SiO2、纯碱、大理石混合高温共热制备玻璃 |
| C.SiO2能溶于氢氟酸、浓硫酸、浓硝酸 |
| D.在高温下SiO2和焦炭反应可制备粗硅 |
您最近一年使用:0次
名校
4 . 如图是利用氯碱工业的原理图。回答下列问题:
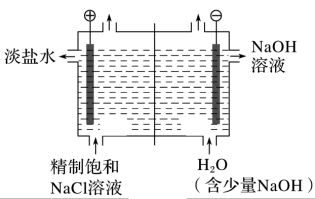
(1)请写出氯碱工业的电极反应方程式:__ ,__ 。(注明电极)
(2)图中的离子交换膜是__ (填“阳离子”或“阴离子”)交换膜,采用该离子交换膜的作用有__ (写出一点)。
(3)请写出检验左室气体产物的方法__ 。
(4)请写出NaOH在工业上的一种用途__ 。

(1)请写出氯碱工业的电极反应方程式:
(2)图中的离子交换膜是
(3)请写出检验左室气体产物的方法
(4)请写出NaOH在工业上的一种用途
您最近一年使用:0次
5 . 我们可以根据物质的组成,性质,结构或用途等进行分类。下列关于物质的分类正确的是
| A.天然气—化石燃料;金刚石和石墨—碳的同位素 |
| B.亚硫酸氢钠—正盐;95%酒精—消毒剂 |
| C.氢氟酸—弱酸;石墨烯—无机非金属材料 |
| D.稀豆浆—胶体;NH4Cl —共价化合物 |
您最近一年使用:0次
6 . 氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高。不溶于酸(氢氟酸除外)。高温下氧气及水蒸气能明显腐蚀氮化硅。一种用工业硅(含少量铁、铜的单质及氧化物)和 (含少量
(含少量 )合成氮化硅的工艺流程如下:
)合成氮化硅的工艺流程如下:

(1) 净化时,铜屑的作用是
净化时,铜屑的作用是___________ ;将硅块粉碎的作用是___________ 。
(2)在氮化炉中每生成 转移电子的物质的量是
转移电子的物质的量是___________ 。
(3)X可能是___________ (选填:“盐酸”、“硝酸”、“硫酸”、“氢氟酸”)。
(4)如何说明氮化硅产品已用水洗干净?___________ 。
(5)推测氮化硅可能有哪些用途:___________ (填字母)。
a.制作切削刀具 b.制作坩埚
c.用作建筑陶瓷 d.制作耐高温轴承
(6)工业上还可以采用化学气相沉积法,在 的保护下,使
的保护下,使 与
与 在高温下反应生成
在高温下反应生成 沉积在石墨表面,该反应的化学方程式为
沉积在石墨表面,该反应的化学方程式为___________ 。
 (含少量
(含少量 )合成氮化硅的工艺流程如下:
)合成氮化硅的工艺流程如下:
(1)
 净化时,铜屑的作用是
净化时,铜屑的作用是(2)在氮化炉中每生成
 转移电子的物质的量是
转移电子的物质的量是(3)X可能是
(4)如何说明氮化硅产品已用水洗干净?
(5)推测氮化硅可能有哪些用途:
a.制作切削刀具 b.制作坩埚
c.用作建筑陶瓷 d.制作耐高温轴承
(6)工业上还可以采用化学气相沉积法,在
 的保护下,使
的保护下,使 与
与 在高温下反应生成
在高温下反应生成 沉积在石墨表面,该反应的化学方程式为
沉积在石墨表面,该反应的化学方程式为
您最近一年使用:0次
7 . 铜及其化合物在电子工业、材料工业、工农业生产及日常生活方面用途非常广泛。回答下列有关问题:
(1)Cu位于周期表中___________ (填“s”、“p”、“d”或“ds”)区,1mol基态 中未成对电子数为
中未成对电子数为___________ 。
(2)下表是Fe和Cu的部分电离能数据:
请解释 大于
大于 的主要原因:
的主要原因:___________ 。
(3)向盛有 水溶液的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色的透明溶液。
水溶液的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色的透明溶液。
(已知: 结构如图,是狭长八面体。)
结构如图,是狭长八面体。)

①根据以上信息,判断化合物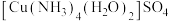 加热时首先失去的组分是
加热时首先失去的组分是___________ ,判断理由是___________ 。
②比较键角:
___________  (填“大于”或“小于”),其原因是
(填“大于”或“小于”),其原因是___________ 。
③ 的空间构型是
的空间构型是___________ 。从分子结构解释 酸性强于
酸性强于 的原因是
的原因是___________ 。
(4)四方晶系 晶胞结构如图所示。
晶胞结构如图所示。

①该化合物中铜的配位数为___________ 。
②已知: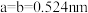 ,
, ,
, 为阿伏加德罗常数的值
为阿伏加德罗常数的值 晶体的密度是
晶体的密度是___________  (列出计算式)。
(列出计算式)。
(1)Cu位于周期表中
 中未成对电子数为
中未成对电子数为(2)下表是Fe和Cu的部分电离能数据:
| 元素 | Fe | Cu |
第一电离能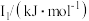 | 759 | 746 |
第二电离能 | 1561 | 1958 |
请解释
 大于
大于 的主要原因:
的主要原因:(3)向盛有
 水溶液的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色的透明溶液。
水溶液的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色的透明溶液。(已知:
 结构如图,是狭长八面体。)
结构如图,是狭长八面体。)
①根据以上信息,判断化合物
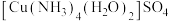 加热时首先失去的组分是
加热时首先失去的组分是②比较键角:

 (填“大于”或“小于”),其原因是
(填“大于”或“小于”),其原因是③
 的空间构型是
的空间构型是 酸性强于
酸性强于 的原因是
的原因是(4)四方晶系
 晶胞结构如图所示。
晶胞结构如图所示。
①该化合物中铜的配位数为
②已知:
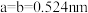 ,
, ,
, 为阿伏加德罗常数的值
为阿伏加德罗常数的值 晶体的密度是
晶体的密度是 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
8 . 物质的性质决定物质的用途。下列有关物质的性质与其对应用途的描述,错误的是
| 选项 | 物质的性质 | 物质的用途 |
| A | 液氨汽化吸收大量热 | 液氨作制冷剂 |
| B | 铁不与浓硫酸反应 | 用铁罐储运浓硫酸 |
| C | 二氧化硫有还原性 | 葡萄酒中添加二氧化硫抗氧化 |
| D | 二氧化硅有光学特性 | 二氧化硅制光导纤维 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-04-30更新
|
338次组卷
|
4卷引用:山西省太原市2020-2021学年高一下学期期中考试化学试题
山西省太原市2020-2021学年高一下学期期中考试化学试题黑龙江省牡丹江市第三高级中学2021-2022学年高一下学期期中考试化学试题(已下线)云南省昆明市官渡区第二中学2023-2024学年高二上学期开学考试化学试题云南省昆明市官渡区第二中学2023-2024学年高三上学期开学考试化学试题



