名校
1 . 葡萄糖酸钙是一种重要的补钙剂,工业上以葡萄糖、碳酸钙为原料,在溴化钠溶液中采用间接电氧化反应制备葡萄糖酸钙,其阳极区反应过程如下:
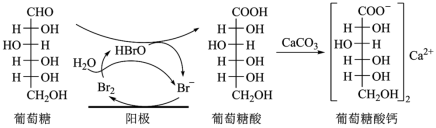
| A.溴化钠起催化和导电作用 |
B.每生成 葡萄糖酸钙,理论上电路中转移了0.1NA电子 葡萄糖酸钙,理论上电路中转移了0.1NA电子 |
| C.葡萄糖酸能通过分子内反应生成含有六元环状结构的产物 |
| D.葡萄糖能发生氧化、还原、取代、加成和消去反应 |
您最近一年使用:0次
7日内更新
|
80次组卷
|
2卷引用:2024届宁夏回族自治区银川一中高三下学期第四次模拟考试理科综合试卷-高中化学
名校
解题方法
2 . I.汽车尾气中含有CO、NOx等有害气体。
(1)NOx能形成酸雨,氮有多种价态的氧化物,氮元素从+1~+5价都有对应的氧化物,常见的有N2O、NO、N2O3、NO2(或N2O4)、N2O5,其中属于酸性氧化物的是___________ 。
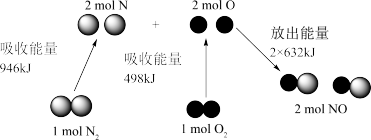
(2)汽车尾气中NO生成过程的能量变化示意图如下:___________ (填“吸热”或“放热”)___________ kJ的能量。
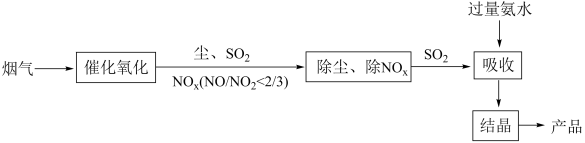
Ⅱ.目前工业上烟气脱硫脱硝的工艺流程如下: > 9)。
> 9)。
(3)“氧化”的目的是___________ 。图中产品中含硫成分为___________ (填化学式)。
Ⅲ.海洋生物参与氮循环的过程如图所示(其它含氮物质不参与反应)。___________ 种价态。反应③和⑤中,若生成等物质的量的N2,则转移的电子数之比为___________ 。
Ⅳ.利用NaOH溶液吸收NO2,避免硝酸生产尾气中的氮氧化物对环境的破坏作用。
(5)已知用NaOH溶液吸收时会生成NaNO2和另一种盐,则吸收NO2的离子方程式为___________ 。
(1)NOx能形成酸雨,氮有多种价态的氧化物,氮元素从+1~+5价都有对应的氧化物,常见的有N2O、NO、N2O3、NO2(或N2O4)、N2O5,其中属于酸性氧化物的是
(2)汽车尾气中NO生成过程的能量变化示意图如下:
Ⅱ.目前工业上烟气脱硫脱硝的工艺流程如下:
 > 9)。
> 9)。(3)“氧化”的目的是
Ⅲ.海洋生物参与氮循环的过程如图所示(其它含氮物质不参与反应)。
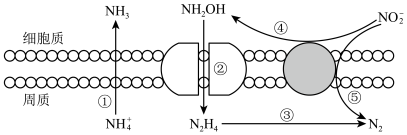
Ⅳ.利用NaOH溶液吸收NO2,避免硝酸生产尾气中的氮氧化物对环境的破坏作用。
(5)已知用NaOH溶液吸收时会生成NaNO2和另一种盐,则吸收NO2的离子方程式为
您最近一年使用:0次
名校
解题方法
3 . 高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。回答下列问题:
(1)SiO2属于___________ (填“酸性”“碱性”或“两性”)氧化物。盛装NaOH溶液的试剂瓶不能用玻璃塞,其原因为___________ (用离子方程式表示)。
(2)用氮化硅(Si3N4)陶瓷制造发动机,能大幅度提高发动机的热效率。工业上制备氮化硅的原理为:3SiCl4+2N2+6H2 Si3N4+12HCl。
Si3N4+12HCl。
①SiCl4是___________ (填“离子化合物”或“共价化合物”)。
②若该反应转移3mol电子,生成Si3N4的质量为___________ g。
(3)芯片制作中的部分流程如图:___________ 。
Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是___________ 。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
②去除磷硅玻璃即除去扩散制结过程中产生的SiO2,下列试剂合适的为___________ (填标号),写出其化学方程式:___________ 。
a.浓硫酸 b.氢氟酸 c.稀硝酸
(1)SiO2属于
(2)用氮化硅(Si3N4)陶瓷制造发动机,能大幅度提高发动机的热效率。工业上制备氮化硅的原理为:3SiCl4+2N2+6H2
 Si3N4+12HCl。
Si3N4+12HCl。①SiCl4是
②若该反应转移3mol电子,生成Si3N4的质量为
(3)芯片制作中的部分流程如图:

Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
②去除磷硅玻璃即除去扩散制结过程中产生的SiO2,下列试剂合适的为
a.浓硫酸 b.氢氟酸 c.稀硝酸
您最近一年使用:0次
名校
4 . 下表是元素周期表的一部分,请按要求回答下列问题:___________ 。
(2)写出⑥最高价氧化物的电子式___________ 。
(3)在②~⑤元素中,原子半径最大的是___________ (填元素符号)。
(4)比较④、⑤、⑥、⑦离子的半径大小___________ (用离子符号表示且用“>”连接)。
(5)以上这些元素中,最不活泼的金属元素是___________ (填元素符号),这些元素的最高价氧化物对应的水化物中,碱性最强的是___________ (填化学式)。
(6)砷(As)是人体必需的微量元素,与③同一主族,As原子比③原子多两个电子层,则砷在周期表中的位置为___________ ,该族第二到四周期元素的气态氢化物的稳定性从大到小的顺序是___________ (用化学式表示且用“>”连接)。

(2)写出⑥最高价氧化物的电子式
(3)在②~⑤元素中,原子半径最大的是
(4)比较④、⑤、⑥、⑦离子的半径大小
(5)以上这些元素中,最不活泼的金属元素是
(6)砷(As)是人体必需的微量元素,与③同一主族,As原子比③原子多两个电子层,则砷在周期表中的位置为
您最近一年使用:0次
5 . 下列反应是氧化还原反应且反应物的总能量低于生成物的总能量的是
| A.CaO+H2O=Ca(OH)2 | B.NaOH+HCl=NaCl+H2O |
| C.2Na2O2+2H2O=4NaOH+O2↑ | D.4HNO3 4NO2+O2+2H2O 4NO2+O2+2H2O |
您最近一年使用:0次
名校
解题方法
6 . 某无色混合气体中可能含有N2、O2、SO2、NO、NO2,现将此混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。下列判断中不正确的是
| A.肯定没有NO2 | B.肯定有SO2 | C.可能有N2和O2 | D.肯定有NO |
您最近一年使用:0次
名校
解题方法
7 . 现有a、b、c、d四个金属电极,用导线两两相连组成原电池。
①a、b相连插入硫酸铜溶液中后,b极变粗;
②a、d相连插入稀硫酸中后,外电路电流从a流向d;
③b、c相连插入稀硫酸中后,c极上有气泡产生;
④c、d相连插入稀硫酸中后,d极溶解。
由此可判断这四种金属的活动性顺序是
①a、b相连插入硫酸铜溶液中后,b极变粗;
②a、d相连插入稀硫酸中后,外电路电流从a流向d;
③b、c相连插入稀硫酸中后,c极上有气泡产生;
④c、d相连插入稀硫酸中后,d极溶解。
由此可判断这四种金属的活动性顺序是
| A.d>a>c>b | B.b>c>d>a | C.d>a>b>c | D.a>b>d>c |
您最近一年使用:0次
名校
解题方法
8 . 蘸有浓氨水的玻璃棒靠近X有白烟产生,X不可能是
| A.浓盐酸 | B.浓硫酸 | C.浓硝酸 | D.氯气 |
您最近一年使用:0次
名校
解题方法
9 . 关于硅及其相关化合物的叙述正确的是
| A.自然界中存在天然游离的硅单质 |
| B.已知C与Si的最高正价都是+4价,由于CO2+H2O=H2CO3,用类比法推知,SiO2+H2O=H2SiO3 |
| C.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物 |
| D.硅元素在金属与非金属的分界线处,因此硅单质具有弱导电性,一般可用于作为半导体材料 |
您最近一年使用:0次
10 . 火药的发明推进了人类历史发展的进程。火药爆炸的原理为S+3C+2KNO3=K2S+N2↑+3CO2↑。下列说法错误的是
| A.KNO3、K2S 均属于钾盐 |
| B.该反应每转移1.2mol电子,生成标准状况下8.96L气体 |
| C.从得失电子角度看,S、C在反应中的作用不同 |
| D.该反应过程属于氮的固定 |
您最近一年使用:0次



