解题方法
1 . 下列化学用语正确的是
A.NaHSO4在水中电离:NaHSO4=Na++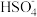 |
B.钠离子的结构示意图: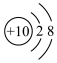 |
| C.次氯酸的结构式:H—O—Cl |
D.CCl4的空间填充模型: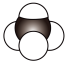 |
您最近一年使用:0次
2 . Ⅰ.请根据题意选择下列物质,并用其字母代号填空:
A.明矾[KAl(SO4)2] B.Ca(OH)2 C.NaHCO3 D.水玻璃
(1)要使焙制的糕点,松软可以添加________ 。
(2)要使含泥沙的水变澄清,可使用________ 。
(3)要中和钢铁厂,电镀厂产生的酸性废水可使用__________ 。
(4)可用作防火材料的是________ 。
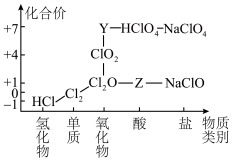
Ⅱ.以化合价为纵坐标,物质类别为横坐标的图像称为“价—类”二维图。如图是氯元素的部分“价—类”二维图。
(5)工业上干燥的Cl2贮存在________ 中。
(6)Y的化学式为________ 。
(7)Cl2转化成Z和HCl的离子方程式为________________ 。
(8)将Cl2与SO2按1∶1通入紫色石蕊溶液中,现象为_________________ 。
A.明矾[KAl(SO4)2] B.Ca(OH)2 C.NaHCO3 D.水玻璃
(1)要使焙制的糕点,松软可以添加
(2)要使含泥沙的水变澄清,可使用
(3)要中和钢铁厂,电镀厂产生的酸性废水可使用
(4)可用作防火材料的是
Ⅱ.以化合价为纵坐标,物质类别为横坐标的图像称为“价—类”二维图。如图是氯元素的部分“价—类”二维图。
(5)工业上干燥的Cl2贮存在
(6)Y的化学式为
(7)Cl2转化成Z和HCl的离子方程式为
(8)将Cl2与SO2按1∶1通入紫色石蕊溶液中,现象为
您最近一年使用:0次
解题方法
3 . 学习小组在实验室中利用下图装置制备SO2并进行相关性质的探究。
(1)仪器Q的名称为_________ 。
(2)装置B是为了观察气体的流速,则试剂M为_________(填字母)。
(3)装置C中出现的现象说明SO2具有_________ 性。
(4)装置E中__________________ (填现象)可说明SO2具有还原性,发生反应的离子方程式为__________________ 。
(5)装置F的作用是_________ 。
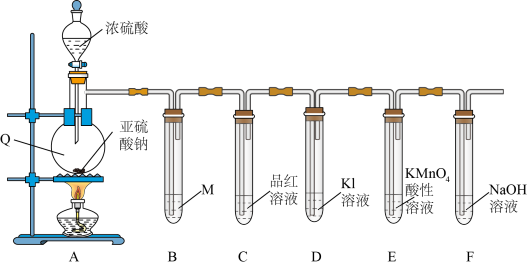
(1)仪器Q的名称为
(2)装置B是为了观察气体的流速,则试剂M为_________(填字母)。
| A.NaOH溶液 | B.饱和NaHSO3溶液 | C.Na2S溶液 | D.Na2SO3溶液 |
(3)装置C中出现的现象说明SO2具有
(4)装置E中
(5)装置F的作用是
您最近一年使用:0次
解题方法
4 . 在配制一定物质的量浓度的溶液时,不会用到的仪器是
A. | B.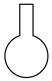 | C.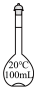 | D.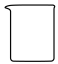 |
您最近一年使用:0次
解题方法
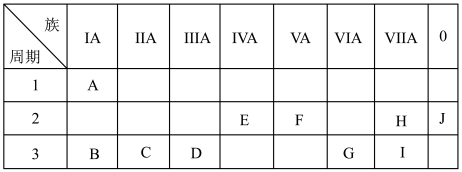
5 . 如图是元素周期表中的一部分。
(1)化学性质最不活泼的元素是_________ ,氧化性最强的单质是__________ 。
(2)最高价氧化物对应的水化物中,碱性最强的是_________ ,呈两性的是_________ 。
(3)在B、C、D、G、I中,原子半径最大的是_________ ,它们的离子半径最大是_________ (填离子符号)。
(4)B的最高价氧化物的水化物与G的最高价氧化物的水化物反应的化学方程式为___________________ 。
(1)化学性质最不活泼的元素是
(2)最高价氧化物对应的水化物中,碱性最强的是
(3)在B、C、D、G、I中,原子半径最大的是
(4)B的最高价氧化物的水化物与G的最高价氧化物的水化物反应的化学方程式为
您最近一年使用:0次
6 . 下列以物质的量为中心的计算正确的是
| A.0.1mol·L-1CaCl2溶液中,c(Cl-)为0.05mol·L-1 |
| B.22g干冰中约含有3.01×1023个CO2分子 |
| C.常温常压下,11.2LO2的质量为16g |
| D.1molNH3的质量为10g |
您最近一年使用:0次
解题方法
7 . 下列物质分离提纯的方法中,正确的是
| A.为除去乙烯中混有的甲烷,将混合气体通入溴水 |
| B.除去乙酸乙酯中少量的乙酸;加氢氧化钠溶液,充分振荡,过滤 |
| C.用盐酸溶液除去BaSO4中混有的CaCO3 |
| D.用饱和Na2CO3溶液除去CO2中的HCl |
您最近一年使用:0次
解题方法
8 . 在2L的密闭容器内,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间变化如下表:
2NO2(g)体系中,n(NO)随时间变化如下表:
(1)用NO表示0~2s内该反应的平均速率v(NO)=_______ mol·L-1·s-1。
(2)下列措施能够使该反应速率加快的是_______ (填字母,下同)。
a.降低温度 b.减小压强 c.使用催化剂
(3)若上述反应在恒容的密闭容器中进行,下列叙述中能说明该反应已达平衡状态的是_______ (填字母)。
a.c(NO):c(O2)=2:1
b.混合气体的颜色保持不变
c.每消耗1molO的同时生成2molNO2
 2NO2(g)体系中,n(NO)随时间变化如下表:
2NO2(g)体系中,n(NO)随时间变化如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)下列措施能够使该反应速率加快的是
a.降低温度 b.减小压强 c.使用催化剂
(3)若上述反应在恒容的密闭容器中进行,下列叙述中能说明该反应已达平衡状态的是
a.c(NO):c(O2)=2:1
b.混合气体的颜色保持不变
c.每消耗1molO的同时生成2molNO2
您最近一年使用:0次
解题方法
9 . 有下列六种有机化合物,请根据要求填空。__________ 。
(2)前三种化合物中能使溴的四氯化碳溶液褪色的是__________ (写名称);发生反应的反应类型为__________ 。
(3)属于环状分子不饱和烃是__________ (写序号)。
(4)④与⑤互为__________ (填“同系物”或“同分异构体”,下同);③与⑥互为___________ 。
(5)③与④反应的化学方程式为____________________ 。
①CH2=CH2 ②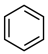 ③CH3COOH ④C2H5OH ⑤CH3OCH3 ⑥HCOOH
③CH3COOH ④C2H5OH ⑤CH3OCH3 ⑥HCOOH
(2)前三种化合物中能使溴的四氯化碳溶液褪色的是
(3)属于环状分子不饱和烃是
(4)④与⑤互为
(5)③与④反应的化学方程式为
您最近一年使用:0次
解题方法
10 . 下列指定反应的离子方程式正确的是
| A.Fe2O3溶于稀硫酸:Fe2O3+6H+=2Fe2++3H2O |
B.盐酸溶解CaCO3: +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
C.H2SO4溶液与Ba(OH)2溶液反应:Ba2++ =BaSO4↓ =BaSO4↓ |
| D.过氧化钠样品溶于水:2Na2O2+2H2O=4Na++4OH-+O2↑ |
您最近一年使用:0次



