名校
1 . 黄金(Au)可溶于王水,反应方程式: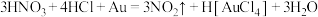 ,下列叙述正确的是
,下列叙述正确的是
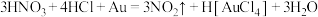 ,下列叙述正确的是
,下列叙述正确的是A.王水是浓硝酸和浓盐酸(物质的量之比为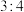 )的混合物 )的混合物 |
B.反应中 、 、 表现出强氧化性 表现出强氧化性 |
C.反应中转移 电子,产生 电子,产生 (标准状况下) (标准状况下) |
D.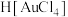 既是氧化产物,又是还原产物 既是氧化产物,又是还原产物 |
您最近一年使用:0次
名校
解题方法
2 . 氨和硫化氢都是非金属元素的气态氢化物,下列关于两者的实验室制法的说法正确的是
| A.发生装置都可以使用启普发生器 | B.都能用无水氯化钙干燥 |
| C.都能利用复分解反应制取 | D.都能用向下排空气法收集 |
您最近一年使用:0次
名校
3 . NCl3(其中N为-3价)可用于漂白和杀菌消毒。NCl3水解的反应原理示意图如题图所示。下列说法正确的是
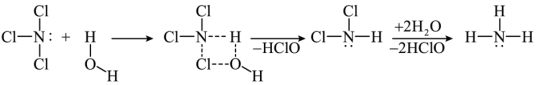
A.HClO的结构式为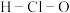 |
B.键角 大于 大于 |
C.基态N原子的轨道表示式为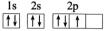 违背了泡利不相容原理 违背了泡利不相容原理 |
D. 的水解过程中 的水解过程中 原子的杂化轨道类型发生了变化 原子的杂化轨道类型发生了变化 |
您最近一年使用:0次
昨日更新
|
116次组卷
|
2卷引用:江苏省前黄高级中学2024届高三下学期二模适应性考试(二)化学试卷
4 . 下列各组指定粒子数目相等的是
A. 和 和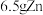 分别与足量稀硝酸反应转移电子数 分别与足量稀硝酸反应转移电子数 |
B. 乙二醇含 乙二醇含 杂化的原子数和常温常压下 杂化的原子数和常温常压下 氖气含原子数 氖气含原子数 |
C.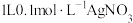 溶液制得 溶液制得 胶粒数与 胶粒数与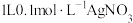 溶液中 溶液中 数 数 |
D. 和 和 的混合气体含分子数和标准状况下 的混合气体含分子数和标准状况下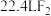 含原子数 含原子数 |
您最近一年使用:0次
5 . 秦始皇陵是我国历史上规模最大的帝王陵墓,秦始皇陵兵马俑被誉为“世界第八大奇迹”,考古发现并出土了大量竹简、兵马俑、钱币、石甲胄等珍贵文物,下列说法错误 的是
| A.竹简密封保存,并充以氮气,可延缓其降解 |
| B.陶制兵马俑的烧制过程涉及化学变化 |
| C.铜制钱币比铁制钱币的耐腐蚀性更强 |
| D.石甲胄的主要成分为合金 |
您最近一年使用:0次
名校
6 . 银氨溶液不能储存,因为放置时会析出有强爆炸性的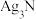 沉淀。可通过加入盐酸转化为AgCl沉淀回收,还可利用羟胺回收银,反应如下:
沉淀。可通过加入盐酸转化为AgCl沉淀回收,还可利用羟胺回收银,反应如下: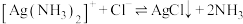 ;
; 。设阿伏加德罗常数值为
。设阿伏加德罗常数值为 。下列说法正确的是
。下列说法正确的是
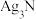 沉淀。可通过加入盐酸转化为AgCl沉淀回收,还可利用羟胺回收银,反应如下:
沉淀。可通过加入盐酸转化为AgCl沉淀回收,还可利用羟胺回收银,反应如下: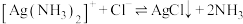 ;
; 。设阿伏加德罗常数值为
。设阿伏加德罗常数值为 。下列说法正确的是
。下列说法正确的是A.向银氨溶液中加入1mol HCl,可以回收AgCl为 |
B.1mol/L  溶液含有配位键数为2 溶液含有配位键数为2 |
C.等物质的量的 和羟胺均含有3 和羟胺均含有3 个氢原子 个氢原子 |
D.羟胺有强还原性,当反应中转移电子数为2 时,需消耗2mol 时,需消耗2mol  |
您最近一年使用:0次
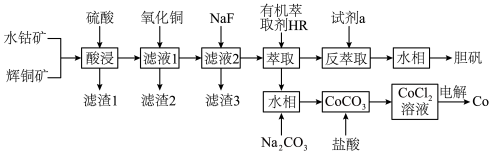
7 . 以水钴矿(Co2O3·H2O,含Fe2O3、MgO、CaO)和辉铜矿(Cu2S,含SiO2、Fe2O3)为原料制取胆矾和单质钴。
①常温下,Ksp(MgF2)=6.25×10-9,Ksp(CaSO4)=7.1×10-7,Ksp(CoCO3)=2.4×10-7;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
③萃取Cu2+的反应原理;Cu2++2HR CuR2+2H+;
CuR2+2H+;
④Mg、Ca、Fe、Co均能与强酸反应产生H2。
回答下列问题:
(1)“酸浸”过程硫元素价态变为+6价,写出“酸浸”过程中主要反应的化学方程式:___________ 。
(2)“滤渣1”的主要成分为___________ 。
(3)常温下,“滤液1”中(Fe元素都以Fe3+形式存在)加“氧化铜”调pH不小于___________ 。
(4)常温下,若“滤液2”中c(Mg2+)=0.015mol/L(忽略溶液中极少量的Ca2+),除去2L“滤液2”中的Mg2+,至少需加入NaF固体的质量为___________ g(忽略溶液体积的变化)。
(5)“反萃取”步骤中加入的“试剂a”为___________ 。
(6)采用惰性电极电解CoCl2溶液﹑在无离子交换膜的条件下,不能用CoSO4溶液代替CoCl2溶液的理由是___________ 。
(7)将制得的胆矾配成溶液,先加入足量氨水,得到深蓝色溶液,再通入SO2至弱酸性,生成白色沉淀。经仪器分析:白色沉淀含H、N,O、S、Cu五种元素,且Cu∶N∶S=1∶1∶l;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为三角锥形和正四面体形。则白色沉淀的化学式为___________ 。
①常温下,Ksp(MgF2)=6.25×10-9,Ksp(CaSO4)=7.1×10-7,Ksp(CoCO3)=2.4×10-7;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 金属离子 | Fe3+ | Fe2+ | Co2+ | Cu2+ |
| 开始沉淀时(c=0.01mol/L)的pH | 2.7 | 7.5 | 7.6 | 4.7 |
| 完全沉淀时(c=10-5mol/L)的pH | 3.7 | 9.0 | 9.1 | 6.2 |
 CuR2+2H+;
CuR2+2H+;④Mg、Ca、Fe、Co均能与强酸反应产生H2。
回答下列问题:
(1)“酸浸”过程硫元素价态变为+6价,写出“酸浸”过程中主要反应的化学方程式:
(2)“滤渣1”的主要成分为
(3)常温下,“滤液1”中(Fe元素都以Fe3+形式存在)加“氧化铜”调pH不小于
(4)常温下,若“滤液2”中c(Mg2+)=0.015mol/L(忽略溶液中极少量的Ca2+),除去2L“滤液2”中的Mg2+,至少需加入NaF固体的质量为
(5)“反萃取”步骤中加入的“试剂a”为
(6)采用惰性电极电解CoCl2溶液﹑在无离子交换膜的条件下,不能用CoSO4溶液代替CoCl2溶液的理由是
(7)将制得的胆矾配成溶液,先加入足量氨水,得到深蓝色溶液,再通入SO2至弱酸性,生成白色沉淀。经仪器分析:白色沉淀含H、N,O、S、Cu五种元素,且Cu∶N∶S=1∶1∶l;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为三角锥形和正四面体形。则白色沉淀的化学式为
您最近一年使用:0次
8 .  的一种制备方法如图所示,下列说法不正确的是
的一种制备方法如图所示,下列说法不正确的是
 的一种制备方法如图所示,下列说法不正确的是
的一种制备方法如图所示,下列说法不正确的是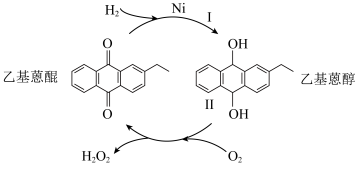
| A.反应Ⅰ中乙基蒽醌被氧化为乙基蒽醇 |
| B.催化剂镍改变了反应速率,未改变反应焓变 |
C.制备原理是 |
| D.乙基蒽醌是总反应的催化剂 |
您最近一年使用:0次
名校
解题方法
9 .  沸点为-87.5℃,可与
沸点为-87.5℃,可与 浴液反应:
浴液反应: ,
, 为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是
 沸点为-87.5℃,可与
沸点为-87.5℃,可与 浴液反应:
浴液反应: ,
, 为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是A.生成1mol ,转移的电子数为2 ,转移的电子数为2 |
B.生成2mol ,断裂的P-H键与O-H键数目比为3∶4 ,断裂的P-H键与O-H键数目比为3∶4 |
C.消耗标准状况下11.2L ,生成2molCu ,生成2molCu |
D.消耗含有孤电子对数4 的 的 ,生成2mol ,生成2mol |
您最近一年使用:0次
10 . 下列关于 的说法不正确的是
的说法不正确的是
 的说法不正确的是
的说法不正确的是A. 的电子式为 的电子式为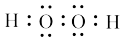 |
B. 是一种绿色氧化剂的原因是氧化产物为 是一种绿色氧化剂的原因是氧化产物为 |
C. 能杀菌消毒的原理是 能杀菌消毒的原理是 的氧化性 的氧化性 |
D. 的漂白原理与 的漂白原理与 的漂白原理不同 的漂白原理不同 |
您最近一年使用:0次



