解题方法
1 . 现有一份部分被氧化的铜片(氧化产物为CuO),称取4.32g铜片,溶于一定体积1.00mol•L-1稀硝酸中,反应恰好完全进行,收集到无色气体448mL(已折算为标准状况)。
(1)该稀硝酸中所含HNO3的物质的量为___________ ;
(2)该铜片被氧化的百分数为___________ 。
(1)该稀硝酸中所含HNO3的物质的量为
(2)该铜片被氧化的百分数为
您最近半年使用:0次
名校
解题方法
2 . 某工厂每天燃烧含硫质量分数为0.64%的煤100吨,如果煤中的硫元素全部转化为 气体,且产生的
气体,且产生的 全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为
全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为_______ 吨。
 气体,且产生的
气体,且产生的 全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为
全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为
您最近半年使用:0次
解题方法
3 . 计算题本题要求写计算过程。
(1)计算出 的物质的量为
的物质的量为___________ 。
(2)配置 溶液,需要NaOH是多少?
溶液,需要NaOH是多少?___________
(1)计算出
 的物质的量为
的物质的量为(2)配置
 溶液,需要NaOH是多少?
溶液,需要NaOH是多少?
您最近半年使用:0次
名校
解题方法
4 . 现有下列8种物质:① ②小苏打 ③
②小苏打 ③ 溶液 ④
溶液 ④ ⑤酒精 ⑥
⑤酒精 ⑥ ⑦氢氧化铁胶体 ⑧空气
⑦氢氧化铁胶体 ⑧空气
(1) 属于分散系的是___________ (填物质序号),小苏打在水中的电离方程式为___________ 。工业制漂白粉的方程式是___________ 。
(2)若氢氧化铁胶体中混有少量的 溶液,提纯的方法是___________。
溶液,提纯的方法是___________。
(3) ⑤酒精分子中含氢原子的物质的量为
⑤酒精分子中含氢原子的物质的量为___________ ,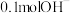 所含电子为
所含电子为___________ 个。
(4)同质量的 和
和 气体在相同条件下的体积比为
气体在相同条件下的体积比为___________ ,其中含有的氢原子数目比为___________ ,由 和
和 组成的混合气体20克,标准状态下体积
组成的混合气体20克,标准状态下体积 ,则氨气与氢气的物质的量为
,则氨气与氢气的物质的量为___________ 。
 ②小苏打 ③
②小苏打 ③ 溶液 ④
溶液 ④ ⑤酒精 ⑥
⑤酒精 ⑥ ⑦氢氧化铁胶体 ⑧空气
⑦氢氧化铁胶体 ⑧空气(1) 属于分散系的是
(2)若氢氧化铁胶体中混有少量的
 溶液,提纯的方法是___________。
溶液,提纯的方法是___________。| A.蒸馏(分馏) | B.过滤 | C.渗析 | D.蒸发 |
 ⑤酒精分子中含氢原子的物质的量为
⑤酒精分子中含氢原子的物质的量为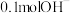 所含电子为
所含电子为(4)同质量的
 和
和 气体在相同条件下的体积比为
气体在相同条件下的体积比为 和
和 组成的混合气体20克,标准状态下体积
组成的混合气体20克,标准状态下体积 ,则氨气与氢气的物质的量为
,则氨气与氢气的物质的量为
您最近半年使用:0次
5 . 在标准状况下,将336LHCl气体溶解于1L水中,所得盐酸溶液的密度为1.18g/cm3.试计算这种盐酸溶液中溶质的物质的量浓度为___________ 。
您最近半年使用:0次
名校
解题方法
6 . 近年来,“氮排放”逐渐引起人们的重视。氮及其化合物与生产生活及环境息息相关,请回答下列问题:
(1)下列环境问题与氮的氧化物排放无关的是___________。
(2)汽车尾气中存在NO和CO,通过在排气管处加装催化剂,可以使其转化为对环境友好的物质,请写出发生反应的化学方程式___________ 。
(3)硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。
①工业生产中为了盛装大量浓硝酸,可选择___________ 作为罐体材料。
A.Mg B.Al C.Fe D.Cu
②为避免硝酸生产尾气中的NO2污染环境,可以使用具有碱性的碳酸钠溶液吸收,发生反应的离子方程式为___________ 。
③硝酸与金属反应会产生氮氧化物。在含有agHNO3的稀硝酸中,加入bg铁粉充分反应, 铁全部溶解并生成NO,有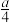 gHNO3被还原,则a:b可能为
gHNO3被还原,则a:b可能为___________ 。
A.2:1 B.3:1 C.4:1 D.8:3
(4)氮化硅(Si3N4)陶瓷材料可用于高温工程的部件、冶金工业等方面的高级耐火材料,可由石英与焦炭在高温的氮气流中制备,反应的化学方程式为___________ 。
(5)氮的同族元素锑(Sb)可形成比纯硫酸更强的酸——氟锑酸(HSbF6),称为超酸。为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为:CH3COOH+H2SO4=[CH3C(OH)2]+[HSO4]-。以此类推,H2SO4与HSbF6之间的化学反应方程式为___________ 。
(1)下列环境问题与氮的氧化物排放无关的是___________。
| A.酸雨 | B.光化学烟雾 | C.臭氧层空洞 | D.白色污染 |
(3)硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。
①工业生产中为了盛装大量浓硝酸,可选择
A.Mg B.Al C.Fe D.Cu
②为避免硝酸生产尾气中的NO2污染环境,可以使用具有碱性的碳酸钠溶液吸收,发生反应的离子方程式为
③硝酸与金属反应会产生氮氧化物。在含有agHNO3的稀硝酸中,加入bg铁粉充分反应, 铁全部溶解并生成NO,有
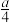 gHNO3被还原,则a:b可能为
gHNO3被还原,则a:b可能为A.2:1 B.3:1 C.4:1 D.8:3
(4)氮化硅(Si3N4)陶瓷材料可用于高温工程的部件、冶金工业等方面的高级耐火材料,可由石英与焦炭在高温的氮气流中制备,反应的化学方程式为
(5)氮的同族元素锑(Sb)可形成比纯硫酸更强的酸——氟锑酸(HSbF6),称为超酸。为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为:CH3COOH+H2SO4=[CH3C(OH)2]+[HSO4]-。以此类推,H2SO4与HSbF6之间的化学反应方程式为
您最近半年使用:0次
2024-04-30更新
|
76次组卷
|
2卷引用:湖北省新高考联考协作体2023-2024学年高一下学期期中考试化学试题(A)
7 . 某 样品露置在空气中部分变质生成
样品露置在空气中部分变质生成 ,为确定其中
,为确定其中 和
和 的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸
的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸 ,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
(1)样品中物质的量之比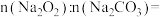
___________ 。
(2)盐酸的物质的量浓度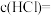
___________ 。
 样品露置在空气中部分变质生成
样品露置在空气中部分变质生成 ,为确定其中
,为确定其中 和
和 的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸
的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸 ,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:| 实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 盐酸体积/mL | 100.0 | 100.0 | 100.0 | 100.0 |
| 样品质量/g | 2.62 | 3.93 | 5.24 | 6.55 |
| 气体总体积/mL | 448 | 560 | 448 | 560 |
(1)样品中物质的量之比
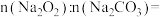
(2)盐酸的物质的量浓度
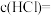
您最近半年使用:0次
名校
8 . 为保持航天器中气体成分恒定,需处理人体呼出气体。下表列出相关气体的成分及含量:
(1)上述气体组分中,N2不参与人体新陈代谢,若有100L空气被人体吸入,则相同条件下,人体呼出气体的体积为___________ L。(保留1位小数)(均为体积百分含量)
(2)设航天器内有100L空气被人体吸入,现将呼出的气体通过Na2O2处理,若Na2O2先与呼出的CO2反应,再与呼出的H2O(g)作用;试通过计算回答:欲使气体恢复至原空气成分且体积仍为100L,是否还需额外补充水蒸气。若需要,应补充多少升的水蒸气;若不需要,应使多少升的水蒸气冷凝。(计算过程保留3位小数)___________ 。
| 成分 | 人体吸入空气 | 人体呼出气体 |
| N2 | 78% | 74% |
| O2 | 21% | 16% |
| H2O(g) | 0.5% | 6% |
| CO2 | 0.03% | 4% |
(2)设航天器内有100L空气被人体吸入,现将呼出的气体通过Na2O2处理,若Na2O2先与呼出的CO2反应,再与呼出的H2O(g)作用;试通过计算回答:欲使气体恢复至原空气成分且体积仍为100L,是否还需额外补充水蒸气。若需要,应补充多少升的水蒸气;若不需要,应使多少升的水蒸气冷凝。(计算过程保留3位小数)
您最近半年使用:0次
解题方法
9 . 工业上常以铝土矿为原料来冶炼金属铝。已知:铝土矿的主要成分是 (其中含有
(其中含有 、
、 等杂质)。为检测某铝土矿样品中
等杂质)。为检测某铝土矿样品中 的含量,进行如下实验过程:
的含量,进行如下实验过程:
①取矿样10.0g加入过量稀盐酸溶解,过滤弃去不溶残渣。
②将滤液稀释并在250mL容量瓶中定容后,取25.0mL逐滴加入 的NaOH溶液。得到如右图所示的变化关系。
的NaOH溶液。得到如右图所示的变化关系。___________ 。
(2)最后所得不溶于NaOH溶液的沉淀的化学式为___________ ,其物质的量为___________ 。
(3)该铝土矿样中 的质量分数为
的质量分数为___________ 。
 (其中含有
(其中含有 、
、 等杂质)。为检测某铝土矿样品中
等杂质)。为检测某铝土矿样品中 的含量,进行如下实验过程:
的含量,进行如下实验过程:①取矿样10.0g加入过量稀盐酸溶解,过滤弃去不溶残渣。
②将滤液稀释并在250mL容量瓶中定容后,取25.0mL逐滴加入
 的NaOH溶液。得到如右图所示的变化关系。
的NaOH溶液。得到如右图所示的变化关系。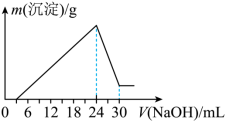
(2)最后所得不溶于NaOH溶液的沉淀的化学式为
(3)该铝土矿样中
 的质量分数为
的质量分数为
您最近半年使用:0次
解题方法
10 . 如图是某学校实验室从化学试剂商店买回来的氢氧化钠试剂标签上的部分内容。某同学从该试剂瓶中取出24.0 g固体,配成1 L溶液,请计算:
(1)所得氢氧化钠溶液的物质的量浓度为___________ 。
(2)从所得氢氧化钠溶液中取出200 mL于一烧杯中,投入2.7 g的金属铝,产生的气体在标准状况下的体积为___________ 。(写出解答步骤)
| 氢氧化钠 化学纯(CP) 500 g 品名:氢氧化钠 化学式:NaOH 相对分子质量:40 |
(2)从所得氢氧化钠溶液中取出200 mL于一烧杯中,投入2.7 g的金属铝,产生的气体在标准状况下的体积为
您最近半年使用:0次



