名校
1 . 下列与食品有关的叙述中没有涉及氧化还原反应的是
| A.用葡萄糖酸-δ-内酯做食品的凝固剂品 |
| B.用抗坏血酸做食品抗氧化剂 |
| C.将植物油氢化,以便运输和储存 |
| D.使用臭氧代替氯气进行自来水消毒 |
您最近一年使用:0次
2 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.22.4LCH4分子中含有10NA个电子 |
| B.16gCH4分子中含有4NA个C-H |
| C.等体积的CH4和NH3所含氢原子数之比为4∶3 |
| D.等质量的CH4和HF所含共价键数目之比为4∶1 |
您最近一年使用:0次
解题方法
3 . 将钛铁矿( )、磷灰石矿
)、磷灰石矿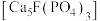 与锂灰石矿三矿耦合,按“原子经济”的绿色工艺技术路线生产磷酸铁锂,同时充分利用伴生元素。工艺流程如图。
与锂灰石矿三矿耦合,按“原子经济”的绿色工艺技术路线生产磷酸铁锂,同时充分利用伴生元素。工艺流程如图。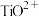 ;
;
②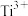 溶液为紫色;常温时,有关电对的电极电势
溶液为紫色;常温时,有关电对的电极电势
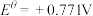 ;
;
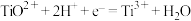
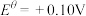 。一般标准电极电势越高,氧化剂的氧化性越强。
。一般标准电极电势越高,氧化剂的氧化性越强。
③25℃时,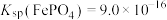 。
。
回答下列问题:
(1)Ti在元素周期表中的位置为______ 。“试剂X”为______ (填化学式)。
(2)“酸解”反应的化学方程式为______ 。
(3)“水解”过程中通过观察溶液保持紫色,判断无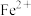 被氧化,该方法的依据是
被氧化,该方法的依据是______ 。
(4)循环利用“滤液2”的操作单元名称为______ 。“气体1”为______ (填化学式)。
(5)“沉淀”反应的化学方程式为______ 。若将铁离子恰好沉淀完全(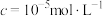 )时,
)时,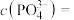
______  。
。
 )、磷灰石矿
)、磷灰石矿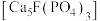 与锂灰石矿三矿耦合,按“原子经济”的绿色工艺技术路线生产磷酸铁锂,同时充分利用伴生元素。工艺流程如图。
与锂灰石矿三矿耦合,按“原子经济”的绿色工艺技术路线生产磷酸铁锂,同时充分利用伴生元素。工艺流程如图。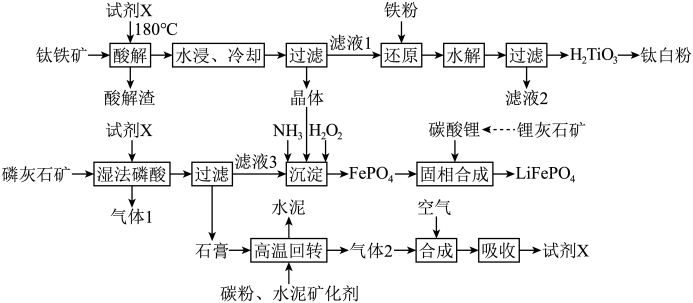
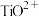 ;
;②
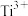 溶液为紫色;常温时,有关电对的电极电势
溶液为紫色;常温时,有关电对的电极电势
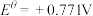 ;
;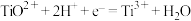
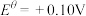 。一般标准电极电势越高,氧化剂的氧化性越强。
。一般标准电极电势越高,氧化剂的氧化性越强。③25℃时,
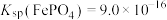 。
。回答下列问题:
(1)Ti在元素周期表中的位置为
(2)“酸解”反应的化学方程式为
(3)“水解”过程中通过观察溶液保持紫色,判断无
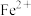 被氧化,该方法的依据是
被氧化,该方法的依据是(4)循环利用“滤液2”的操作单元名称为
(5)“沉淀”反应的化学方程式为
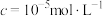 )时,
)时,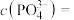
 。
。
您最近一年使用:0次
名校
4 . 由重晶石矿(主要成分是 ,含
,含 等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
 ,含
,含 等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
| A.“高温焙烧”前将原料研磨处理,能加快“高温焙烧”的反应速率 |
B.“高温焙烧”时只有 被C还原 被C还原 |
| C.“浸取过滤”发生的主要反应是氧化还原反应 |
| D.“高温焙烧”和“结晶”两处操作均需用到蒸发皿 |
您最近一年使用:0次
5 . 下列物质的电子式书写正确的是
A. | B.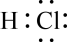 | C.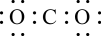 | D. 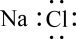 |
您最近一年使用:0次
解题方法
6 . 常温下,下列各组离子一定能在指定溶液中大量共存的是
A.与Al反应能放出H2的溶液中: 、 、 、 、 、 、 |
B.能使石蕊试液变红的透明溶液中: 、 、 、 、 、Cl- 、Cl- |
C.含大量NaHSO4的溶液中:Na+、Ca2+、CH3COO-、 |
D.能使酚酞试液变红的溶液中:K+、Na+、 、 、 |
您最近一年使用:0次
名校
解题方法
7 . 下列反应的离子方程式或化学方程式书写正确的是
A. 与 与 反应: 反应: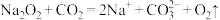 |
B.Al与NaOH溶液反应: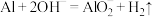 |
C. 溶液与过量NaOH溶液反应: 溶液与过量NaOH溶液反应: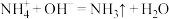 |
D.工业制粗硅: |
您最近一年使用:0次
8 . 用 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.常温常压下,22g  中所含非极性键数目为2 中所含非极性键数目为2 |
B.标准状况下, 个溴分子的体积为1L 个溴分子的体积为1L |
C.标准状况下,22.4L  中含有的 中含有的 数为 数为 |
D.28g  与 与 的混合气体含 的混合气体含 个分子 个分子 |
您最近一年使用:0次
解题方法
9 . 化学在日常防疫中发挥了重要作用,各类杀菌消毒剂逐渐被人们认识和使用。下列是我们常见的几种消毒剂:①“84”消毒液;②3%H2O2溶液;③漂白粉;④ClO2;⑤O3;⑥碘酒;⑦75%酒精;⑧高铁酸钠(Na2FeO4)。按要求回答下列问题。
(1)上述杀菌消毒剂属于电解质的是___________ ,属于非电解质的是__________ 。(填序号)。
(2)“84”消毒液可由Cl2和NaOH溶液反应制得,若与“洁厕灵”(盐酸是成分之一)混合使用会产生黄绿色有毒气体,原因是_________ (用离子方程式表示)。
(3)H2O2是一种绿色环保型消毒剂,其结构式为__________ ,含有化学键的类型为__________ 。
(4)O3是一种强氧化剂,具有强大的杀菌能力。O3与O2的关系是互为__________ 。
(5)高铁酸钠(Na2FeO4)是一种多功能新型净水剂。工业上可在NaOH溶液中,用NaClO氧化Fe(OH)3的方法制备Na2FeO4,其离子方程式为__________ ,Na2FeO4在水中可以发生反应: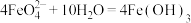 (胶体)
(胶体)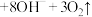 ,当反应转移的电子数为
,当反应转移的电子数为 时,生成标准状态下O2的体积约为
时,生成标准状态下O2的体积约为__________ 。
(1)上述杀菌消毒剂属于电解质的是
(2)“84”消毒液可由Cl2和NaOH溶液反应制得,若与“洁厕灵”(盐酸是成分之一)混合使用会产生黄绿色有毒气体,原因是
(3)H2O2是一种绿色环保型消毒剂,其结构式为
(4)O3是一种强氧化剂,具有强大的杀菌能力。O3与O2的关系是互为
(5)高铁酸钠(Na2FeO4)是一种多功能新型净水剂。工业上可在NaOH溶液中,用NaClO氧化Fe(OH)3的方法制备Na2FeO4,其离子方程式为
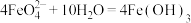 (胶体)
(胶体)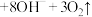 ,当反应转移的电子数为
,当反应转移的电子数为 时,生成标准状态下O2的体积约为
时,生成标准状态下O2的体积约为
您最近一年使用:0次
10 . 将盛12mL一氧化氮和36mL二氧化氮混合气体的烧瓶倒置于水中,通入一定量的氧气,完全反应后,剩余气体体积为4mL,且该气体支持燃烧,则充入的氧气的体积为
| A.15mL | B.18mL | C.20mL | D.22mL |
您最近一年使用:0次



