解题方法
1 . 水热法制备 的流程如图,下列叙述正确的是
的流程如图,下列叙述正确的是
 的流程如图,下列叙述正确的是
的流程如图,下列叙述正确的是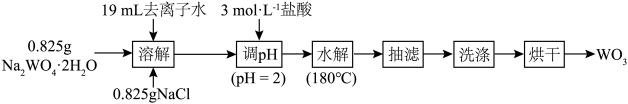
| A.本实验使用托盘天平称量 | B. 作反应的氧化剂 作反应的氧化剂 |
C.调 为2的目的是促进反应完全 为2的目的是促进反应完全 | D.用 溶液检验产品是否洗净 溶液检验产品是否洗净 |
您最近半年使用:0次
解题方法
2 . 一种催化还原NO的机理如图所示,下列说法正确的是
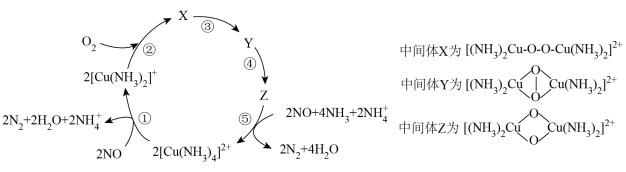

| A.中间体X和Z中O和Cu的化合价均不变 |
B.使用催化剂 ,可以提高NO的反应速率和平衡转化率 ,可以提高NO的反应速率和平衡转化率 |
| C.过程①中既有极性键的断裂,也有极性键的形成 |
D.该催化还原过程的总反应方程式为 |
您最近半年使用:0次
今日更新
|
3次组卷
|
2卷引用:2024届新疆维吾尔自治区高三下学期三模考试理综试题-高中化学
解题方法
3 . 化学是现代生产、生活与科技的中心学科之一,下列说法正确的是
| A.中国天眼FAST用到的碳化硅及制作宇航服常用的聚四氟乙烯都属于有机高分子材料 |
| B.“蛟龙”号载人潜水器最关键的部件—耐压球壳是用稀土金属钛(第ⅣB族)制造而成 |
| C.2023年诺贝尔化学奖授予了“发现和合成量子点(纳米级粒子)”的三位科学家,量子点形成分散系后可能具有丁达尔效应 |
| D.超分子内部分子之间通过共价键结合 |
您最近半年使用:0次
今日更新
|
0次组卷
|
2卷引用:2024届新疆维吾尔自治区高三下学期三模考试理综试题-高中化学
4 . 稍过量零价铁与亚硫酸钠体系能有效降解废水中有机污染物活性红。
已知:
ⅰ.体系中产生的 、
、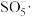 和
和 可将活性红氧化,其中
可将活性红氧化,其中 具有强氧化性
具有强氧化性
ⅱ.

ⅲ. 开始沉淀时pH=6.3,完全沉淀时pH=8.3
开始沉淀时pH=6.3,完全沉淀时pH=8.3
 开始沉淀时pH=1.5,完全沉淀时pH=2.8
开始沉淀时pH=1.5,完全沉淀时pH=2.8 体系中各含硫粒子的物质的量分数与pH的关系
体系中各含硫粒子的物质的量分数与pH的关系
下列说法不正确 的是
已知:
ⅰ.体系中产生的
 、
、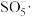 和
和 可将活性红氧化,其中
可将活性红氧化,其中 具有强氧化性
具有强氧化性ⅱ.


ⅲ.
 开始沉淀时pH=6.3,完全沉淀时pH=8.3
开始沉淀时pH=6.3,完全沉淀时pH=8.3 开始沉淀时pH=1.5,完全沉淀时pH=2.8
开始沉淀时pH=1.5,完全沉淀时pH=2.8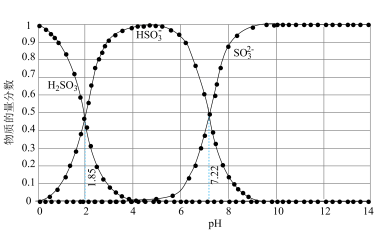
 体系中各含硫粒子的物质的量分数与pH的关系
体系中各含硫粒子的物质的量分数与pH的关系 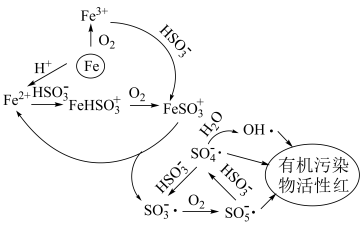
下列说法
A.由图1,25℃时 的 的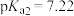 |
| B.pH=4时较pH=8时具有更好的降解效果 |
C.反应一段时间后零价铁表面产生 ,投入 ,投入 可消除 可消除 |
| D.用等物质的量的硫酸亚铁代替零价铁可提高有机物的降解率 |
您最近半年使用:0次
解题方法
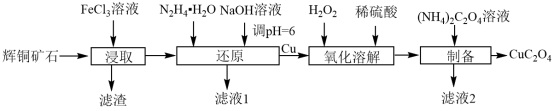
5 . 以辉铜矿(主要成分为Cu2S,含少量SiO2)为原料制备草酸铜(CuC2O4)的流程如图所示:
(1)滤渣中含有单质S和___________ (填化学式),写出“浸取”时反应的化学方程式:___________ 。
(2)“还原”时除生成Cu外,还有N2生成,写出该反应的离子方程式:___________ 。
(3)“氧化溶解”时,也可以直接用稀硝酸溶解Cu,但没有采用此法,考虑的主要原因是___________ 。
(4)向滤液1中加入(或通入)___________(填字母),可得到一种可循环利用的物质。
(5)“制备”时 过多会导致
过多会导致 与
与 生成环状结构的配离子
生成环状结构的配离子 ,该配离子的结构式为
,该配离子的结构式为___________ (不考虑立体异构)。
(6)将一定质量的CuC2O4置于Ar气中热解,测得剩余固体的质量与原始固体的质量的比值随温度变化的曲线如图1所示。350~400℃下剩余固体的化学式为___________ 。 为
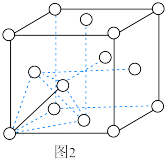
为___________  (已知该晶胞的晶胞参数为anm,阿伏加德罗常数的值为
(已知该晶胞的晶胞参数为anm,阿伏加德罗常数的值为 )。
)。
(1)滤渣中含有单质S和
(2)“还原”时除生成Cu外,还有N2生成,写出该反应的离子方程式:
(3)“氧化溶解”时,也可以直接用稀硝酸溶解Cu,但没有采用此法,考虑的主要原因是
(4)向滤液1中加入(或通入)___________(填字母),可得到一种可循环利用的物质。
| A.铁 | B.氯气 | C.高锰酸钾 | D.氯化氢 |
 过多会导致
过多会导致 与
与 生成环状结构的配离子
生成环状结构的配离子 ,该配离子的结构式为
,该配离子的结构式为(6)将一定质量的CuC2O4置于Ar气中热解,测得剩余固体的质量与原始固体的质量的比值随温度变化的曲线如图1所示。350~400℃下剩余固体的化学式为
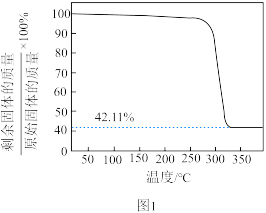
 为
为 (已知该晶胞的晶胞参数为anm,阿伏加德罗常数的值为
(已知该晶胞的晶胞参数为anm,阿伏加德罗常数的值为 )。
)。
您最近半年使用:0次
名校
解题方法
6 . 新能源汽车工业飞速发展依赖于锂离子电池的新型电极材料的研究取得的重大成果。 可以实现海水中
可以实现海水中 的富集,对锂离子电池的研究作出重要贡献。以软锰矿(含
的富集,对锂离子电池的研究作出重要贡献。以软锰矿(含 及少量
及少量 和
和 )为原料生产高纯
)为原料生产高纯 的工艺流程如图甲。
的工艺流程如图甲。
(1)“浸锰”时, 生成
生成 的离子方程式为
的离子方程式为___________ 。
(2)步骤Ⅱ中, 的萃取率与
的萃取率与 的关系如图乙,当
的关系如图乙,当 后,随
后,随 增大,
增大, 萃取率下降的原因是
萃取率下降的原因是___________ 。 ,若
,若 ,常温下调节
,常温下调节 范围应为
范围应为___________ {已知该条件下,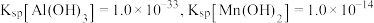 }。
}。
(4)海水中锂的总含量为陆地总含量的5000倍以上,但海水中锂的质量浓度仅为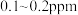 ,从海水中提取锂首先需要对低浓度的
,从海水中提取锂首先需要对低浓度的 进行选择性富集,而
进行选择性富集,而 能够嵌入高纯
能够嵌入高纯 并在一定条件下脱出,据此可以进行
并在一定条件下脱出,据此可以进行 的富集。
的富集。
①以 和高纯
和高纯 为原料,充分混合后在720℃下煅烧
为原料,充分混合后在720℃下煅烧 ,冷却至室温后即可得到复合氧化物
,冷却至室温后即可得到复合氧化物 。用
。用 的盐酸在60℃下处理
的盐酸在60℃下处理 ,将其中所有
,将其中所有 置换后得到
置换后得到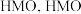 可以和
可以和 反应再生成
反应再生成 ,然后
,然后 与酸作用脱出
与酸作用脱出 从而实现
从而实现 的富集。如此循环处理。合成
的富集。如此循环处理。合成 的化学方程式为
的化学方程式为___________ ;
②用酸处理 时,除离子交换反应之外,也会发生一个副反应,该副反应导致固体中M的平均化合价有所提高,则副反应的生成物中含
时,除离子交换反应之外,也会发生一个副反应,该副反应导致固体中M的平均化合价有所提高,则副反应的生成物中含 元素的微粒是
元素的微粒是___________ 。这一副反应对再生后的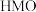 的锂富集性能的影响是
的锂富集性能的影响是___________ 。
(5)利用高纯 实施电化学富集锂是行之有效的方法。电化学系统(如图丙所示)的工作步骤如下:
实施电化学富集锂是行之有效的方法。电化学系统(如图丙所示)的工作步骤如下:
步骤1:向 所在的腔室通入海水,启动电源1,使海水中的
所在的腔室通入海水,启动电源1,使海水中的 进入
进入 结构而形成
结构而形成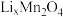 ;
;
步骤2:关闭电源1和海水通道,启动电源2,同时向电极2上通入空气,使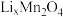 中的
中的 脱出进入腔室2。
脱出进入腔室2。 对
对 的富集效果,将
的富集效果,将 的
的 溶液通入
溶液通入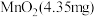 所在腔室,启动电源1,使电流恒定在
所在腔室,启动电源1,使电流恒定在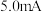 ,累计工作
,累计工作 后发现
后发现 的电极电势快速下降,则
的电极电势快速下降,则 中的
中的
___________ (已知 电子的电量为
电子的电量为 。电流效率为
。电流效率为 )。
)。
②电源2工作时, 电极上发生的电极反应为
电极上发生的电极反应为___________ 。
 可以实现海水中
可以实现海水中 的富集,对锂离子电池的研究作出重要贡献。以软锰矿(含
的富集,对锂离子电池的研究作出重要贡献。以软锰矿(含 及少量
及少量 和
和 )为原料生产高纯
)为原料生产高纯 的工艺流程如图甲。
的工艺流程如图甲。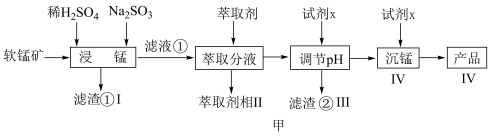
(1)“浸锰”时,
 生成
生成 的离子方程式为
的离子方程式为(2)步骤Ⅱ中,
 的萃取率与
的萃取率与 的关系如图乙,当
的关系如图乙,当 后,随
后,随 增大,
增大, 萃取率下降的原因是
萃取率下降的原因是
 ,若
,若 ,常温下调节
,常温下调节 范围应为
范围应为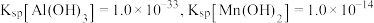 }。
}。(4)海水中锂的总含量为陆地总含量的5000倍以上,但海水中锂的质量浓度仅为
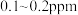 ,从海水中提取锂首先需要对低浓度的
,从海水中提取锂首先需要对低浓度的 进行选择性富集,而
进行选择性富集,而 能够嵌入高纯
能够嵌入高纯 并在一定条件下脱出,据此可以进行
并在一定条件下脱出,据此可以进行 的富集。
的富集。①以
 和高纯
和高纯 为原料,充分混合后在720℃下煅烧
为原料,充分混合后在720℃下煅烧 ,冷却至室温后即可得到复合氧化物
,冷却至室温后即可得到复合氧化物 。用
。用 的盐酸在60℃下处理
的盐酸在60℃下处理 ,将其中所有
,将其中所有 置换后得到
置换后得到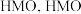 可以和
可以和 反应再生成
反应再生成 ,然后
,然后 与酸作用脱出
与酸作用脱出 从而实现
从而实现 的富集。如此循环处理。合成
的富集。如此循环处理。合成 的化学方程式为
的化学方程式为②用酸处理
 时,除离子交换反应之外,也会发生一个副反应,该副反应导致固体中M的平均化合价有所提高,则副反应的生成物中含
时,除离子交换反应之外,也会发生一个副反应,该副反应导致固体中M的平均化合价有所提高,则副反应的生成物中含 元素的微粒是
元素的微粒是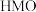 的锂富集性能的影响是
的锂富集性能的影响是(5)利用高纯
 实施电化学富集锂是行之有效的方法。电化学系统(如图丙所示)的工作步骤如下:
实施电化学富集锂是行之有效的方法。电化学系统(如图丙所示)的工作步骤如下:步骤1:向
 所在的腔室通入海水,启动电源1,使海水中的
所在的腔室通入海水,启动电源1,使海水中的 进入
进入 结构而形成
结构而形成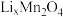 ;
;步骤2:关闭电源1和海水通道,启动电源2,同时向电极2上通入空气,使
 中的
中的 脱出进入腔室2。
脱出进入腔室2。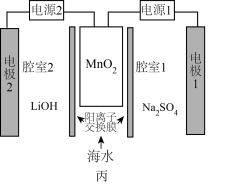
 对
对 的富集效果,将
的富集效果,将 的
的 溶液通入
溶液通入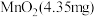 所在腔室,启动电源1,使电流恒定在
所在腔室,启动电源1,使电流恒定在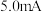 ,累计工作
,累计工作 后发现
后发现 的电极电势快速下降,则
的电极电势快速下降,则 中的
中的
 电子的电量为
电子的电量为 。电流效率为
。电流效率为 )。
)。②电源2工作时,
 电极上发生的电极反应为
电极上发生的电极反应为
您最近半年使用:0次
7 . 亚氯酸钠( )具有强氧化性、受热易分解,可用作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示.已知高浓度的
)具有强氧化性、受热易分解,可用作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示.已知高浓度的 易爆炸.下列说法错误的是
易爆炸.下列说法错误的是
 )具有强氧化性、受热易分解,可用作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示.已知高浓度的
)具有强氧化性、受热易分解,可用作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示.已知高浓度的 易爆炸.下列说法错误的是
易爆炸.下列说法错误的是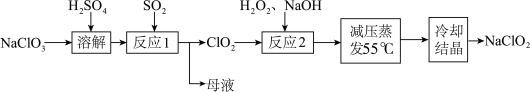
A.“反应1”中 是还原产物,母液中主要成分是 是还原产物,母液中主要成分是 |
B.“反应1”需要通入 稀释 稀释 ,以防发生爆炸 ,以防发生爆炸 |
C.“反应2”中,氧化剂和还原剂的物质的量之比为 |
D.若还原产物均为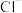 时, 时, 的氧化能力是等质量 的氧化能力是等质量 的2.5倍 的2.5倍 |
您最近半年使用:0次
8 . 下述装置或操作能实现相应实验目的的是
| 装置或操作 |
|
|
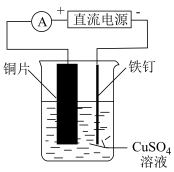
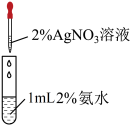
| 实验目的 | 铁钉表面镀铜 | 配制银氨溶液 |
| 选项 | A | B |
| 装置或操作 |
|
|
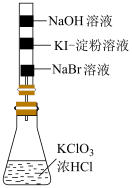
| 实验目的 | 验证氧化性:Cl2>Br2>I2 | 检验1-溴丙烷的消去反应产物丙烯 |
| 选项 | C | D |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 . NA为阿伏加德罗常数的值,下列说法正确的是
A.4.4g C2H4O中含有 键的数目为0.6NA 键的数目为0.6NA |
| B.3molNO2与H2O完全反应时转移电子的数目为4NA |
| C.常温下,1LpH=6.5的H2O2溶液中由水电离产生H+的数目为10-7.5NA |
D.常温下,1L0.1mol/LK2Cr2O7溶液中 的数目为0.1NA 的数目为0.1NA |
您最近半年使用:0次
解题方法
10 . 下列物质的用途或性质与解释对应关系错误的是
选项 | 用途或性质 | 解释 |
A | 钠钾合金用作核反应堆的传热介质 | 钠、钾均为活泼金属,金属性强 |
B |
|
|
C | 钢瓶可用于储存液氯 | 常温下,铁与液氯不反应 |
D | 聚乙炔具有导电性 | 聚乙炔结构中存在共轭大 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次

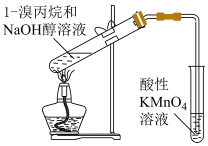
 能使酸性高锰酸钾溶液褪色
能使酸性高锰酸钾溶液褪色 键
键

