名校
解题方法
1 . 如图为元素周期表的一部分,请根据元素①~⑧在表中的位置,回答下列问题:

(1)请写出元素⑦在元素周期表中的位置
(2)由元素⑤形成的化合物Na3N遇水反应生成氨气(NH3)和一种强碱,该反应的化学方程式为
(3)③、④、⑤、⑥的简单离子半径由大到小的顺序是
(4)由表中元素形成的常见无机化合物A、B、C、X有以下转化关系:

若A、B、C含同一金属元素,X为氢氧化钠,所有反应都在溶液中进行。反应①的离子方程式为
您最近一年使用:0次
解题方法
2 . X、Y、Z、M为原子序数依次增大的短周期主族元素,这四种元素原子的最外层电子数之和等于12。A~G是由上述四种元素组成的化合物,其转化关系如图所示,其中C是一种强碱,焰色试验呈黄色。

回答下列问题:
(1)元素Y在元素周期表中的位置是___________ 。
(2)Y、Z、M三种元素的原子半径由大到小的顺序为___________ (用元素符号表示)。
(3)能说明Z的非金属性强于Y的依据是___________ (写一点即可)。
(4)写出反应①的离子方程式___________ 。
(5)去除A溶液中混有的少量B的方法是___________ 。
(6)3.9g固体D与足量F反应转移的电子数目为___________ 。
(7)下列实验方案中,能测定出物质A和B的混合物中B的质量分数的是___________ (填标号)。
a.取mg混合物充分加热,质量减少ng
b.取mg混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到ng固体
c.取mg混合物与足量NaOH溶液充分反应,得到ng溶液
d.取mg混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加ng

回答下列问题:
(1)元素Y在元素周期表中的位置是
(2)Y、Z、M三种元素的原子半径由大到小的顺序为
(3)能说明Z的非金属性强于Y的依据是
(4)写出反应①的离子方程式
(5)去除A溶液中混有的少量B的方法是
(6)3.9g固体D与足量F反应转移的电子数目为
(7)下列实验方案中,能测定出物质A和B的混合物中B的质量分数的是
a.取mg混合物充分加热,质量减少ng
b.取mg混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到ng固体
c.取mg混合物与足量NaOH溶液充分反应,得到ng溶液
d.取mg混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加ng
您最近一年使用:0次
名校
3 . A、B、C、D、E、F、G为中学化学常见物质,它们之间有如图转化关系(反应条件已略去)。已知:A、C、D、E均含有同种非金属元素M,A为气态氢化物;G是一种紫红色的金属单质;B是空气的组成成分,在空气中占比约为21%。根据学知识,按要求回答下列问题:

Ⅰ.若A具有臭鸡蛋气味,且能与C反应生成一种淡黄色非金属单质,反应①为非氧化还原反应,反应②为E的浓溶液与G反应,则:
(1)M元素在元素周期表中的位置为_______ 。
(2)写出反应②的化学方程式:_______ ,该反应中体现了E的浓溶液的强氧化性和_______ 性。
(3)将C通入足量溴水中,发生反应的离子方程式为_______ ;将C通入少量品红溶液中可观察到的现象为_______ 。
Ⅱ.若光照条件下,E的浓溶液易分解得到B、D、F3种物质;大量排放汽车尾气中的C、D会导致光化学烟雾,已知:反应②为E的稀溶液与G反应。
(4)写出A+B→C+F的化学方程式:_______ 。
(5)常温下,将60mL C、D的混合气体与30mL B同时通入水中,充分反应后,剩余7.5mL气体,则60mL混合气体中C的体积分数可能为_______ (填标号)。
①15.00% ②25.00% ③41.25% ④68.75%

Ⅰ.若A具有臭鸡蛋气味,且能与C反应生成一种淡黄色非金属单质,反应①为非氧化还原反应,反应②为E的浓溶液与G反应,则:
(1)M元素在元素周期表中的位置为
(2)写出反应②的化学方程式:
(3)将C通入足量溴水中,发生反应的离子方程式为
Ⅱ.若光照条件下,E的浓溶液易分解得到B、D、F3种物质;大量排放汽车尾气中的C、D会导致光化学烟雾,已知:反应②为E的稀溶液与G反应。
(4)写出A+B→C+F的化学方程式:
(5)常温下,将60mL C、D的混合气体与30mL B同时通入水中,充分反应后,剩余7.5mL气体,则60mL混合气体中C的体积分数可能为
①15.00% ②25.00% ③41.25% ④68.75%
您最近一年使用:0次
2022-05-20更新
|
574次组卷
|
3卷引用:河南省安阳市2021-2022学年高一下学期阶段性考试(四)化学试题
河南省安阳市2021-2022学年高一下学期阶段性考试(四)化学试题河南省许平汝漯2021-2022学年高一下学期5月大联考化学试题(已下线)第15练 实验综合题与无机综合题-2022年【暑假分层作业】高一化学(人教版2019必修第二册)
4 . B、D、C、A、E五种元素的原子序数顺序依次增大,其中只有E为金属元素,D、C元素在元素周期表中位置相邻,在一定条件下,B的单质可以分别和A、C、D的单质化合生成甲、乙、丙化合物,C的单质和D的单质化合可得丁,戊、己、庚均为化合物。已知乙、丙每个分子中均含有10个电子,如图为相互转化关系:
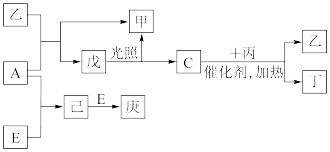
请回答下列问题:
(1)写出C、D氢化物的稳定性由强到弱的顺序_______ (用化学式表示)。
(2) A、B、D三种元素形成的化合物中其中一种可用作化肥,写该化合物的电子式_______ 。
(3)写出C与丙反应的化学反应方程式_______ 。
(4)写出工业上冶炼金属E的主要化学方程式:_______ 。
(5)工业上通过如下转化可制得含A元素的钾盐KAO3晶体:
NaA溶液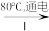 NaAO3
NaAO3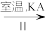 KAO3晶体
KAO3晶体
①完成Ⅰ中反应的总化学方程式:_______NaA+_______H2O _______NaAO3+_______。
_______NaAO3+_______。_______
②Ⅱ中反应过程能析出KClO3晶体而无其他晶体析出的原因是_______ 。

请回答下列问题:
(1)写出C、D氢化物的稳定性由强到弱的顺序
(2) A、B、D三种元素形成的化合物中其中一种可用作化肥,写该化合物的电子式
(3)写出C与丙反应的化学反应方程式
(4)写出工业上冶炼金属E的主要化学方程式:
(5)工业上通过如下转化可制得含A元素的钾盐KAO3晶体:
NaA溶液
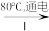 NaAO3
NaAO3 KAO3晶体
KAO3晶体①完成Ⅰ中反应的总化学方程式:_______NaA+_______H2O
 _______NaAO3+_______。
_______NaAO3+_______。②Ⅱ中反应过程能析出KClO3晶体而无其他晶体析出的原因是
您最近一年使用:0次
5 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题。
(1)表中某元素最高价氧化物的水化物与其氢化物之间能相互反应生成离子化合物,则该离子化合物的名称是____ ,由元素④、⑥、⑦、⑧形成的简单离子的半径由大到小的顺序是____ (用离子符号表示)。②、④元素的最简单氢化物的沸点由高到低的顺序是____ 。(用化学式表示)
(2)分别由上述两种元素组成、均为10e-的阴、阳离子,在加热条件下反应生成两种10e-的分子,写出该反应的离子方程式____ 。
(3)元素周期表中氧化性最强的元素是____ (写元素符号),该元素的单质和水反应的化学方程式为___ 。
(4)以上元素组成的物质有下列框图中的转化关系,其中f为⑥的单质,甲为10电子微粒,h是⑨的单质。
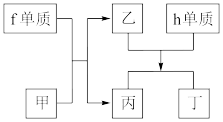
①丁属于___ (选填“离子化合物”或“共价化合物”)。
②请写出h单质与乙反应的化学方程式____ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | Ⅶ | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑨ | ⑧ | ||||
(2)分别由上述两种元素组成、均为10e-的阴、阳离子,在加热条件下反应生成两种10e-的分子,写出该反应的离子方程式
(3)元素周期表中氧化性最强的元素是
(4)以上元素组成的物质有下列框图中的转化关系,其中f为⑥的单质,甲为10电子微粒,h是⑨的单质。

①丁属于
②请写出h单质与乙反应的化学方程式
您最近一年使用:0次
解题方法
6 . X、Y、Z为短周期主族元素,且原子序数依次增大,Y、Z位于相邻主族,这三种元素形成的化合物甲为 ,化合物甲受热分解产生的物质及后续有关物质的转化关系如下图所示:
,化合物甲受热分解产生的物质及后续有关物质的转化关系如下图所示:
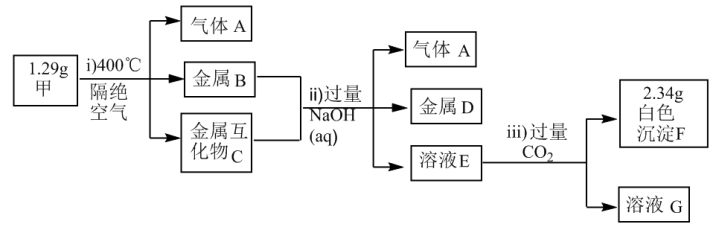
已知:金属互化物是由两种或两种以上的金属组成,其组成金属具有单质的性质。
回答下列问题:
(1)Y在元素周期表中的位置是___________ 。
(2)F受热分解生成两性氧化物,则F与烧碱溶液反应的离子方程式是___________ 。
(3)若溶液G中只有一种溶质,则该溶液中阴离子的浓度由大到小的顺序是___________ 。
(4)1.29g甲在隔绝空气的条件下,加热到400℃,完全分解产生的气体A的体积(标准状况)为___________ L。
 ,化合物甲受热分解产生的物质及后续有关物质的转化关系如下图所示:
,化合物甲受热分解产生的物质及后续有关物质的转化关系如下图所示:
已知:金属互化物是由两种或两种以上的金属组成,其组成金属具有单质的性质。
回答下列问题:
(1)Y在元素周期表中的位置是
(2)F受热分解生成两性氧化物,则F与烧碱溶液反应的离子方程式是
(3)若溶液G中只有一种溶质,则该溶液中阴离子的浓度由大到小的顺序是
(4)1.29g甲在隔绝空气的条件下,加热到400℃,完全分解产生的气体A的体积(标准状况)为
您最近一年使用:0次
名校
解题方法
7 . A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
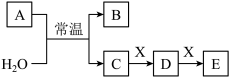
(1)若A为常见的金属单质,焰色试验呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:__ 。证明D已经氧化变质的方法是:取少量D固体溶于水中,__ 。
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强。该元素在元素周期表中的位置为__ ,则X可能为__ (填代号)。
a.NaHCO3 b.Na2CO3 c.Fe(OH)3 d.NaAlO2
(3)若A为淡黄色粉末,则A的电子式为__ 。若X为一种最常见的造成温室效应的气体。若鉴别等浓度的D、E两种溶液,可选择的试剂为__ (填代号)。
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为__ ,E是__ (填化学式)。

(1)若A为常见的金属单质,焰色试验呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强。该元素在元素周期表中的位置为
a.NaHCO3 b.Na2CO3 c.Fe(OH)3 d.NaAlO2
(3)若A为淡黄色粉末,则A的电子式为
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为
您最近一年使用:0次
解题方法
8 . X、Y、Z、W 是原子序数依次增大的短周期元素,Y 和W同主族,且X、Z原子序数之和是Y、W原子序数之和的 。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
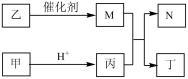
(1)W在元素周期表中的位置是_______________________ 。
(2)Y、Z、W的离子半径由大到小的顺序为__________ (用元素符号表示)。
(3)写出乙的电子式_____________ ,M 的结构式_____________________ 。
(4)丁与H2S相比沸点高的是_______ (用化学式表示);原因是_______________ 。
(5)N 与乙烯均能使酸性 KMnO4溶液褪色,原理______________ (填“相同”或“不相同”);N使酸性KMnO4溶液褪色的离子方程式为 ________________________ 。
 。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
(1)W在元素周期表中的位置是
(2)Y、Z、W的离子半径由大到小的顺序为
(3)写出乙的电子式
(4)丁与H2S相比沸点高的是
(5)N 与乙烯均能使酸性 KMnO4溶液褪色,原理
您最近一年使用:0次
名校
解题方法
9 . A、B、C、D、E、F、G均为常见短周期元素,原子序数依次递增。已知A、B、C能分别与D 组成二元化合物K、L、M,甲、乙分别是B、D的单质,常温下分别是常见的固体和气体,化合物M是产生光化学烟雾的主要气体之一,丙是C的最高价氧化物对应的水化物,它们之间有如图所示转化关系。E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的主族元素。请回答下列问题:
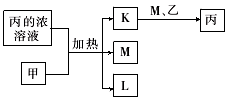
(1)C在元素周期表中的位置为_________ 。
(2)甲与丙的浓溶液反应的化学方程式_______________ 。
(3)D与E按原子个数比1:1形成化合物的电子式为________ ,其与水发生反应的化学方程式是_______________ 。
(4)E、F、G形成的简单离子,半径由大到小顺序是________ (用离子符号表示)。B、F、G元素的非金属性由强到弱的顺序__________ (用元素符号表示)。

(1)C在元素周期表中的位置为
(2)甲与丙的浓溶液反应的化学方程式
(3)D与E按原子个数比1:1形成化合物的电子式为
(4)E、F、G形成的简单离子,半径由大到小顺序是
您最近一年使用:0次
2018-07-16更新
|
244次组卷
|
5卷引用:河南省漯河市临颍县南街高级中学2019-2020学年高一下学期期末考试化学试题
名校
解题方法
10 . I. 短周期元素X、Y、Z、W在周期表中的相对位置如图所示,其中W元素的原子结构示意图为 。
。
请回答下列问题:
(1)Z元素在元素周期表中的位置是__________________________________ 。
(2)X、Y、Z三种元素的原子半径由大到小的顺序为_________ (元素符号表示)。
(3)X、Z、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为________ (用化学式表示)。
(4)用电子式表示WY2的形成过程__________________________________ 。
(5)写出W单质与浓硫酸反应的化学方程式_____________________________ 。
Ⅱ. A、B、C三种物质存在如图转化关系。
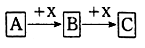
(6)若B为白色胶状不溶物,则A与C反应的离子方程式为_______________ 。
 。
。| W | X | Y |
| Z |
(1)Z元素在元素周期表中的位置是
(2)X、Y、Z三种元素的原子半径由大到小的顺序为
(3)X、Z、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为
(4)用电子式表示WY2的形成过程
(5)写出W单质与浓硫酸反应的化学方程式
Ⅱ. A、B、C三种物质存在如图转化关系。
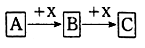
(6)若B为白色胶状不溶物,则A与C反应的离子方程式为
您最近一年使用:0次



