名校
解题方法
1 . 抗新冠新药的合成
有机化合物G是一种抗新型冠状病毒口服药的合成中间体,其合成路线如下,

(1)A的系统命名为_____ ;G分子中至少有_____ 个原子共面。
(2)C→D的反应方程式为_____ 。
(3)D→E中新生成的官能团名称是_____ ;E→F的反应类型是_____ 。
(4)检验G中是否有少量F残留的操作是_____ 。
(5)写出一种同时满足下列条件的E的同分异构体的结构简式。_____
ⅰ、分子中含有苯环
ⅱ、属于酯类化合物,能发生银镜反应
ⅲ、分子中含有2种化学环境不同的氢原子
(6)化合物E的Ka为1.35×10-3,而苯甲酸(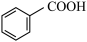 )的Ka为6.46×10-5,从结构角度解释两者Ka存在较大差异的原因
)的Ka为6.46×10-5,从结构角度解释两者Ka存在较大差异的原因_____ 。
(7)设计以D为原料合成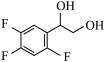 的路线
的路线_____ 。
有机化合物G是一种抗新型冠状病毒口服药的合成中间体,其合成路线如下,

(1)A的系统命名为
(2)C→D的反应方程式为
(3)D→E中新生成的官能团名称是
(4)检验G中是否有少量F残留的操作是
(5)写出一种同时满足下列条件的E的同分异构体的结构简式。
ⅰ、分子中含有苯环
ⅱ、属于酯类化合物,能发生银镜反应
ⅲ、分子中含有2种化学环境不同的氢原子
(6)化合物E的Ka为1.35×10-3,而苯甲酸(
 )的Ka为6.46×10-5,从结构角度解释两者Ka存在较大差异的原因
)的Ka为6.46×10-5,从结构角度解释两者Ka存在较大差异的原因(7)设计以D为原料合成
 的路线
的路线
您最近一年使用:0次
名校
2 . 某研究性学习小组为合成 查阅资料得知一条合成路线:
查阅资料得知一条合成路线:
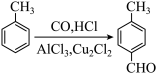
原料气CO的制备原理:HCOOH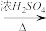 CO↑+H2O,并设计出原料气的制备装置(如图)。
CO↑+H2O,并设计出原料气的制备装置(如图)。
(提示:甲酸(HCOOH)通常是一种无色易挥发的液体,它在浓硫酸作用下易分解)
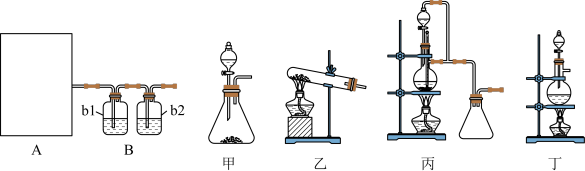
请完成下列问题:
(1)图A是利用甲酸制取CO的发生装置.根据实验原理,应选择图_____ (填“甲”、“乙”、“丙”或“丁”);选择的理由是______________________ 。
(2)若用以上装置制备干燥纯净的CO,b1和b2中盛装的试剂分别是____________ ,_____ 。
(3)CO还可以和丙烯和氢气制取正丁醇,方程式如下:
CH3CH=CH2+CO+H2 CH3CH2CH2CHO
CH3CH2CH2CHO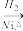 CH3CH2CH2CH2OH;
CH3CH2CH2CH2OH;
在制取原料丙烯时,会产生少量SO2、CO2及水蒸气,某小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是_______ (填序号)。
①2%品红溶液 ②溴水 ③石灰水 ④无水CuSO4 ⑤饱和Na2SO3溶液
(4)产物 中往往会混有少量甲苯,为了制取较纯净的产物,该小组对这两种有机物的物理性质进行了查阅,资料如下:
中往往会混有少量甲苯,为了制取较纯净的产物,该小组对这两种有机物的物理性质进行了查阅,资料如下:
甲苯是无色透明液体,密度0.87,沸点:110.6℃,不溶于水,可混溶于苯等多数有机溶剂。无色或淡黄色透明液体,密度1.015,沸点204-205℃,微溶于水,易溶于醇、醚。通过这些资料,该小组设计了某些方法来进行产物的提纯,合理的是_________ 。
A 分液 B过滤 C蒸馏 D将甲苯氧化成苯甲酸再进行分液
(5)得到较纯净的产物之后,某位同学为了研究产物的化学性质,将产物和甲苯分别取样,并分别滴加溴水,发现溴水最终都褪色了,于是得出结论:产物和甲苯的化学性质相似。这位同学的结论是否正确?若不正确,请说明理由。_____ 。
 查阅资料得知一条合成路线:
查阅资料得知一条合成路线:
原料气CO的制备原理:HCOOH
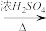 CO↑+H2O,并设计出原料气的制备装置(如图)。
CO↑+H2O,并设计出原料气的制备装置(如图)。(提示:甲酸(HCOOH)通常是一种无色易挥发的液体,它在浓硫酸作用下易分解)

请完成下列问题:
(1)图A是利用甲酸制取CO的发生装置.根据实验原理,应选择图
(2)若用以上装置制备干燥纯净的CO,b1和b2中盛装的试剂分别是
(3)CO还可以和丙烯和氢气制取正丁醇,方程式如下:
CH3CH=CH2+CO+H2
 CH3CH2CH2CHO
CH3CH2CH2CHO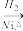 CH3CH2CH2CH2OH;
CH3CH2CH2CH2OH;在制取原料丙烯时,会产生少量SO2、CO2及水蒸气,某小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是
①2%品红溶液 ②溴水 ③石灰水 ④无水CuSO4 ⑤饱和Na2SO3溶液
(4)产物
 中往往会混有少量甲苯,为了制取较纯净的产物,该小组对这两种有机物的物理性质进行了查阅,资料如下:
中往往会混有少量甲苯,为了制取较纯净的产物,该小组对这两种有机物的物理性质进行了查阅,资料如下: 甲苯是无色透明液体,密度0.87,沸点:110.6℃,不溶于水,可混溶于苯等多数有机溶剂。无色或淡黄色透明液体,密度1.015,沸点204-205℃,微溶于水,易溶于醇、醚。通过这些资料,该小组设计了某些方法来进行产物的提纯,合理的是
A 分液 B过滤 C蒸馏 D将甲苯氧化成苯甲酸再进行分液
(5)得到较纯净的产物之后,某位同学为了研究产物的化学性质,将产物和甲苯分别取样,并分别滴加溴水,发现溴水最终都褪色了,于是得出结论:产物和甲苯的化学性质相似。这位同学的结论是否正确?若不正确,请说明理由。
您最近一年使用:0次
2020-03-22更新
|
89次组卷
|
2卷引用:上海市奉贤区2015届高三上学期期中调研测试化学试题
名校
解题方法
3 . 苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一、下面是它的一种实验室合成路线:
 +H2O+H2SO4
+H2O+H2SO4
 +NH4HSO4
+NH4HSO4
 +Cu(OH)2
+Cu(OH)2
 (苯乙酸铜)+ H2O
(苯乙酸铜)+ H2O
制备苯乙酸的装置示意图(加热和夹持装置等略)如下:

已知:苯乙酸( )的熔点为
)的熔点为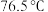 ,微溶于冷水,溶于乙醇。
,微溶于冷水,溶于乙醇。
具体步骤:
ⅰ.在 三颈烧瓶a中加入
三颈烧瓶a中加入 的硫酸。
的硫酸。
ⅱ.将a中的溶液加热至 ,缓缓滴加
,缓缓滴加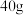 苯乙腈(
苯乙腈( )到过量硫酸溶液中,然后升温至
)到过量硫酸溶液中,然后升温至 继续反应。反应结束后加适量冷水,再分离出苯乙酸粗品。
继续反应。反应结束后加适量冷水,再分离出苯乙酸粗品。
ⅲ.将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入 搅拌
搅拌 ,过滤,滤液静置一段时间,析出苯乙酸铜晶体。回答下列问题:
,过滤,滤液静置一段时间,析出苯乙酸铜晶体。回答下列问题:
(1)配制70%硫酸时,加入蒸馏水与浓硫酸的先后顺序是:先加___________ ,后加___________ 。
(2)在装置中,仪器b的名称是___________。
(3)仪器c的作用是_________ ;反应分离苯乙酸粗品时,加适量冷水的目的是_______ 。
(4)下列仪器中可用于分离苯乙酸粗品,除漏斗外,还有___________。
(5)写出用 和
和 溶液制备
溶液制备 沉淀的化学方程式
沉淀的化学方程式___________ 。
(6)最终得到 苯乙酸晶体,则苯乙酸的产率是
苯乙酸晶体,则苯乙酸的产率是___________ 。(写出计算过程,结果用百分数表示,保留小数点后两位数字)
(7)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置电解 溶液,该电池的负极反应式为
溶液,该电池的负极反应式为___________ 。

 +H2O+H2SO4
+H2O+H2SO4
 +NH4HSO4
+NH4HSO4 +Cu(OH)2
+Cu(OH)2
 (苯乙酸铜)+ H2O
(苯乙酸铜)+ H2O制备苯乙酸的装置示意图(加热和夹持装置等略)如下:

已知:苯乙酸(
 )的熔点为
)的熔点为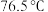 ,微溶于冷水,溶于乙醇。
,微溶于冷水,溶于乙醇。具体步骤:
ⅰ.在
 三颈烧瓶a中加入
三颈烧瓶a中加入 的硫酸。
的硫酸。ⅱ.将a中的溶液加热至
 ,缓缓滴加
,缓缓滴加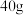 苯乙腈(
苯乙腈( )到过量硫酸溶液中,然后升温至
)到过量硫酸溶液中,然后升温至 继续反应。反应结束后加适量冷水,再分离出苯乙酸粗品。
继续反应。反应结束后加适量冷水,再分离出苯乙酸粗品。ⅲ.将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入
 搅拌
搅拌 ,过滤,滤液静置一段时间,析出苯乙酸铜晶体。回答下列问题:
,过滤,滤液静置一段时间,析出苯乙酸铜晶体。回答下列问题:(1)配制70%硫酸时,加入蒸馏水与浓硫酸的先后顺序是:先加
(2)在装置中,仪器b的名称是___________。
| A.球形分液漏斗 | B.梨形分液漏斗 | C.恒压滴液漏斗 | D.长颈漏斗 |
(3)仪器c的作用是
(4)下列仪器中可用于分离苯乙酸粗品,除漏斗外,还有___________。
| A.分液漏斗 | B.玻璃棒 | C.烧杯 | D.直形冷凝管 |
(5)写出用
 和
和 溶液制备
溶液制备 沉淀的化学方程式
沉淀的化学方程式(6)最终得到
 苯乙酸晶体,则苯乙酸的产率是
苯乙酸晶体,则苯乙酸的产率是(7)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置电解
 溶液,该电池的负极反应式为
溶液,该电池的负极反应式为
您最近一年使用:0次
名校
4 . 为证明乙烯能被酸性KMnO4溶液氧化,某小组按下图装置制备乙烯并检验其化学性质。完成下列填空:
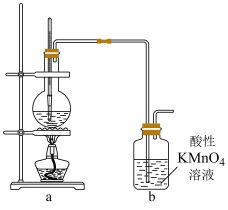
(1)首项检验该装置气密性。检验气密性的操作是__________ 。
(2)向圆底烧瓶中加入药品的顺序是:先加入______ ,再缓慢加入_______ ,最后再加入几粒碎瓷片。
(3)加热圆底烧瓶,使温度迅速上升到______ ℃,观察到烧瓶中的无色液体逐渐变黑。该黑色的物质是__________ 。
(4)酸性KMnO4溶液很快褪色,但不能说明乙烯具有还原性。理由是____________________________ 。
(5)选用下列装置(可重复使用也不可用)来证明乙烯具有还原性,请在a,b装置间补充装置,按编号依次排列,并按照对应顺序写出装置内所放的药品。
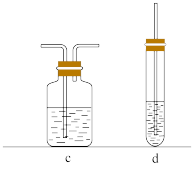
装置:a→____ →b
药品:(a药品略)________________________ (b酸性KMnO4溶液)
(6)若将b中酸性KMnO4溶液换成溴水,溴水也能褪色且可观察到b底部有少量无色油状液体生成,如何通过实验证明该无色油状液体中含有溴元素?_____________________________________
(7)试设计一条以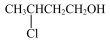 为原料合成
为原料合成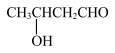 的合成路线
的合成路线____________________________ 。(合成路线常用的表示方式为:甲 乙
乙
 目标产物)
目标产物)

(1)首项检验该装置气密性。检验气密性的操作是
(2)向圆底烧瓶中加入药品的顺序是:先加入
(3)加热圆底烧瓶,使温度迅速上升到
(4)酸性KMnO4溶液很快褪色,但不能说明乙烯具有还原性。理由是
(5)选用下列装置(可重复使用也不可用)来证明乙烯具有还原性,请在a,b装置间补充装置,按编号依次排列,并按照对应顺序写出装置内所放的药品。

装置:a→
药品:(a药品略)
(6)若将b中酸性KMnO4溶液换成溴水,溴水也能褪色且可观察到b底部有少量无色油状液体生成,如何通过实验证明该无色油状液体中含有溴元素?
(7)试设计一条以
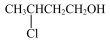 为原料合成
为原料合成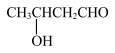 的合成路线
的合成路线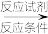 乙
乙
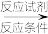 目标产物)
目标产物)
您最近一年使用:0次
名校
解题方法
5 . 实验室用如图所示装置制取溴乙烷。在试管I中依次加入2mL蒸馏水、4mL浓硫酸、2mL95%的乙醇和3g溴化钠粉末,在试管II中加入冰水混合物,在烧杯中注入自来水。加热试管I至微沸状态数分钟后,冷却。

(1)试管I中浓硫酸与溴化钠加热反应生成氢溴酸,写出氢溴酸与乙醇在加热时反应的化学方程式:_____ 。
(2)溴乙烷的官能团为______ (结构简式)。
(3)试管II中冰水混合物的作用是______ 。
(4)若试管II中获得的有机物呈棕黄色,除去其中的杂质最佳的试剂是_____ (填序号)。
a.CCl4 b.NaOH溶液 c.Na2SO3溶液 d.稀硫酸
(5)设计实验证明溴乙烷中含有溴元素(说明操作、现象和结论):______ 。
(6)已知溴乙烷可以与钠发生反应:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr。应用该反应原理,下列化合物中可以与钠反应合成环丁烷的是_____ (填序号)。
a.CH3CH2CH2CH2Br b.CH3CHBrCH2CH2Br
c.CH3CH2CHBrCH2Br d.CH2BrCH2CH2CH2Br
(7)写出由溴苯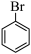 制备环己酮
制备环己酮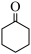 的流程:
的流程:_____ 。
(合成路线常用的表示方式为:甲 乙……
乙…… 目标产物)
目标产物)

(1)试管I中浓硫酸与溴化钠加热反应生成氢溴酸,写出氢溴酸与乙醇在加热时反应的化学方程式:
(2)溴乙烷的官能团为
(3)试管II中冰水混合物的作用是
(4)若试管II中获得的有机物呈棕黄色,除去其中的杂质最佳的试剂是
a.CCl4 b.NaOH溶液 c.Na2SO3溶液 d.稀硫酸
(5)设计实验证明溴乙烷中含有溴元素(说明操作、现象和结论):
(6)已知溴乙烷可以与钠发生反应:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr。应用该反应原理,下列化合物中可以与钠反应合成环丁烷的是
a.CH3CH2CH2CH2Br b.CH3CHBrCH2CH2Br
c.CH3CH2CHBrCH2Br d.CH2BrCH2CH2CH2Br
(7)写出由溴苯
 制备环己酮
制备环己酮 的流程:
的流程:(合成路线常用的表示方式为:甲
 乙……
乙…… 目标产物)
目标产物)
您最近一年使用:0次
2023-03-17更新
|
456次组卷
|
2卷引用:上海市七宝中学2022-2023学年高二下学期开学等级考化学试题
名校
6 . 有机合成是有机化学的重要组成部分,如图是关于气体A制备和性质的合成路线图。已知C是一种塑料,D是一种植物生长调节剂,可以催熟果实。
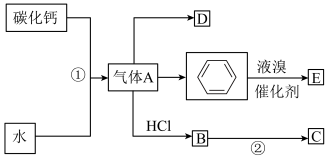
(1)①的化学方程式为______ 。
(2)②的化学方程式为______ ,该反应属于______ 反应(填反应类型)。
(3)D中的官能团为______ (填名称),写出实验室制D的化学方程式为______ ,该反应属于______ 反应(填反应类型)。
(4)与链烃相比,苯的化学性质的主要特征是 (单选)。
(5)证明苯制备E为取代反应的实验方案是______ 。已知硝基为间位定位基团,溴原子为邻、对位定位基团,写出以苯原料,制各间溴硝基苯的合成路线_____ 。
(合成路线的表示方式为:甲 乙
乙 目标产物)
目标产物)
(6)与上述物质有关的化学实验的说法中,正确的是 (单选)。

(1)①的化学方程式为
(2)②的化学方程式为
(3)D中的官能团为
(4)与链烃相比,苯的化学性质的主要特征是 (单选)。
| A.难氧化、难取代、难加成 | B.易氧化、易取代、易加成 |
| C.难氧化、能加成、易取代 | D.易氧化、易加成、难取代 |
(合成路线的表示方式为:甲
 乙
乙 目标产物)
目标产物)(6)与上述物质有关的化学实验的说法中,正确的是 (单选)。
| A.实验室制备乙烯时,产生的气体使溴水褪色,能证明有乙烯生成 |
| B.除去溴苯中的溴,可用稀NaOH溶液反复洗涤,并用分液漏斗分液 |
| C.实验室制乙炔,反应物为固体和液体,且常温条件下反应,可以用启普发生器 |
| D.制取硝基苯时,试管中先加入浓H2SO4,再逐滴滴入浓HNO3和苯 |
您最近一年使用:0次
名校
7 . 实验室用图所示的装置制取溴乙烷。在试管I中依次加入2mL蒸馏水、4mL浓硫酸、2mL95%的乙醇和3g溴化钠粉末,在试管II中加入冰水混合物,在烧杯中注入自来水。加热试管I至微沸状态数分钟后,冷却。

(1)试管I中浓硫酸与溴化钠加热反应生成氢溴酸,写出氢溴酸与乙醇在加热时反应的化学方程式:_______ 。
(2)溴乙烷为无色油状液体,其官能团为_______ (写名称);
(3)试管II中冰水混合物的作用是_______ 。
(4)若试管II中获得的有机物呈棕黄色,除去其中的杂质最佳的试剂是_______(填序号)。
(5)设计实验证明溴乙烷中含有溴元素(说明操作、现象和结论):_______ 。
(6)已知溴乙烷可以与钠发生反应:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr。应用该反应原理,下列化合物中可以与钠反应合成环丁烷的是_______(填序号)。
(7)写出由溴苯( )制备环己酮(
)制备环己酮( )的流程
)的流程_______ 。(合成路线常用的表示方式为:甲 乙
乙
 目标产物)
目标产物)

(1)试管I中浓硫酸与溴化钠加热反应生成氢溴酸,写出氢溴酸与乙醇在加热时反应的化学方程式:
(2)溴乙烷为无色油状液体,其官能团为
(3)试管II中冰水混合物的作用是
(4)若试管II中获得的有机物呈棕黄色,除去其中的杂质最佳的试剂是_______(填序号)。
| A.CCl4 | B.NaOH溶液 | C.Na2SO3溶液 | D.稀硫酸 |
(6)已知溴乙烷可以与钠发生反应:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr。应用该反应原理,下列化合物中可以与钠反应合成环丁烷的是_______(填序号)。
| A.CH3CH2CH2CH2Br | B.CH3CHBrCH2CH2Br | C.CH3CH2CHBrCH2Br | D.CH2BrCH2CH2CH2Br |
 )制备环己酮(
)制备环己酮( )的流程
)的流程 乙
乙
 目标产物)
目标产物)
您最近一年使用:0次
2022-04-23更新
|
405次组卷
|
2卷引用:上海市大同中学2021-2022学年高二下学期期中学情调研化学(等级考)试题
名校
解题方法
8 . I.将如图装置放置在光亮的地方,随后观察到如下实验现象:大试管内壁上有油状液滴生成、饱和食盐水中有少量固体析出、黄绿色气体颜色变浅、试管内液面有所上升。
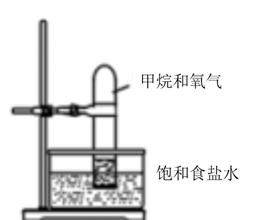
(1)油状液滴中属于非极性分子的电子式为________ 。
(2)水槽中盛放饱和食盐水而不是蒸馏水是为了抑制________ 与水的反应。试管内液面上升的原因是________ 极易溶于水。
II.乙烯是一种重要的化工原料,以乙烯为原料生产部分化工产品的反应如下(部分反应条件已略去):
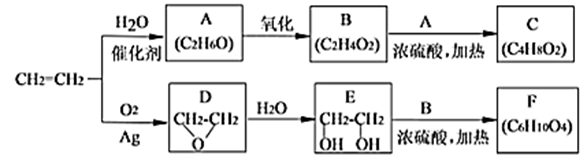
请回答下列问题:
(3)A的名称是________ ,含有的官能团名称是________ 。实验室A转化为乙烯的反应条件为________ 。
(4)B和A反应生成C的化学方程式为________ ,该反应的类型为________ 。
(5)F的结构简式为______________ 。
(6)写出D的同分异构体的结构简式__________________ 。
(7)乙炔也是常见的一种化工原料,它可以制取很多化工产品,例如:聚氯乙烯塑料。写出乙炔合成聚氯乙烯的合成路线。(合成路线常用的表示方式为:A B
B ……目标产物)
……目标产物)______________

(1)油状液滴中属于非极性分子的电子式为
(2)水槽中盛放饱和食盐水而不是蒸馏水是为了抑制
II.乙烯是一种重要的化工原料,以乙烯为原料生产部分化工产品的反应如下(部分反应条件已略去):

请回答下列问题:
(3)A的名称是
(4)B和A反应生成C的化学方程式为
(5)F的结构简式为
(6)写出D的同分异构体的结构简式
(7)乙炔也是常见的一种化工原料,它可以制取很多化工产品,例如:聚氯乙烯塑料。写出乙炔合成聚氯乙烯的合成路线。(合成路线常用的表示方式为:A
 B
B ……目标产物)
……目标产物)
您最近一年使用:0次
名校
解题方法
9 . 硫酸的工业制备是一个重要的化工生产过程,但同时在生产过程中会产生大量SO2等污染物。以硫酸工业的尾气、氨水、石灰石、焦炭及氯化钾为原料可以合成有重要用途的硫化钙、硫酸钾、氯化铵、亚硫酸铵等物质。合成路线如下:
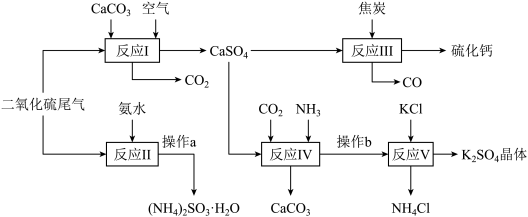
完成下列填空:
(1)某电厂每月用煤300t(煤中含硫的质量分数为2.5%),若燃烧时煤中的硫全部转化为二氧化硫,现用反应Ⅰ的原理将尾气中的SO2转化为石膏,且反应过程中96%的硫转化为石膏,则可生产石膏______ t。
(2)操作a中,必须的操作步骤有蒸发、___________ 、___________ 等;
(3)反应Ⅲ中氧化剂与还原剂的物质的量之比为__________ ;
(4)写出反应Ⅳ的方程式______________ ;操作b所得滤液中阳离子的检验方法是________________ 。
(5)反应Ⅴ在25℃,40%乙二醇溶液中进行,该复分解反应能顺利进行的原因是___________ ;
(6)该生产过程中可以循环使用的物质是_______________ 。

完成下列填空:
(1)某电厂每月用煤300t(煤中含硫的质量分数为2.5%),若燃烧时煤中的硫全部转化为二氧化硫,现用反应Ⅰ的原理将尾气中的SO2转化为石膏,且反应过程中96%的硫转化为石膏,则可生产石膏
(2)操作a中,必须的操作步骤有蒸发、
(3)反应Ⅲ中氧化剂与还原剂的物质的量之比为
(4)写出反应Ⅳ的方程式
(5)反应Ⅴ在25℃,40%乙二醇溶液中进行,该复分解反应能顺利进行的原因是
(6)该生产过程中可以循环使用的物质是
您最近一年使用:0次
2022·上海·一模
解题方法
10 . 硫酸四氨合铜晶体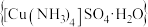 常用作杀虫剂、媒染剂,也是碱性镀铜中电镀液的主要成分。某学习小组在实验室以铜为主要原料合成该物质,设计的合成路线为
常用作杀虫剂、媒染剂,也是碱性镀铜中电镀液的主要成分。某学习小组在实验室以铜为主要原料合成该物质,设计的合成路线为
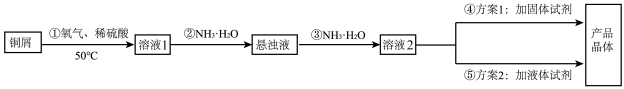
已知: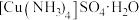 为绛蓝色晶体,常温下在空气中易与水和二氧化碳反应,生成铜的碱式盐使晶体变成绿色的粉末。在溶液中存在以下电离
为绛蓝色晶体,常温下在空气中易与水和二氧化碳反应,生成铜的碱式盐使晶体变成绿色的粉末。在溶液中存在以下电离 解离
解离 过程:
过程:
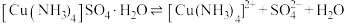 ,
,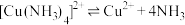
 及
及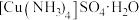 在水中均可溶,在乙醇中均难溶。
在水中均可溶,在乙醇中均难溶。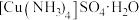 在乙醇和水的混合溶剂中的溶解度随乙醇体积分数的增大而减小。若在铜氨溶液中加入乙醇,会析出绛蓝色的硫酸四氨合铜晶体;实验表明,若在铜氨溶液中加入硫酸铵或硫酸钠,同样会有硫酸四氨合铜晶体析出。
在乙醇和水的混合溶剂中的溶解度随乙醇体积分数的增大而减小。若在铜氨溶液中加入乙醇,会析出绛蓝色的硫酸四氨合铜晶体;实验表明,若在铜氨溶液中加入硫酸铵或硫酸钠,同样会有硫酸四氨合铜晶体析出。
回答下列问题:
(1)实验室通常采用将铜屑浸泡在热的稀硫酸中,然后向其中不断通入热空气的方法来制备 溶液。
溶液。
 写出制备
写出制备 溶液时发生反应的离子方程式:
溶液时发生反应的离子方程式:________________________ 。
 为了使制备过程中稀硫酸的温度保持在
为了使制备过程中稀硫酸的温度保持在 ,需要对稀硫酸进行加热保温。应该采用的加热方式为
,需要对稀硫酸进行加热保温。应该采用的加热方式为________ ,该加热方式的优点为________________________ 。
(2)方案 向溶液
向溶液 中所加的固体试剂为
中所加的固体试剂为________  填
填 种试剂的化学式
种试剂的化学式 ;试说明为何加入该固体试剂后会有
;试说明为何加入该固体试剂后会有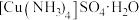 晶体析出:
晶体析出:________________________ 。
(3)方案 的实验步骤为
的实验步骤为 加热蒸发,
加热蒸发, 冷却溶液,
冷却溶液, 加
加 乙醇、结晶
乙醇、结晶 。
。
该方案存在一定缺陷,因为利用方案 得到的产品晶体中往往含有
得到的产品晶体中往往含有________ 杂质,产生杂质的原因是________________ 。
(4)方案 、
、 的最后操作步骤均为过滤、洗涤、干燥。
的最后操作步骤均为过滤、洗涤、干燥。
 过滤操作的主要目的是将固液混合物进行分离。中学化学中常见的用于固液混合物分离的操作有“倾析法”“普通过滤”和“减压过滤”等,操作示意图如下:
过滤操作的主要目的是将固液混合物进行分离。中学化学中常见的用于固液混合物分离的操作有“倾析法”“普通过滤”和“减压过滤”等,操作示意图如下:

减压过滤相对于普通过滤的优点为________  填字母下同
填字母下同 。
。
A.过滤速度相对较快
B.能过滤胶状混合物
C.得到的固体物质相对比较干燥
D.可以过滤具有强腐蚀性的固液混合物
 洗涤步骤中可选用的洗涤液是
洗涤步骤中可选用的洗涤液是________ 。
A.乙醇与乙醚的混合液 蒸馏水
蒸馏水
C.乙醇和水的混合液 饱和硫酸钠溶液
饱和硫酸钠溶液
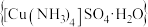 常用作杀虫剂、媒染剂,也是碱性镀铜中电镀液的主要成分。某学习小组在实验室以铜为主要原料合成该物质,设计的合成路线为
常用作杀虫剂、媒染剂,也是碱性镀铜中电镀液的主要成分。某学习小组在实验室以铜为主要原料合成该物质,设计的合成路线为
已知:
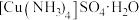 为绛蓝色晶体,常温下在空气中易与水和二氧化碳反应,生成铜的碱式盐使晶体变成绿色的粉末。在溶液中存在以下电离
为绛蓝色晶体,常温下在空气中易与水和二氧化碳反应,生成铜的碱式盐使晶体变成绿色的粉末。在溶液中存在以下电离 解离
解离 过程:
过程: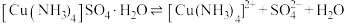 ,
,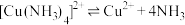
 及
及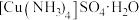 在水中均可溶,在乙醇中均难溶。
在水中均可溶,在乙醇中均难溶。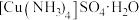 在乙醇和水的混合溶剂中的溶解度随乙醇体积分数的增大而减小。若在铜氨溶液中加入乙醇,会析出绛蓝色的硫酸四氨合铜晶体;实验表明,若在铜氨溶液中加入硫酸铵或硫酸钠,同样会有硫酸四氨合铜晶体析出。
在乙醇和水的混合溶剂中的溶解度随乙醇体积分数的增大而减小。若在铜氨溶液中加入乙醇,会析出绛蓝色的硫酸四氨合铜晶体;实验表明,若在铜氨溶液中加入硫酸铵或硫酸钠,同样会有硫酸四氨合铜晶体析出。回答下列问题:
(1)实验室通常采用将铜屑浸泡在热的稀硫酸中,然后向其中不断通入热空气的方法来制备
 溶液。
溶液。 写出制备
写出制备 溶液时发生反应的离子方程式:
溶液时发生反应的离子方程式: 为了使制备过程中稀硫酸的温度保持在
为了使制备过程中稀硫酸的温度保持在 ,需要对稀硫酸进行加热保温。应该采用的加热方式为
,需要对稀硫酸进行加热保温。应该采用的加热方式为(2)方案
 向溶液
向溶液 中所加的固体试剂为
中所加的固体试剂为 填
填 种试剂的化学式
种试剂的化学式 ;试说明为何加入该固体试剂后会有
;试说明为何加入该固体试剂后会有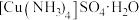 晶体析出:
晶体析出:(3)方案
 的实验步骤为
的实验步骤为 加热蒸发,
加热蒸发, 冷却溶液,
冷却溶液, 加
加 乙醇、结晶
乙醇、结晶 。
。该方案存在一定缺陷,因为利用方案
 得到的产品晶体中往往含有
得到的产品晶体中往往含有(4)方案
 、
、 的最后操作步骤均为过滤、洗涤、干燥。
的最后操作步骤均为过滤、洗涤、干燥。 过滤操作的主要目的是将固液混合物进行分离。中学化学中常见的用于固液混合物分离的操作有“倾析法”“普通过滤”和“减压过滤”等,操作示意图如下:
过滤操作的主要目的是将固液混合物进行分离。中学化学中常见的用于固液混合物分离的操作有“倾析法”“普通过滤”和“减压过滤”等,操作示意图如下:
减压过滤相对于普通过滤的优点为
 填字母下同
填字母下同 。
。A.过滤速度相对较快
B.能过滤胶状混合物
C.得到的固体物质相对比较干燥
D.可以过滤具有强腐蚀性的固液混合物
 洗涤步骤中可选用的洗涤液是
洗涤步骤中可选用的洗涤液是A.乙醇与乙醚的混合液
 蒸馏水
蒸馏水C.乙醇和水的混合液
 饱和硫酸钠溶液
饱和硫酸钠溶液
您最近一年使用:0次



