2010·江苏扬州·模拟预测
1 . 氯碱工业的原料饱和食盐水中含有一定量的铵根离子,在电解时会生成性质极不稳定的三氯化氮,容易引起爆炸。
(1)三氯化氮易水解,其水解的最初产物除生成氨气外,另一产物为_________ 。
(2)为除去饱和食盐水中的铵根离子,可在碱性条件下通入氯气,反应生成氮气。该反应的离子方程式为________ 。该工艺选择氯气的优点是__________ 。(答一点即可)
(3)过量氯气用Na2S2O3除去,反应中S2O32-被氧化为SO42-。若过量的氯气为10-3 mol/L,则理论上生成的SO42-为___________ mol/L。
(4)生产和实验中广泛采用甲醛法测定样品的含氮量。甲醛和铵根离子的反应如下:
4NH4++ 6HCHO =(CH2)6N4H+(一元酸)+ 3H+ + 6H2O
实验步骤如下:
①甲醛中常含有微量甲酸,应先除去。可取甲醛bmL于锥形瓶,加入1滴酚酞,用浓度为Cmol/L的NaOH溶液中和,滴定管的初始读数V1mL,当溶液呈微红色时,滴定管的读数V2mL。
②向其中加入饱和食盐水试样amL,静置1分钟。
③再加1~2滴酚酞,再用上述NaOH溶液滴定至微红色,滴定管的读数V3mL。
则饱和食盐水中的含氮量为__________ mg/L。
(1)三氯化氮易水解,其水解的最初产物除生成氨气外,另一产物为
(2)为除去饱和食盐水中的铵根离子,可在碱性条件下通入氯气,反应生成氮气。该反应的离子方程式为
(3)过量氯气用Na2S2O3除去,反应中S2O32-被氧化为SO42-。若过量的氯气为10-3 mol/L,则理论上生成的SO42-为
(4)生产和实验中广泛采用甲醛法测定样品的含氮量。甲醛和铵根离子的反应如下:
4NH4++ 6HCHO =(CH2)6N4H+(一元酸)+ 3H+ + 6H2O
实验步骤如下:
①甲醛中常含有微量甲酸,应先除去。可取甲醛bmL于锥形瓶,加入1滴酚酞,用浓度为Cmol/L的NaOH溶液中和,滴定管的初始读数V1mL,当溶液呈微红色时,滴定管的读数V2mL。
②向其中加入饱和食盐水试样amL,静置1分钟。
③再加1~2滴酚酞,再用上述NaOH溶液滴定至微红色,滴定管的读数V3mL。
则饱和食盐水中的含氮量为
您最近一年使用:0次
10-11高三上·浙江杭州·阶段练习
2 . 金属锡的纯度可以通过下述方法测定:将样品溶于盐酸Sn+2HCl=SnCl2+H2↑,再加过量的FeCl3溶液。发生如下反应:SnCl2+2FeCl3=SnCl4+2FeCl2,最后可用一定浓度的K2Cr2O7溶液滴定生成的Fe2+,此时还原产物为Cr3+。现有金属锡试样0.613g,经上述反应后,共用去0.1mol/L的K2Cr2O7的硫酸溶液16.0mL。
⑴ 写出K2Cr2O7氧化Fe2+的离子方程式,并配平__________________ ;
⑵ 试样中锡的质量分数(假定杂质不参加反应)__________________ 。
⑴ 写出K2Cr2O7氧化Fe2+的离子方程式,并配平
⑵ 试样中锡的质量分数(假定杂质不参加反应)
您最近一年使用:0次
10-11高三上·浙江杭州·阶段练习
3 . 某天然碱可以看作是CO2和NaOH反应后的产物组成的一种物质。为了测定该物质的成分,进行如下实验:⑴称取3.32g天然碱样品,加入30mL过量稀盐酸,产生672mL CO2气体(标准状况);⑵另称取3.32g天然碱样品,在300℃下加热至分解完全,产生CO2 112mL(标准状况)和0.45g水。试通过计算,确定天然碱的化学式。
您最近一年使用:0次
解题方法
4 . 某化学探究小组拟用铜片制取Cu(NO3)2,并探究其化学性质。
I.他们先把铜粉放在空气中灼烧,再与稀HNO3反应制取硝酸铜。
(1)如果直接用铜屑与稀HNO3反应来制取硝酸铜,可能导致的两个不利因素是______ 。
(2)实验中铜粉应该放在_____ (选填“蒸发皿”、“坩埚”或“烧杯”)中灼烧。欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤按顺序分别是___ 、____ 、过滤。
II.为了探究Cu(NO3)2的热稳定性,探究小组按下图中的装置进行实验。(图中铁架台、铁夹和加热设备均略去)
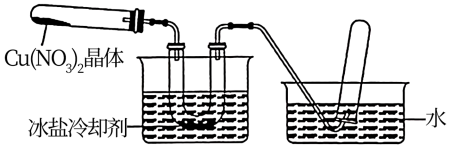
往左试管中放入研细的无水Cu(NO3)2晶体并加热,观察到左试管中有红棕色气体生成,最终残留黑色粉末;用U形管除去红棕色气体,在右试管中收集到无色气体。
(1)红棕色气体是____ 。
(2)当导管口不再有气泡冒出时,停止反应,这时在操作上应注意________ 。
(3)探究小组判断Cu(NO3)2的分解属于氧化还原反应,产物除了红棕色气体和黑色固体外,进一步分析、推断,分解产物中一定还含有_____ 。
III.为了探究Cu(NO3)2在酸性条件下跟铁单质的反应。他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质。该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请在下面表格中补充写出实验操作步骤、预期现象与结论___ 、___ 、___ 。
I.他们先把铜粉放在空气中灼烧,再与稀HNO3反应制取硝酸铜。
(1)如果直接用铜屑与稀HNO3反应来制取硝酸铜,可能导致的两个不利因素是
(2)实验中铜粉应该放在
II.为了探究Cu(NO3)2的热稳定性,探究小组按下图中的装置进行实验。(图中铁架台、铁夹和加热设备均略去)

往左试管中放入研细的无水Cu(NO3)2晶体并加热,观察到左试管中有红棕色气体生成,最终残留黑色粉末;用U形管除去红棕色气体,在右试管中收集到无色气体。
(1)红棕色气体是
(2)当导管口不再有气泡冒出时,停止反应,这时在操作上应注意
(3)探究小组判断Cu(NO3)2的分解属于氧化还原反应,产物除了红棕色气体和黑色固体外,进一步分析、推断,分解产物中一定还含有
III.为了探究Cu(NO3)2在酸性条件下跟铁单质的反应。他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质。该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请在下面表格中补充写出实验操作步骤、预期现象与结论
| 实验操作步骤 | 预期现象与结论 |
| 步骤1:观察样品 | 溶液呈蓝绿色, (填“能”或“不能”)确定 产物中铁元素的化合价 |
| 步骤2:取少量溶液,滴加酸性KMnO4溶液 | |
| 步骤3: | 若溶液变为红色,说明产物中含+3价的铁 元素;若溶液颜色无明显变化,则说明产物 中不含+3价的铁元素 |
您最近一年使用:0次
解题方法
5 . 某化学探究小组拟用铜片制取Cu(NO3)2,并探究其化学性质。
Ⅰ、他们先把铜粉放在空气中灼烧,再与稀硝酸反应制取硝酸铜。
(1)如果直接用铜屑与稀硝酸反应来制取硝酸铜,可能导致的两个不利因素是_______________ 、________________ 。
(2)实验中铜粉应该放在_________ (填“蒸发皿”“坩埚”或“烧杯”)中灼烧。欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤按顺序分别是_________ 、________ 、过滤。
Ⅱ、为了探究Cu(NO3)2在酸性条件下跟铁单质的反应。他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质。
(3)该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请按下表格式补充写出实验操作步骤、预期现象与结论。
Ⅰ、他们先把铜粉放在空气中灼烧,再与稀硝酸反应制取硝酸铜。
(1)如果直接用铜屑与稀硝酸反应来制取硝酸铜,可能导致的两个不利因素是
(2)实验中铜粉应该放在
Ⅱ、为了探究Cu(NO3)2在酸性条件下跟铁单质的反应。他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质。
(3)该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请按下表格式补充写出实验操作步骤、预期现象与结论。
| 实验操作步骤 | 预期现象与结论 |
| 步骤1:观察样品 | 溶液呈蓝绿色,① |
| 步骤2: 取少量溶液,滴加酸性KMnO4溶液 | ② |
| 步骤3: ③ | 若溶液变为红色,说明产物中含+3价的铁元素;若溶液颜色无明显变化,则说明产物中不含+3价的铁元素 |
您最近一年使用:0次
解题方法
6 . 某化学探究小组拟用铜片制取Cu(NO3)2,并探究其化学性质。
Ⅰ、他们先把铜粉放在空气中灼烧,再与稀硝酸反应制取硝酸铜。
(1)如果直接用铜屑与稀硝酸反应来制取硝酸铜:
①铜屑与稀硝酸反应的化学反应方程式为____________________ ;
②可能导致的两个不利因素是_____________ 、________________ 。
(2)实验中,欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤按顺序是_____ 、______ 、过滤、晾干。
Ⅱ、为了探究Cu(NO3)2在酸性条件下跟铁单质的反应。他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质。
(3)该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请按下表格式补充写出实验操作步骤、预期现象与结论。
Ⅰ、他们先把铜粉放在空气中灼烧,再与稀硝酸反应制取硝酸铜。
(1)如果直接用铜屑与稀硝酸反应来制取硝酸铜:
①铜屑与稀硝酸反应的化学反应方程式为
②可能导致的两个不利因素是
(2)实验中,欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤按顺序是
Ⅱ、为了探究Cu(NO3)2在酸性条件下跟铁单质的反应。他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质。
(3)该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请按下表格式补充写出实验操作步骤、预期现象与结论。
| 实验操作步骤 | 预期现象与结论 |
| 步骤1:观察样品 | 溶液呈蓝绿色,① |
| 步骤2:取少量溶液,滴加酸性KMnO4溶液 | ② |
| 步骤3:③另取少量溶液,滴加KSCN溶 | ③ |
您最近一年使用:0次
解题方法
7 . 某化学探究小组拟用铜片制取Cu(NO3)2,并探究其化学性质。
(一)他们先把铜粉放在空气中灼烧,再与稀HNO3反应制取硝酸铜。
(1)如果直接用铜屑与稀HNO3反应来制取硝酸铜,可能导致的两个不利因素______________ 、____________ 。
(2)实验中铜粉应该放在_____________ (填“蒸发皿”、“坩埚”或“烧杯”)中灼烧。欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤是_____________ 、过滤。
(二)为了探究Cu(NO3)2的热稳定性,探究小组按下图中的装置进行实验。(图中铁架台、铁夹和加热设备均略去)
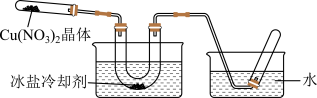
往左试管中放入研细的无水Cu(NO3)2晶体并加热,观察到左试管中有红棕色气体生成,最终残留黑色粉末;用U形管除去红棕色气体,在右试管中收集到无色气体。
(3)当导管口不再有气泡冒出时,停止反应,这时在操作上应注意________________ 。
(4)探究小组判断Cu(NO3)2的分解属于氧化还原反应,产物除了红棕色气体和黑色固体外,进一步分析、推断,分解产物中一定还含有____________ 。
(三)为了探究Cu(NO3)2在酸性条件下跟铁单质的反应。他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质。
(5)反应中最先起氧化作用的是__________ 。
(6)该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请按下表格式补充写出实验操作步骤、预期现象与结论。
(一)他们先把铜粉放在空气中灼烧,再与稀HNO3反应制取硝酸铜。
(1)如果直接用铜屑与稀HNO3反应来制取硝酸铜,可能导致的两个不利因素
(2)实验中铜粉应该放在
(二)为了探究Cu(NO3)2的热稳定性,探究小组按下图中的装置进行实验。(图中铁架台、铁夹和加热设备均略去)

往左试管中放入研细的无水Cu(NO3)2晶体并加热,观察到左试管中有红棕色气体生成,最终残留黑色粉末;用U形管除去红棕色气体,在右试管中收集到无色气体。
(3)当导管口不再有气泡冒出时,停止反应,这时在操作上应注意
(4)探究小组判断Cu(NO3)2的分解属于氧化还原反应,产物除了红棕色气体和黑色固体外,进一步分析、推断,分解产物中一定还含有
(三)为了探究Cu(NO3)2在酸性条件下跟铁单质的反应。他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质。
(5)反应中最先起氧化作用的是
(6)该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请按下表格式补充写出实验操作步骤、预期现象与结论。
| 实验操作步骤 | 预期现象与结论 |
| 步骤1:观察样品 | 溶液呈蓝绿色, 确定产物中铁元素的价态 |
| 步骤2:取少量溶液,滴加酸性KMnO4溶液 | |
| 步骤3: | 若溶液变为红色,说明产物中含+3价的铁元素; 若溶液颜色无明显变化,则说明产物中不含+3价的铁元素 |
您最近一年使用:0次



