名校
1 . 下列实验操作能达到相应目的的是
| 选项 | 实验目的 | 实验内容 |
| A | 制备氢氧化铁胶体 | 向沸腾的氢氧化钠溶液中逐滴加入饱和氯化铁溶液 |
| B | 检验溶液中是否含 | 取少量溶液,向其中加入浓 溶液,加热,在试管口放置湿润的蓝色石蕊试纸,观察试纸是否变红 溶液,加热,在试管口放置湿润的蓝色石蕊试纸,观察试纸是否变红 |
| C | 证明二氧化硫具有漂白性 | 将二氧化硫气体通入含有酚酞的氢氧化钠溶液中,观察溶液颜色变化 |
| D | 检验溶液中是否含 | 向溶液中加入几滴 溶液,观察溶液是否变红色 溶液,观察溶液是否变红色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-12更新
|
333次组卷
|
3卷引用:福建省福州屏东中学2022-2023学年高一下学期期中考试化学试题
2 . 下列关于胶体的叙述不正确的是
| A.胶体区别于溶液和浊液的本质特征是分散质粒子直径在1~100nm之间 |
| B.“朝坛雾卷,曙岭烟沉”,雾有丁达尔现象是因为胶体粒子对光有散射作用 |
C.向氢氧化钠溶液中滴入几滴 饱和溶液,即可得到 饱和溶液,即可得到 胶体 胶体 |
D.用激光笔分别照射 溶液和 溶液和 胶体时,观察到的现象不相同 胶体时,观察到的现象不相同 |
您最近一年使用:0次
2023-06-08更新
|
416次组卷
|
2卷引用:福建省福州延安中学2023-2024学年高一上学期11月期中考试化学试题
3 . 下列说法不正确的是
| A.KAl(SO4)2•12H2O溶于NaOH溶液可形成Al(OH)3胶体 |
| B.将KCl溶液从常温加热至80℃,溶液的pH变小但仍保持中性 |
| C.常温下,NaCN溶液呈碱性,说明HCN是弱电解质 |
| D.常温下,pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大 |
您最近一年使用:0次
2023-01-16更新
|
172次组卷
|
4卷引用:福建省莆田第七中学、第十一中学、第十五中学等校2023-2024学年高二上学期期末联考化学试题
福建省莆田第七中学、第十一中学、第十五中学等校2023-2024学年高二上学期期末联考化学试题江苏省句容高级中学2022-2023学年高二上学期期末调研化学试题(已下线)专题09 水溶液中的离子平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(江苏专用)江苏省常熟市中学2023-2024学年高二上学期12月学业水平调研化学试卷
名校
解题方法
4 . 如图所示为实验室中制备胶体的一种方法。下列说法正确的是
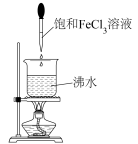

| A.该制备方法属于物理方法 | B.烧杯中液体的颜色逐渐变浅 |
| C.可用丁达尔效应判断是否制得胶体 | D.加热能促使该分散系中的分散质粒子直径减小 |
您最近一年使用:0次
2023-01-05更新
|
416次组卷
|
7卷引用:福建省龙岩市一级校联考2023-2024学年高一上学期11月期中考试化学试题
名校
解题方法
5 . 央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是_______ 价。 是一种酸根离子,则
是一种酸根离子,则 属于
属于_______ (填“酸”、“碱”、“盐”或“氧化物”)。
(2)明胶的水溶液和 溶液共同具备的性质是
溶液共同具备的性质是_______ (填序号)。
a.都不稳定,密封放置会产生沉淀
b.分散质粒子可通过滤纸
c.二者均有丁达尔效应
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的_______ (填序号)。
A.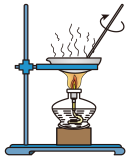 B.
B. 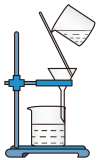 C.
C.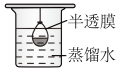
(4)实验室常用向煮沸的蒸馏水中滴加饱和 溶液制备
溶液制备 胶体,证明有胶体生成的最常用的实验操作是
胶体,证明有胶体生成的最常用的实验操作是_______ 。如向其中滴入过量稀硫酸,出现的现象是_______ 。
(1)已知
 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是 是一种酸根离子,则
是一种酸根离子,则 属于
属于(2)明胶的水溶液和
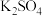 溶液共同具备的性质是
溶液共同具备的性质是a.都不稳定,密封放置会产生沉淀
b.分散质粒子可通过滤纸
c.二者均有丁达尔效应
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的
A.
 B.
B.  C.
C.
(4)实验室常用向煮沸的蒸馏水中滴加饱和
 溶液制备
溶液制备 胶体,证明有胶体生成的最常用的实验操作是
胶体,证明有胶体生成的最常用的实验操作是
您最近一年使用:0次
2022-10-25更新
|
207次组卷
|
3卷引用:福建省福州延安中学2023-2024学年高一上学期10月月考化学试题
名校
解题方法
6 . 为完成下列各组实验,所选玻璃仪器和试剂均准确、完整的是(不考虑存放试剂的容器)
| 实验目的 | 玻璃仪器 | 试剂 | |
| A | 配制 一定物质的量浓度的NaCl溶液 一定物质的量浓度的NaCl溶液 | 容量瓶、烧杯、量筒、玻璃棒 | 蒸馏水、NaCl固体 |
| B | 测定NaOH溶液浓度 | 烧杯、锥形瓶、胶头滴管、酸式滴定管 | 待测NaOH溶液、已知浓度的盐酸、甲基橙试剂 |
| C | 制备 胶体 胶体 | 烧杯、酒精灯、胶头滴管 | 蒸馏水、饱和 溶液 溶液 |
| D | 制备乙酸乙酯 | 试管、量筒、导管、酒精灯 | 冰醋酸、无水乙醇、饱和 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-10更新
|
1268次组卷
|
5卷引用:福建省福州八中2022-2023学年高三上学期质检模拟考化学试题
福建省福州八中2022-2023学年高三上学期质检模拟考化学试题(已下线)专题11 化学实验基础(练)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题05 突破化学实验基础(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)广东省广州市广东实验中学2023届高三第三次阶段考试化学试题(已下线)化学(广东卷02)-2024年高考押题预测卷
7 . 下列关于胶体的叙述正确的是
A.实验室将 溶液与氢氧化钠溶液混合制备氢氧化铁胶体 溶液与氢氧化钠溶液混合制备氢氧化铁胶体 |
| B.实验室制备的氢氧化铁胶体能导电,说明氢氧化铁胶体带电 |
C.向 胶体中逐滴滴加稀盐酸,先产生红褐色沉淀,后沉淀溶解 胶体中逐滴滴加稀盐酸,先产生红褐色沉淀,后沉淀溶解 |
| D.胶体区别于其他分散系的本质是能否发生丁达尔效应 |
您最近一年使用:0次
2023-01-04更新
|
239次组卷
|
3卷引用:福建省厦门大学附属科技中学2023-2024学年高一上学期12月月考化学试卷
名校
解题方法
8 . 现代生活需要人们有一定的科学素养,下列有关化学的科学常识说法正确的是
| A.碳酸钠俗名小苏打,可用作糕点膨松剂 |
| B.食物腐败、Fe(OH)3胶体的制备都与氧化还原反应有关 |
| C.为防止馅饼等富脂食品氧化变质,常在包装袋中放入生石灰 |
| D.榨苹果汁时加入维生素C,可减缓其在空气中发生颜色变化 |
您最近一年使用:0次
2022-12-30更新
|
411次组卷
|
3卷引用:福建省泉州市永春第一中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
9 . I、现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。甲同学:向1mol/L的FeCl3溶液中加少量NaOH溶液。乙同学:直接加热饱和FeCl3溶液。丙同学:向25mL沸水中逐滴加入5-6滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。试回答下列问题:
(1)其中操作正确的同学是___________ 。
(2)证明有Fe(OH)3胶体生成的简单实验操作是___________ 。
II、高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(3)干法制备高铁酸钠的主要反应为: 2FeSO4+6Na2O2=2Na2FeO4+2X+2Na2SO4+O2↑
①该反应中物质X应是___________ ,该反应的还原剂是___________ 。
②简要说明K2FeO4作为水处理剂时,在水处理过程中所起的作用___________
(4)已知湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、C1O-、OH-、FeO 、C1-、H2O
、C1-、H2O
①完成并配平湿法制备高铁酸钾(K2FeO4)的离子方程式,并用单线桥标出该反应的电子转移方向和数目:___________
②已知有3.21gFe(OH)3参加了反应,则上述反应共转移了___________ 个电子,
③根据(1)、(2)推测FeO 能和下列
能和下列___________ (填序号)物质反应。
A.KMnO4 B.SO2 C.H2S D.O2
(1)其中操作正确的同学是
(2)证明有Fe(OH)3胶体生成的简单实验操作是
II、高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(3)干法制备高铁酸钠的主要反应为: 2FeSO4+6Na2O2=2Na2FeO4+2X+2Na2SO4+O2↑
①该反应中物质X应是
②简要说明K2FeO4作为水处理剂时,在水处理过程中所起的作用
(4)已知湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、C1O-、OH-、FeO
 、C1-、H2O
、C1-、H2O①完成并配平湿法制备高铁酸钾(K2FeO4)的离子方程式,并用单线桥标出该反应的电子转移方向和数目:
②已知有3.21gFe(OH)3参加了反应,则上述反应共转移了
③根据(1)、(2)推测FeO
 能和下列
能和下列A.KMnO4 B.SO2 C.H2S D.O2
您最近一年使用:0次
10 . 下列实验操作能达到实验目的是
A.用带磨口玻璃瓶塞的玻璃瓶保存 溶液 溶液 |
| B.温度计被打破,洒在地面上的水银可以用水冲洗 |
C.配制浓 和浓 和浓 的混酸溶液时,将浓 的混酸溶液时,将浓 慢慢加到浓 慢慢加到浓 中,并及时用玻璃棒搅拌 中,并及时用玻璃棒搅拌 |
| D.向沸水中逐滴加入饱和氯化铁溶液并不断加热搅拌可得到氢氧化铁胶体 |
您最近一年使用:0次
2022-12-02更新
|
209次组卷
|
2卷引用:福建省德化一中、永安一中、漳平一中三校协作2022-2023学年高三上学期12月联考化学试题



