名校
解题方法
1 . 下表列出了①~⑩十种元素在周期表中的位置:
请按要求回答下列问题:
(1)上述元素中,金属性最强的是______ (填元素名称),最高价氧化物对应水化物酸性最强的是______ (填化学式)
(2)由元素③形成的单质的结构式为______ ,由元素⑥和⑨形成化合物乙,请用电子式表示物质乙的形成过程______ 。
(3)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为______ 。
(4)可以比较⑤、⑥两元素金属性强弱的实验是______。
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
4 | ⑩ |
(1)上述元素中,金属性最强的是
(2)由元素③形成的单质的结构式为
(3)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为
(4)可以比较⑤、⑥两元素金属性强弱的实验是______。
| A.比较这两种元素最高价氧化物对应的水化物的碱性 |
| B.将⑤的单质投入到⑥的盐溶液中 |
| C.将这两种元素的单质分别放入冷水中 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
您最近一年使用:0次
2 . 短周期主族元素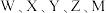 的原子序数依次增大,元素
的原子序数依次增大,元素 位于同一周期,且元素
位于同一周期,且元素 能组成红棕色的大气污染物,金属元素M的单质与冷水反应缓慢,但可与沸水迅速发生置换反应生成W的单质。下列有关说法错误的是
能组成红棕色的大气污染物,金属元素M的单质与冷水反应缓慢,但可与沸水迅速发生置换反应生成W的单质。下列有关说法错误的是
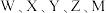 的原子序数依次增大,元素
的原子序数依次增大,元素 位于同一周期,且元素
位于同一周期,且元素 能组成红棕色的大气污染物,金属元素M的单质与冷水反应缓慢,但可与沸水迅速发生置换反应生成W的单质。下列有关说法错误的是
能组成红棕色的大气污染物,金属元素M的单质与冷水反应缓慢,但可与沸水迅速发生置换反应生成W的单质。下列有关说法错误的是A.简单离子半径: |
B.简单氢化物的还原性: |
C.由 三种元素组成的化合物的水溶液可能呈碱性 三种元素组成的化合物的水溶液可能呈碱性 |
D.M的氯化物的电子式为 |
您最近一年使用:0次
名校
解题方法
3 . I 亚硝酰氯(NOCl)是有机药物制备的重要试剂,可按以下流程合成和利用。
(1)NOCl的电子式为___________ ,化合物X的结构简式为___________ 。
(2)下列说法正确的是___________。
(3)已知浓盐酸和浓硝酸混合配制王水时会产生亚硝酰氯,写出该反应的化学方程式___________ 。
Ⅱ 请回答下列问题:
(4)由磷原子核形成的三种微粒:a. 、b.
、b. 、c.
、c. ,半径由大到小的顺序为
,半径由大到小的顺序为___________ (填标号,下同);再失去一个电子所需最低能量由大到小的顺序为___________ 。
(5)比较H-O-H键角大小;H3O+___________ H2O(填“>”、“<”或“=”)。
(6)C为有机材料的主角,Si为无机材料的主角,SiC结构类似金刚石,下图为SiC的晶胞图,其中两个正方体中心重合、各面分别平行,其中心为Si原子(用•表示),试在小立方体画出相应C原子(用 表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。
表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。___________

(1)NOCl的电子式为
(2)下列说法正确的是___________。
| A.NOCl中的氮元素呈正价 |
| B.NOCl分子的空间结构为直线形 |
C.化合物X的沸点低于氯乙酰胺(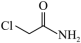 ) ) |
| D.工业上可以用蒸馏水吸收多余的NOCl,防止污染环境 |
(3)已知浓盐酸和浓硝酸混合配制王水时会产生亚硝酰氯,写出该反应的化学方程式
Ⅱ 请回答下列问题:
(4)由磷原子核形成的三种微粒:a.
 、b.
、b. 、c.
、c. ,半径由大到小的顺序为
,半径由大到小的顺序为(5)比较H-O-H键角大小;H3O+
(6)C为有机材料的主角,Si为无机材料的主角,SiC结构类似金刚石,下图为SiC的晶胞图,其中两个正方体中心重合、各面分别平行,其中心为Si原子(用•表示),试在小立方体画出相应C原子(用
 表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。
表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。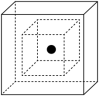
您最近一年使用:0次
名校
4 . 下列化学用语表示正确的是
| A.光导纤维主要成分的分子式:SiO2 |
| B.O2和O3互为同素异形体 |
C.空间填充模型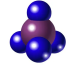 ,可表示CH4分子,也可表示CCl4分子 ,可表示CH4分子,也可表示CCl4分子 |
D.NH4Cl的电子式: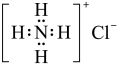 |
您最近一年使用:0次
名校
解题方法
5 . 十九世纪初,科学家用氰酸银(AgOCN)与NH4Cl在一定条件下反应制得尿素[CO(NH2)2]实现了由无机物到有机物的合成。下列有关说法正确的是
A.NH4Cl电子式为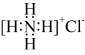 | B.电负性:C<O<N |
| C.氰酸铵与尿素互为同分异构体 | D.尿素中所有原子可能处于同一平面 |
您最近一年使用:0次
名校
6 . 无机物 均为短周期元素组成的物质,且均含有同种元素,其中
均为短周期元素组成的物质,且均含有同种元素,其中 是最简单氢化物、
是最简单氢化物、 是单质:上述物质在一定条件下可以发生如下转化。
是单质:上述物质在一定条件下可以发生如下转化。 为强碱,则
为强碱,则 的电子式为
的电子式为___________ 。
(2)若 为二元弱酸,则
为二元弱酸,则 的化学式为
的化学式为___________ 。
(3)若 为强酸,
为强酸, 在标准状况下是白色固体,则:
在标准状况下是白色固体,则:
① 的浓溶液与炭反应的化学方程式
的浓溶液与炭反应的化学方程式___________ 。
② 溶于水显酸性的原因(化学原理)是
溶于水显酸性的原因(化学原理)是___________ 。
(4)若 为强酸,且
为强酸,且 和
和 可以发生反应生成一种盐
可以发生反应生成一种盐 ,则:
,则:
① 的催化氧化是工业上制备硝酸的基础,其化学方程式
的催化氧化是工业上制备硝酸的基础,其化学方程式___________ 。
②实验室检验 中阳离子的离子方程式为
中阳离子的离子方程式为___________ 。
 均为短周期元素组成的物质,且均含有同种元素,其中
均为短周期元素组成的物质,且均含有同种元素,其中 是最简单氢化物、
是最简单氢化物、 是单质:上述物质在一定条件下可以发生如下转化。
是单质:上述物质在一定条件下可以发生如下转化。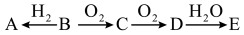
 为强碱,则
为强碱,则 的电子式为
的电子式为(2)若
 为二元弱酸,则
为二元弱酸,则 的化学式为
的化学式为(3)若
 为强酸,
为强酸, 在标准状况下是白色固体,则:
在标准状况下是白色固体,则:①
 的浓溶液与炭反应的化学方程式
的浓溶液与炭反应的化学方程式②
 溶于水显酸性的原因(化学原理)是
溶于水显酸性的原因(化学原理)是(4)若
 为强酸,且
为强酸,且 和
和 可以发生反应生成一种盐
可以发生反应生成一种盐 ,则:
,则:①
 的催化氧化是工业上制备硝酸的基础,其化学方程式
的催化氧化是工业上制备硝酸的基础,其化学方程式②实验室检验
 中阳离子的离子方程式为
中阳离子的离子方程式为
您最近一年使用:0次
名校
7 . 下列有关化学用语正确的是
A.15N的原子结构示意图: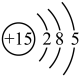 |
B.NaOH的电子式: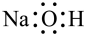 |
C.基态Cr原子的价层电子轨道表示式: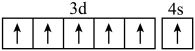 |
D.NH3分子的VSER模型: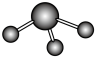 |
您最近一年使用:0次
名校
8 . 氯化钠是一种重要的化工原料,用它可以制取日常生活中常使的消毒剂、清洁剂等多种物质,如下图所示(X和Y都是单质)。___________ ;NaCl的电子式为___________ 。
(2)漂白粉的有效成分是___________ (填化学式);漂白粉在空气中的漂白原理的化学方程式为___________ 。
(3)曾有报道,因“洁厕灵”(酸性洗涤剂)与“84”消毒液(主要成分是NaClO)混合使用而发生中毒事件,用离子方程式分析其原因:___________ 。
(4)写出NaCl水溶液通电后发生反应的离子方程式___________ 。
(5)工业上甲醇(CH3OH)在NaOH(aq)下可做燃料电池,则氧气作电池的___________ 极;负极发生的电极反应式为___________ 。

(2)漂白粉的有效成分是
(3)曾有报道,因“洁厕灵”(酸性洗涤剂)与“84”消毒液(主要成分是NaClO)混合使用而发生中毒事件,用离子方程式分析其原因:
(4)写出NaCl水溶液通电后发生反应的离子方程式
(5)工业上甲醇(CH3OH)在NaOH(aq)下可做燃料电池,则氧气作电池的
您最近一年使用:0次
名校
9 . 反应 应用于石油开采。下列说法正确的是
应用于石油开采。下列说法正确的是
 应用于石油开采。下列说法正确的是
应用于石油开采。下列说法正确的是A. 的电子式为 的电子式为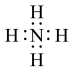 | B. 中N原子采用 中N原子采用 杂化 杂化 |
C. 晶体属于离子晶体 晶体属于离子晶体 | D. 为含极性键的非极性分子 为含极性键的非极性分子 |
您最近一年使用:0次
名校
10 . 下列化学用语描述正确的是
A. 的空间结构: 的空间结构: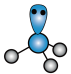 (三角锥形) (三角锥形) |
B.二氧化碳的空间填充模型: |
C. 的结构示意图: 的结构示意图: |
D.磷基态原子价层电子排布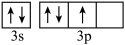 违背了泡利原理 违背了泡利原理 |
您最近一年使用:0次



