解题方法
1 . 现有四种前20号元素的有关信息如表所示:
下列说法错误的是
| 元素 | 相关信息 |
| W | 在前20号元素中,原子半径最大 |
| X | W+与X2-具有相同的电子层结构 |
| Y | 原子最外层电子数是内层电子数的2倍 |
| Z | 地壳中含量最多的元素 |
| A.原子序数大小顺序:W>X>Z>Y |
| B.X、Z的简单气态氢化物的稳定性:H2X<H2Z |
C.Y与Z组成的三原子分子的电子式为: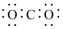 |
| D.W所在的主族中,金属单质的熔沸点逐渐降低 |
您最近一年使用:0次
解题方法
2 . 1—20号元素中的A、B、C、D、E五种元素,它们的原子序数按E、C、D、A、B依次增大,E原子最外层有4个电子;A-与B+的核外电子排布相同;D的气态氢化物的化学式为H2D,最高价氧化物中D的质量分数为40%,且D原子核内质子数和中子数相等;C的原子序数比D少9,比B少12。
(1)写元素符号:A_____ ,B_____ ,C_______ ,D_______ ,E_______ 。
(2)画出A-、B+的结构示意图:_______ ,_______ 。
(3)D最高价氧化物对应的水化物化学式为____ ,C的气态氢化物的化学式为______ 。
(4)D、C最高价氧化物对应的水化物相互反应的离子方程式:_______ 。
(1)写元素符号:A
(2)画出A-、B+的结构示意图:
(3)D最高价氧化物对应的水化物化学式为
(4)D、C最高价氧化物对应的水化物相互反应的离子方程式:
您最近一年使用:0次
名校
解题方法
3 . 有A、B、C、D、E五种元素,它们可能是原子或离子,且为短周期元素,A与B可形成BA型化合物,且A元素是非金属性最强的元素。金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8个;C元素有三种同位素C1、C2、C3,自然界里含量最多的是C1,C3原子的质量数是C1的3倍,C2原子的质量数是C1的2倍。D的气态氢化物水溶液显碱性,而其最高价氧化物水化物为强酸。E元素原子的最外层电子数比次外层电子数多4个,E离子的核外电子数比质子数多2个。
(1)写出A元素名称:______ ,C2粒子的符号:______ 。
(2)画出E离子的结构示意图:______ ,E的氢化物的分子式______ 。
(3)写出B与E化合的化学方程式:______ 。
(4)写出A的单质、B的单质分别与水反应的溶液混合后发生的反应的离子方程式:______ 。
(5)A与C形成的化合物中含化学键类型是:______ ,用电子式表示该化合物:______ 。
(1)写出A元素名称:
(2)画出E离子的结构示意图:
(3)写出B与E化合的化学方程式:
(4)写出A的单质、B的单质分别与水反应的溶液混合后发生的反应的离子方程式:
(5)A与C形成的化合物中含化学键类型是:
您最近一年使用:0次
4 . 元素周期表是学习和研究化学的重要工具,下面是元素周期表的部分内容,请根据下表回答问题:
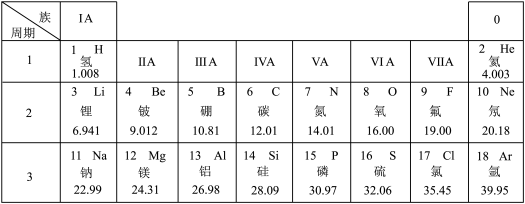
(1)发现了元素周期律并编制出元素周期表的化学家是___________(填字母)。
(2)氟元素是人体必需微量元素之一,能防治龋齿。氟元素的相对原子质量为___________ 。
(3)已知某微粒的结构示意图为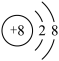 ,请写出该微粒的符号
,请写出该微粒的符号___________ 。
(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化学式为___________ 。

(1)发现了元素周期律并编制出元素周期表的化学家是___________(填字母)。
| A.门捷列夫 | B.拉瓦锡 | C.道尔顿 | D.阿伏加德罗 |
(3)已知某微粒的结构示意图为
 ,请写出该微粒的符号
,请写出该微粒的符号(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化学式为
您最近一年使用:0次
5 . 有A、B、C、D四种有机物,A、B属于烃类物质,C、D都是烃的衍生物。A是含氢质量分数最大的有机物,分子结构为正四面体;B的球棍模型为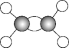 ;C的相对分子质量为46,能与Na反应,但不能与NaOH溶液反应;D的空间填充模型为
;C的相对分子质量为46,能与Na反应,但不能与NaOH溶液反应;D的空间填充模型为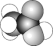 ,向该物质的水溶液中滴加紫色石蕊溶液,溶液变红色。请回答下列问题:
,向该物质的水溶液中滴加紫色石蕊溶液,溶液变红色。请回答下列问题:
(1)A的电子式是_______ ,C中官能团的名称是_______ 。
(2)B的结构简式是_______ ,该物质发生加聚反应的化学方程式为_______ 。
(3)已知B可以发生如图转化过程:
B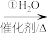 C
C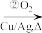 CH3CHO
CH3CHO 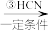
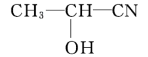
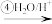
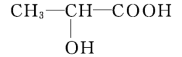
完成转化①、②反应的化学方程式:①_______ ;②_______ 。
 ;C的相对分子质量为46,能与Na反应,但不能与NaOH溶液反应;D的空间填充模型为
;C的相对分子质量为46,能与Na反应,但不能与NaOH溶液反应;D的空间填充模型为 ,向该物质的水溶液中滴加紫色石蕊溶液,溶液变红色。请回答下列问题:
,向该物质的水溶液中滴加紫色石蕊溶液,溶液变红色。请回答下列问题:(1)A的电子式是
(2)B的结构简式是
(3)已知B可以发生如图转化过程:
B
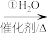 C
C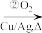 CH3CHO
CH3CHO 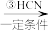

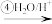
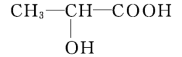
完成转化①、②反应的化学方程式:①
您最近一年使用:0次
解题方法
6 . 二氧化氯消毒剂是国际上公认的高效消毒灭菌剂,回答下列问题:
I.制备ClO2
实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:
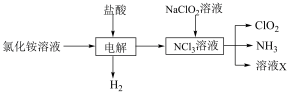
(1)NH4Cl的电子式为___________ 。
(2)若NaClO2与NCl3完全反应,则“溶液X”中的溶质为________ (填化学式)。
Ⅱ.NaClO2的应用
(3)NaClO2具有强氧化性,可将烟气中的NO氧化为NO ,在该反应过程中无有毒气体生成。其他条件相同时,以NaClO2溶液为吸收剂,测得相同时间内NO的氧化率随NaClO2的起始浓度的变化情况如图所示。
,在该反应过程中无有毒气体生成。其他条件相同时,以NaClO2溶液为吸收剂,测得相同时间内NO的氧化率随NaClO2的起始浓度的变化情况如图所示。
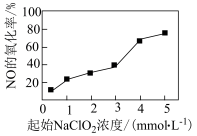
①NaClO2溶液在酸性条件下除去NO的离子方程式为___________ 。
②NO的氧化率随起始NaClO2浓度的增大而增大,原因是___________ 。
(4)ClO2具有较好的杀菌消毒作用。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克氯气的氧化能力。若ClO2的还原产物为Cl-,则ClO2的有效氯含量为___________ (保留2位小数)。
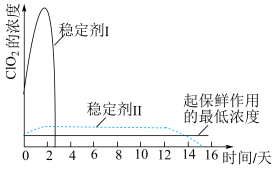
(5)ClO2能被多种稳定剂吸收,若将其用于果蔬保鲜,你认为下图中效果较好的稳定剂是___________ (填“稳定剂I”或“稳定剂Ⅱ”),原因是___________ 。
I.制备ClO2
实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:

(1)NH4Cl的电子式为
(2)若NaClO2与NCl3完全反应,则“溶液X”中的溶质为
Ⅱ.NaClO2的应用
(3)NaClO2具有强氧化性,可将烟气中的NO氧化为NO
 ,在该反应过程中无有毒气体生成。其他条件相同时,以NaClO2溶液为吸收剂,测得相同时间内NO的氧化率随NaClO2的起始浓度的变化情况如图所示。
,在该反应过程中无有毒气体生成。其他条件相同时,以NaClO2溶液为吸收剂,测得相同时间内NO的氧化率随NaClO2的起始浓度的变化情况如图所示。
①NaClO2溶液在酸性条件下除去NO的离子方程式为
②NO的氧化率随起始NaClO2浓度的增大而增大,原因是
(4)ClO2具有较好的杀菌消毒作用。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克氯气的氧化能力。若ClO2的还原产物为Cl-,则ClO2的有效氯含量为
(5)ClO2能被多种稳定剂吸收,若将其用于果蔬保鲜,你认为下图中效果较好的稳定剂是

您最近一年使用:0次
名校
解题方法
7 . 化学元素周期表(Periodictableofelements)是根据元素原子核电荷数从小至大排序的化学元素列表。如表是元素周期表的一部分,根据表中给出的10种元素(其中X、Y、Z分别表示某种化学元素),按要求作答。
(1)Z元素符号是___________ 。
(2)表中元素化学性质最稳定的是___________ (填元素符号)。
(3)地壳中含量最多的元素在元素周期表中的位置是___________ 。
(4)写出Na的原子结构示意图___________ 。
(5)主要用来制作高纯半导体、耐高温材料、光导纤维通信材料的元素名称是___________ 。
(6)卤族元素之一,属周期系VIIA族,在元素周期表中位于第二周期的元素是___________ 。
(7)O2与S单质相比,更难与H2化合的是___________ 。
(8)写出N元素的气态氢化物的化学式___________ ,该物质与水反应的化学方程式:___________ 。
(9)Cl2与水反应的生成物中具有漂白作用的是___________ (填化学式),写出Cl2与NaOH溶液反应的离子方程式:___________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | X | N | O | F | Y | |||
| 3 | Na | Z | Al | Si | S | Cl |
(2)表中元素化学性质最稳定的是
(3)地壳中含量最多的元素在元素周期表中的位置是
(4)写出Na的原子结构示意图
(5)主要用来制作高纯半导体、耐高温材料、光导纤维通信材料的元素名称是
(6)卤族元素之一,属周期系VIIA族,在元素周期表中位于第二周期的元素是
(7)O2与S单质相比,更难与H2化合的是
(8)写出N元素的气态氢化物的化学式
(9)Cl2与水反应的生成物中具有漂白作用的是
您最近一年使用:0次
解题方法
8 . A、B、C、D、E、F、G的原子序数依次增大的元素,A、D元素的原子最外层电子数相同,A元素的一种原子没有中子;B的一种同位素可用于考古断代;C是地壳中含量最多的一种元素;D元素的阳离子电子层结构与氖原子相同;E的最外层电子数是电子层数的2倍;F的单质具有强氧化性。G是用途最广泛的金属元素,它的单质能被磁铁所吸引;试回答以下问题:
(1)E的原子结构示意图:______ 。
(2)D单质与C单质在加热条件下反应产物的电子式________ ,该物质与A2C反应的离子方程式______ 。
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为______ 。
(4)用电子式写出A2C的形成过程________ 。
(1)E的原子结构示意图:
(2)D单质与C单质在加热条件下反应产物的电子式
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为
(4)用电子式写出A2C的形成过程
您最近一年使用:0次
名校
9 . 白藜芦醇( )广泛存在于葡萄、桑椹等植物果实中,它具有抗肿瘤、抗氧化、延缓衰老等功效。下列说法正确的是
)广泛存在于葡萄、桑椹等植物果实中,它具有抗肿瘤、抗氧化、延缓衰老等功效。下列说法正确的是
 )广泛存在于葡萄、桑椹等植物果实中,它具有抗肿瘤、抗氧化、延缓衰老等功效。下列说法正确的是
)广泛存在于葡萄、桑椹等植物果实中,它具有抗肿瘤、抗氧化、延缓衰老等功效。下列说法正确的是A.1个白藜芦醇分子中含有6个 分子和1个 分子和1个 分子 分子 |
| B.1个白藜芦醇分子是由14个碳元素、12个氢元素和3个氧元素组成的 |
C.白藜芦醇中C、H、O三种元素的质量比为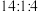 |
| D.白藜芦醇中氧元素的质量分数为48% |
您最近一年使用:0次
2022-09-07更新
|
128次组卷
|
2卷引用:山东省临沂市重点中学2022-2023学年高一上学期9月入学考试化学试题
名校
解题方法
10 . 人体必需的一些元素在周期表中的分布情况如下:______ 。 是一种绿色氧化剂,电子式为
是一种绿色氧化剂,电子式为________ 。
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将 通入水中,可以得到一种具有漂白性的分子,写出它的结构式
通入水中,可以得到一种具有漂白性的分子,写出它的结构式________ 。
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是________ ,原子序数为____ 。
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性 溶液中加入
溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为___________ 。
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_______(填字母)。

 是一种绿色氧化剂,电子式为
是一种绿色氧化剂,电子式为(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将
 通入水中,可以得到一种具有漂白性的分子,写出它的结构式
通入水中,可以得到一种具有漂白性的分子,写出它的结构式(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性
 溶液中加入
溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_______(填字母)。
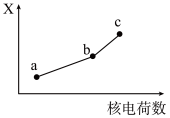
| A.若a、b、c表示氧族元素,则X表示对应氢化物的沸点 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第ⅠA族元素,则X表示对应离子的氧化性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
您最近一年使用:0次
2024-01-24更新
|
71次组卷
|
2卷引用:山东省邹城市第二中学2023-2024学年高一上学期12月月考化学试题



