解题方法
1 . 某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径≤2.5um的悬浮颗粒物,已知1μm=1×10-6m),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系___________ (填“属于"或“不属于)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为___________ (填“酸”或“碱”)性。
(3)洗涤含SO2的烟气,以下物质可作洗涤剂的是___________ (填字母)
a.Ca(OH)2 b.CaCl2 c.Na2CO3 d.NaHSO3
(4)硫酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产品用于制造石膏。脱硫反应的化学方程式为___________ 。
②某硫酸化工厂,使用一种含杂质为25%的黄铁矿石(FeS2)为原料。若取2吨该矿石,可制得98%的浓硫酸___________ 吨(假设生产过程中96%SO2转化为SO3)。
(1)PM2.5分散在空气中形成的分散系
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH | SO | NO | Cl- |
| 浓度/mol/L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(3)洗涤含SO2的烟气,以下物质可作洗涤剂的是
a.Ca(OH)2 b.CaCl2 c.Na2CO3 d.NaHSO3
(4)硫酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产品用于制造石膏。脱硫反应的化学方程式为
②某硫酸化工厂,使用一种含杂质为25%的黄铁矿石(FeS2)为原料。若取2吨该矿石,可制得98%的浓硫酸
您最近一年使用:0次
2 . 回答下列问题:
(1)在0.5molAl2(SO4)3中,所含铝离子的物质的量为_______ ,硫酸根离子的物质的量为_______ ,离子个数共有_______ 。
(2)两份物质的量相等的SO2和SO3,物质的量之比_______ ,所含硫原子的物质的量之比_______ ,所含氧原子数目之比为_______ 。
在标准状况下,物质①4gH2,②33.6LCH4,③1molH2O,④3.01×1023个O2。(填序号,下同)
(3)电子数最多的是_______ 。
(4)分子数最多的是_______ 。
(5)原子数最少的是_______ 。
(6)体积最小的是_______ 。
(1)在0.5molAl2(SO4)3中,所含铝离子的物质的量为
(2)两份物质的量相等的SO2和SO3,物质的量之比
在标准状况下,物质①4gH2,②33.6LCH4,③1molH2O,④3.01×1023个O2。(填序号,下同)
(3)电子数最多的是
(4)分子数最多的是
(5)原子数最少的是
(6)体积最小的是
您最近一年使用:0次
名校
解题方法
3 . 守恒是重要的科学原理,我们在学习化学的过程中接触过很多守恒:质量守恒、原子守恒、电子守恒、电荷守恒等。请回答以下问题:
(1)某溶液中只有 、
、 、
、 和
和 四种离子,已知
四种离子,已知 、
、 、
、 的物质的量浓度分别2mol/L、1mol/L、1mol/L,则
的物质的量浓度分别2mol/L、1mol/L、1mol/L,则 的物质的量浓度为
的物质的量浓度为___________ mol/L。
(2)同温同压下,某集气瓶充满 时为116g,充满
时为116g,充满 时为122g,充满气体A时为114g,则A的相对分子质量为
时为122g,充满气体A时为114g,则A的相对分子质量为___________ 。
(3)在浓盐酸中 与
与 反应的离子方程式为:
反应的离子方程式为: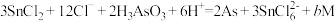 ,则b的数值为
,则b的数值为___________ 。
(4)在100mL 溶液中通入2.24L氯气(标准状况);溶液中有1/2的
溶液中通入2.24L氯气(标准状况);溶液中有1/2的 被氧化成单质
被氧化成单质 ,则原
,则原 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为___________ mol/L。
(5)已知:1mol 与一定浓度的
与一定浓度的 反应,生成
反应,生成 、
、 、NO和
、NO和 ,表现氧化性的硝酸的物质的量是
,表现氧化性的硝酸的物质的量是___________ mol。
(1)某溶液中只有
 、
、 、
、 和
和 四种离子,已知
四种离子,已知 、
、 、
、 的物质的量浓度分别2mol/L、1mol/L、1mol/L,则
的物质的量浓度分别2mol/L、1mol/L、1mol/L,则 的物质的量浓度为
的物质的量浓度为(2)同温同压下,某集气瓶充满
 时为116g,充满
时为116g,充满 时为122g,充满气体A时为114g,则A的相对分子质量为
时为122g,充满气体A时为114g,则A的相对分子质量为(3)在浓盐酸中
 与
与 反应的离子方程式为:
反应的离子方程式为: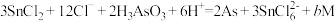 ,则b的数值为
,则b的数值为(4)在100mL
 溶液中通入2.24L氯气(标准状况);溶液中有1/2的
溶液中通入2.24L氯气(标准状况);溶液中有1/2的 被氧化成单质
被氧化成单质 ,则原
,则原 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为(5)已知:1mol
 与一定浓度的
与一定浓度的 反应,生成
反应,生成 、
、 、NO和
、NO和 ,表现氧化性的硝酸的物质的量是
,表现氧化性的硝酸的物质的量是
您最近一年使用:0次
名校
4 . 为了食品安全,我国禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。下列对于过氧化钙(CaO2)的叙述错误的是
| A.CaO2可以用作鱼池增氧剂 |
| B.CaO2中阴阳离子的个数比为1:2 |
| C.CaO2和水反应时,每消耗2molCaO2能生成22.4L气体 |
D.CaO2和CO2反应的化学方程式为: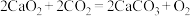 |
您最近一年使用:0次
5 . 下列说法正确的是(NA为阿伏加德罗常数)
| A.28g氮气含有的原子数为NA |
| B.4g金属钙变成钙离子时失去的电子数为0.2NA |
| C.0.2molO2、0.3molCO2、0.5molSO2的气体总体积约为22.4L |
| D.24gO2分子和24gO3分子所含的氧原子数目相等 |
您最近一年使用:0次
名校
6 . 下列关于阿伏伽德罗常数(NA)的说法错误的是
A.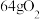 所含的分子数目为2NA 所含的分子数目为2NA |
B.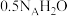 含有的原子数目约为 含有的原子数目约为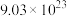 个 个 |
| C.1molNaCl含有的离子数目为2NA |
| D.NA个氦气分子的物质的量是0.5mol |
您最近一年使用:0次
名校
解题方法
7 . 《环境科学》刊发了我国科研部门采用零价铁活化过硫酸钠( ,其中S为+6价)去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示。设阿伏加德罗常数的值为
,其中S为+6价)去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示。设阿伏加德罗常数的值为 ,
,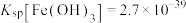 。下列叙述正确的是
。下列叙述正确的是
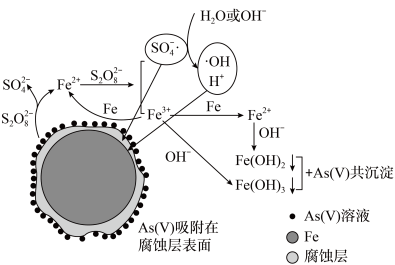
A.1 mol过硫酸钠( )含 )含 个过氧键 个过氧键 |
B.若56 g Fe参加反应,共有 个 个 被还原 被还原 |
C.室温下,中间产物 溶于水所得饱和溶液中 溶于水所得饱和溶液中 为 为 mol⋅L mol⋅L |
| D.pH越小,越有利于去除废水中的正五价砷 |
您最近一年使用:0次
名校
解题方法
8 . 乙炔水化法、乙烯氧化法是工业上制备乙醛的两个重要方法,反应原理分别为: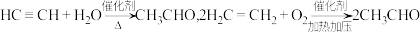 。以下叙述不正确的是
。以下叙述不正确的是
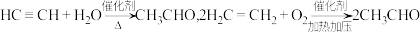 。以下叙述不正确的是
。以下叙述不正确的是A. 的电子式为 的电子式为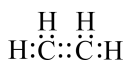 |
| B.根据价层电子互斥模型,18g水的中心原子含有2mol孤电子对 |
C.乙烯氧化法中,生成0.1mol乙醛时,转移的电子数约为 |
D.标准状况下,11.2L 中含有π键的数目约为 中含有π键的数目约为 |
您最近一年使用:0次
2024-03-31更新
|
148次组卷
|
2卷引用:山东省德州市第一中学2023-2024学年高二下学期3月月考化学试题
解题方法
9 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.100 mL 1 mol/LCuSO4溶液中含有氧原子的数目为0.4NA |
| B.0.3 mol/LMgCl2溶液中Cl-的数目为0.6NA |
| C.标准状况下,22.4 L CO和N2混合气体中所含原子的数目为2NA |
| D.11.8 g金属R与足量盐酸反应生成RCl2并放出0.4 g H2,则M(R)=118 g/mol |
您最近一年使用:0次
10 . 设NA表示阿伏加 德罗常数的值。回答下列问题:
(1)0.3molNH3分子中所含原子数与___________ 个H2O分子中所含原子数相等。
(2)含0.4molAl3+的Al2(SO4)3中所含的SO 的物质的量是
的物质的量是___________ 。
(3)等物质的量O2和臭氧(O3),其质量之比为___________ 。若O2和O3质量相等,则其原子数之比为___________ 。
(4)1.5molH2SO4的质量是___________ ,其中含有___________ molH,含有___________ g氧元素。
(5)9.03×1023个NH3分子含___________ mol氨分子,___________ mol氮原子,___________ 个氢原子。
(1)0.3molNH3分子中所含原子数与
(2)含0.4molAl3+的Al2(SO4)3中所含的SO
 的物质的量是
的物质的量是(3)等物质的量O2和臭氧(O3),其质量之比为
(4)1.5molH2SO4的质量是
(5)9.03×1023个NH3分子含
您最近一年使用:0次



