1 . 用 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.标准状况下,11.2L  含有的分子数为 含有的分子数为 |
B.常温常压下,3.2g  与 与 混合气体,含有的氧原子数目为 混合气体,含有的氧原子数目为 |
C.1L 1mol/L的 溶液中,含有的离子总数为 溶液中,含有的离子总数为 |
D.标准状况下,2.24L  与钠反应,转移的电子数一定为 与钠反应,转移的电子数一定为 |
您最近一年使用:0次
2023-07-29更新
|
296次组卷
|
3卷引用:陕西省西安铁一中学2023-2024学年高一上学期期末考试化学试题
名校
解题方法
2 . 研究小组以 (绿色固体)、
(绿色固体)、 、THF(四氯呋喃,液体)等物质为原料制备固体配合物
、THF(四氯呋喃,液体)等物质为原料制备固体配合物 ,该配合物可作为有机反应的催化剂
,该配合物可作为有机反应的催化剂
(1)无水 (紫色固体,易升华)的制备装置如图所示(夹持装置略)。
(紫色固体,易升华)的制备装置如图所示(夹持装置略)。

①仪器a的名称为________ 。
②本实验持续通入 的目的有赶走体系中原有的空气、
的目的有赶走体系中原有的空气、________ 。
③反应管的温度升到660℃时发生反应,生成 和
和 (光气),其化学方程式为
(光气),其化学方程式为________ 。 有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是
有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是________ (填化学式)。
④反应管右端有15cm在加热炉外,其作用是________________ 。
(2) 的合成装置如图所示(搅拌和夹持装置咯)
的合成装置如图所示(搅拌和夹持装置咯)

将制备的无水 和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为
和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为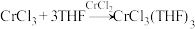 。
。
实验时烧瓶中THF受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与滤纸套筒内的物质接触。当液面达到虹吸管3顶端时,经虹吸管3返回双颈烧瓶.从而实现了THF与 的连续反应及产物的连续萃取。
的连续反应及产物的连续萃取。
①锌粉的作用是________________ (用化学方程式表示)。
② 和
和 在THF的溶解性分别为
在THF的溶解性分别为________ 、________ (填“溶”或“不溶”)。
③合成反应完成后,取下双颈烧瓶,蒸发THF得到固体产品6.7410g。则该实验的产率为________ %。[已知: 的摩尔质量为152g/mol;
的摩尔质量为152g/mol; 的摩尔质量为374.5g/mol]
的摩尔质量为374.5g/mol]
 (绿色固体)、
(绿色固体)、 、THF(四氯呋喃,液体)等物质为原料制备固体配合物
、THF(四氯呋喃,液体)等物质为原料制备固体配合物 ,该配合物可作为有机反应的催化剂
,该配合物可作为有机反应的催化剂(1)无水
 (紫色固体,易升华)的制备装置如图所示(夹持装置略)。
(紫色固体,易升华)的制备装置如图所示(夹持装置略)。
①仪器a的名称为
②本实验持续通入
 的目的有赶走体系中原有的空气、
的目的有赶走体系中原有的空气、③反应管的温度升到660℃时发生反应,生成
 和
和 (光气),其化学方程式为
(光气),其化学方程式为 有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是
有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是④反应管右端有15cm在加热炉外,其作用是
(2)
 的合成装置如图所示(搅拌和夹持装置咯)
的合成装置如图所示(搅拌和夹持装置咯)
将制备的无水
 和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为
和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为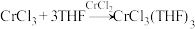 。
。实验时烧瓶中THF受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与滤纸套筒内的物质接触。当液面达到虹吸管3顶端时,经虹吸管3返回双颈烧瓶.从而实现了THF与
 的连续反应及产物的连续萃取。
的连续反应及产物的连续萃取。①锌粉的作用是
②
 和
和 在THF的溶解性分别为
在THF的溶解性分别为③合成反应完成后,取下双颈烧瓶,蒸发THF得到固体产品6.7410g。则该实验的产率为
 的摩尔质量为152g/mol;
的摩尔质量为152g/mol; 的摩尔质量为374.5g/mol]
的摩尔质量为374.5g/mol]
您最近一年使用:0次
2023-03-14更新
|
700次组卷
|
4卷引用:2024届陕西省西安中学高三下学期三模理综试题-高中化学
解题方法
3 . 下列说法正确的是
A.1mol氢约含有 个氢 个氢 |
B.22g二氧化碳含有的氧原子数约等于 |
| C.当质量以克为单位时,钠的摩尔质量在数值上等于它的相对原子质量 |
D. 的摩尔质量是46g 的摩尔质量是46g |
您最近一年使用:0次
2022-11-11更新
|
187次组卷
|
2卷引用:陕西省商洛市2023-2024学年洛南中学高一(上)期末化学模拟试卷
名校
4 . 向100mLFe2(SO4)3和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量关系如图所示。忽略溶液体积的变化,下列说法错误的是
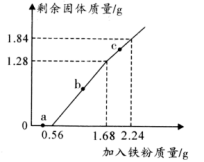
| A.a点时溶液中的阳离子为Cu2+、Fe2+和Fe3+ |
B.c点时溶液中发生的反应为: |
| C.c点时溶液中溶质的物质的量浓度为0.5mol/L |
D.原溶液中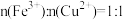 |
您最近一年使用:0次
2021-12-29更新
|
269次组卷
|
4卷引用:陕西省汉中市九校联盟2023-2024学年高一上学期1月期末化学试题
名校
5 . (1)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为___ 。
(2)在25℃、101kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为____ 。
(3)VL Al2(SO4)3溶液中含Al3+ag,将此溶液稀释到4VL,则稀释后溶液中SO 的物质的量浓度是
的物质的量浓度是___ 。
(2)在25℃、101kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为
(3)VL Al2(SO4)3溶液中含Al3+ag,将此溶液稀释到4VL,则稀释后溶液中SO
 的物质的量浓度是
的物质的量浓度是
您最近一年使用:0次
2020-11-24更新
|
354次组卷
|
3卷引用:陕西省宝鸡市渭滨区2023-2024学年高一上学期期末考试化学试题
陕西省宝鸡市渭滨区2023-2024学年高一上学期期末考试化学试题山东省济南市第一中学2020-2021学年高一上学期期中考试化学试题(已下线)第二章 海水中的重要元素——钠和氯(A卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)



