1 . 用 溶液处理火箭发射场附近废水中偏二甲肼
溶液处理火箭发射场附近废水中偏二甲肼 的反应原理为
的反应原理为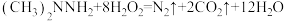 ,NA为阿伏加德罗常数的值。下列说法正确的是
,NA为阿伏加德罗常数的值。下列说法正确的是
 溶液处理火箭发射场附近废水中偏二甲肼
溶液处理火箭发射场附近废水中偏二甲肼 的反应原理为
的反应原理为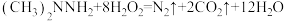 ,NA为阿伏加德罗常数的值。下列说法正确的是
,NA为阿伏加德罗常数的值。下列说法正确的是A.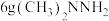 中所含氮原子数目为0.4NA 中所含氮原子数目为0.4NA |
B.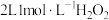 溶液中氧原子数目为4NA 溶液中氧原子数目为4NA |
C.标准状况下,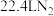 中孤电子对数目为2NA 中孤电子对数目为2NA |
D.反应生成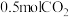 时转移电子数目为2NA 时转移电子数目为2NA |
您最近一年使用:0次
名校
解题方法
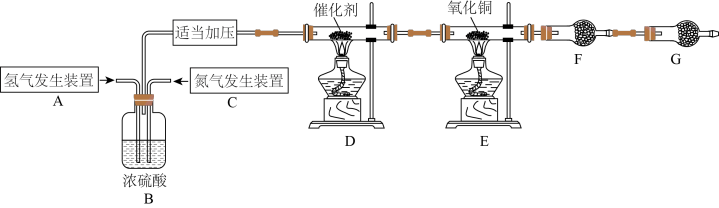
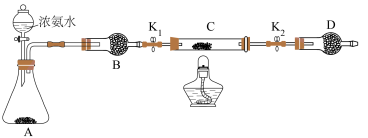
2 . 某学习小组根据氨气还原氧化铜的反应,设计实验测定铜元素相对原子质量Ar(Cu)(近似值)。甲同学模拟合成氨工业制备氨气,反应前先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),由此计算Ar(Cu)。装置图如下: 。请回答下列问题:
。请回答下列问题:
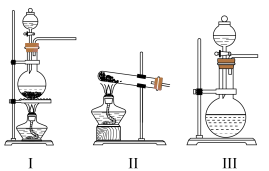
(1)C装置应选用______ (填“Ⅰ”“Ⅱ”或“Ⅲ”)。
(2)装置B的作用是:①使气体混合均匀;②______ ;③______ 。
(3)氨气还原炽热氧化铜(产物之一为空气中含量最多的气体)化学方程式为____________________ 。
(4)干燥管F中盛放的干燥剂为______(填字母代号)。
(5)G装置的作用是①______ ;②______ 。
若没有G装置,测得结果Ar(Cu)______ (填“偏大”“偏小”或“无影响”)。
(6)乙同学认为上述装置操作麻烦,对原装置改进,新装置如图所示。实验前将石英玻璃管(带两端开关K1和K2)(设为装置C)称重,记为m1 g。将氧化铜装入石英玻璃管中,再次将装置C称重,记为m2 g。按下图连接好装置进行实验,通入NH3,充分反应直至C恒重,记为m3 g。______ (填化学式)
②根据实验记录,计算铜元素相对原子质量Ar(Cu)=______ (用含有m1、m2、m3的式子表示)。
 。请回答下列问题:
。请回答下列问题:(1)C装置应选用
(2)装置B的作用是:①使气体混合均匀;②
(3)氨气还原炽热氧化铜(产物之一为空气中含量最多的气体)化学方程式为
(4)干燥管F中盛放的干燥剂为______(填字母代号)。
| A.五氧化二磷 | B.无水CuSO4 | C.碱石灰 | D.无水CaCl2 |
(5)G装置的作用是①
若没有G装置,测得结果Ar(Cu)
(6)乙同学认为上述装置操作麻烦,对原装置改进,新装置如图所示。实验前将石英玻璃管(带两端开关K1和K2)(设为装置C)称重,记为m1 g。将氧化铜装入石英玻璃管中,再次将装置C称重,记为m2 g。按下图连接好装置进行实验,通入NH3,充分反应直至C恒重,记为m3 g。
②根据实验记录,计算铜元素相对原子质量Ar(Cu)=
您最近一年使用:0次
2024-03-12更新
|
587次组卷
|
5卷引用:湖北省云学名校联盟2023-2024学年高一下学期3月联考化学试卷
3 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A. 熔融的 熔融的 中含有 中含有 个阳离子 个阳离子 |
B.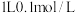 氢硫酸溶液中 氢硫酸溶液中 数目为 数目为 |
C.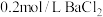 溶液中含有的 溶液中含有的 数目为 数目为 |
D.常温常压下,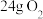 和 和 的混合物含有 的混合物含有 个氧原子 个氧原子 |
您最近一年使用:0次
4 . 有一质量为11.76g的Fe、CuO、Fe2O3混合固体,完全溶解在200mL2mol/L稀盐酸中,然后向溶液中加铁粉,剩余固体质量与加入铁粉质量的关系如图所示。下列说法正确的是


| A.0~m1阶段发生反应为Fe+2H+=Fe2++H2↑ |
B.混合固体中 的质量为0.01mol 的质量为0.01mol |
| C.5.04~m2阶段发生反应为2Fe3++Fe=3Fe2+ |
| D.图中m2=5.6 |
您最近一年使用:0次
名校
5 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.Cl2分子中含有的共价键数目为NA |
| B.0.1 mol FeCl3完全水解可得Fe(OH)3胶粒的数目为NA |
| C.标准状况下,22.4 L O2与22.4 L HF含分子数均为NA |
| D.7.8 g Na2O2与足量水反应转移电子数目为0.1NA |
您最近一年使用:0次
6 . 设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.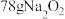 与足量 与足量 反应,转移的电子数为 反应,转移的电子数为 |
B.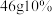 的乙醇溶液中,含分子数为 的乙醇溶液中,含分子数为 |
C.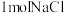 中含有的 中含有的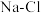 键数为 键数为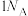 |
D.等质量的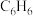 和 和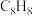 中含有的C原子数均为 中含有的C原子数均为 |
您最近一年使用:0次
2024-02-24更新
|
118次组卷
|
2卷引用:湖北省新高考联考协作体2023-2024学年高二下学期2月收心考试化学试题
名校
7 . 设 表示阿伏加德罗常数值,下列叙述正确的是
表示阿伏加德罗常数值,下列叙述正确的是
 表示阿伏加德罗常数值,下列叙述正确的是
表示阿伏加德罗常数值,下列叙述正确的是A.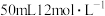 浓盐酸与足量 浓盐酸与足量 共热,转移的电子数目为 共热,转移的电子数目为 |
B.标准状况下,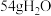 中含有分子数为 中含有分子数为 个 个 |
C.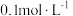 的硫酸铝溶液所含的硫酸根离子的数目就是 的硫酸铝溶液所含的硫酸根离子的数目就是 |
D.在溶有 的胶体中,含有 的胶体中,含有 个 个 胶粒 胶粒 |
您最近一年使用:0次
2024-02-18更新
|
48次组卷
|
2卷引用:湖北省部分县市区省级示范高中温德克英协作体2023-2024学年高二上学期期末综合性调研考试化学试题
8 . 用表示阿伏加德罗常数的值.下列叙述正确的有
A.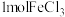 与水完全反应形成的胶体中含有 与水完全反应形成的胶体中含有 个 个 胶体粒子 胶体粒子 |
B.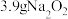 固体所含阴离子数为 固体所含阴离子数为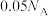 |
C.将 通过 通过 使其增重 使其增重 ,反应中转移的电子数为 ,反应中转移的电子数为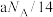 |
D.常温下, 氦气所含的原子数目为 氦气所含的原子数目为 |
您最近一年使用:0次
9 . 物质的量在定量计算中有重要应用,设 是阿伏加德罗常数的值。下列说法正确的是
是阿伏加德罗常数的值。下列说法正确的是
 是阿伏加德罗常数的值。下列说法正确的是
是阿伏加德罗常数的值。下列说法正确的是A.0.5moL/L 溶液中含有 溶液中含有 个 个 |
B.标准状况下,等体积的 和 和 所含的分子数均为 所含的分子数均为 |
C.同温同压下,等质量的CO与 的体积之比为11:7 的体积之比为11:7 |
| D.将5.85gNaCl固体完全溶于1L水中,所得c(NaCl)为0.1mol/L |
您最近一年使用:0次
名校
10 . 用 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.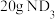 溶于水形成的氨水中质子数约为 溶于水形成的氨水中质子数约为 |
B.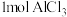 完全水解生成的 完全水解生成的 胶体粒子数目为 胶体粒子数目为 |
C.高温下,铁粉与水蒸气反应,固体的质量增加 ,则转移电子数目为 ,则转移电子数目为 |
D.质量分数为46%的乙醇水溶液中所含氢原子数为 |
您最近一年使用:0次
2023-11-11更新
|
648次组卷
|
4卷引用:湖北省黄冈市蕲春县实验高级中学2024届高三一轮复习10月月考化学试题
湖北省黄冈市蕲春县实验高级中学2024届高三一轮复习10月月考化学试题(已下线)题型02 阿伏加德罗常数的判断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)黑龙江省龙东五地市2023-2024学年高三上学期期中考试化学试题黑龙江省齐齐哈尔市普高联谊校2023-2024学年高三上学期11月月考化学试题



