1 . 设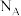 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
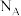 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.1mol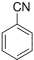 最多消耗 最多消耗 的个数为 的个数为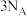 |
B.25℃,101kPa下,44.8LCO和 的混合气体的分子数等于 的混合气体的分子数等于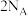 |
| C.80gNaOH溶解在1L水中,所得溶液中溶质的物质的量浓度是2mol/L |
D.铅酸蓄电池的正极质量增加3.2g时,电路中通过的电子数目为 |
您最近半年使用:0次
2 . 《天工开物》记载:“凡火药以硝石、硫磺为主,草木灰为辅……而后火药成声”,涉及的主要反应为 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,22.4 L  中含有的π键数为 中含有的π键数为 |
B.1 mol  分子中的电子总数为 分子中的电子总数为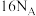 |
C.常温下,1 mol⋅L  溶液中 溶液中 数为 数为 |
D.12 g C完全反应转移电子数为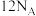 |
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
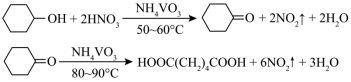
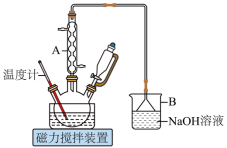
3 . 1,6己二酸是常用的化工原料,在高分子材料、医药、润滑剂的制造等方面都有重要作用。实验室利用图中的装置(夹持装置已省略),以环己醇和硝酸为反应物制备1,6己二酸。反应原理为:
实验步骤如下:
Ⅰ.向三颈烧瓶中加入0.03gNH4VO3固体和18mL浓HNO3(略过量),向恒压滴液漏斗中加入6mL环己醇
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇。调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕
Ⅲ.将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,___________,干燥,得到粗产品
Ⅳ.1,6-己二酸粗产品的提纯
(1)将步骤Ⅲ补充完整:_______ 。步骤Ⅳ提纯方法的名称为_______ 。如图为1,6己二酸在水中的溶解度曲线,80℃时1,6-己二酸水溶液的密度为ρg·mL-1;该溶液的物质的量浓度为_______ 。
| 试剂 | 相对分子质量 | 密度/(g·mL-1) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 环己醇 | 100 | 0.962 | 25.9 | 161.8 | 可溶于水、乙醇、乙醚 |
| 1,6-己二酸 | 146 | 1.360 | 152 | 330.5 | 微溶于冷水,易溶于乙醇 |
| NH4VO3 | 117 | 2.326 | 210(分解) | — | 微溶于冷水,易溶于热水 |
Ⅰ.向三颈烧瓶中加入0.03gNH4VO3固体和18mL浓HNO3(略过量),向恒压滴液漏斗中加入6mL环己醇
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇。调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕
Ⅲ.将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,___________,干燥,得到粗产品
Ⅳ.1,6-己二酸粗产品的提纯
(1)将步骤Ⅲ补充完整:

| A.46.07% | B.57.08% | C.63.03% | D.74.61% |
您最近半年使用:0次
4 . 在标准状况下,将336LHCl气体溶解于1L水中,所得盐酸溶液的密度为1.18g/cm3.试计算这种盐酸溶液中溶质的物质的量浓度为___________ 。
您最近半年使用:0次
5 . CO与H2S反应可以制得COS,其化学方程式为 。NA为阿伏加德罗常数的值,下列有关说法正确的是
。NA为阿伏加德罗常数的值,下列有关说法正确的是
 。NA为阿伏加德罗常数的值,下列有关说法正确的是
。NA为阿伏加德罗常数的值,下列有关说法正确的是A.2.8g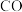 中含有的中子数为1.4NA 中含有的中子数为1.4NA |
B.pH=3的H2S溶液中 的数目为0.001NA 的数目为0.001NA |
C.0.1molCOS中 键数目为0.4NA 键数目为0.4NA |
| D.生成2.24LH2(标准状况),转移电子数目为0.4NA |
您最近半年使用:0次
6 .  为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.标准状况下, 完全反应,转移电子数目一定为 完全反应,转移电子数目一定为 |
B.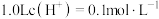 的 的 溶液中 溶液中 的数目为 的数目为 |
C.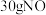 与 与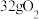 混合后所含原子总数小于 混合后所含原子总数小于 |
D.若核反应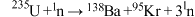 ( (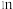 为中子)体系内中子增加 为中子)体系内中子增加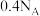 ,则消耗 ,则消耗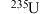 质量为 质量为 |
您最近半年使用:0次
7 .  为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.100g46%的乙醇溶液中含有O-H键的数目为 |
B.标准状况下,11.2LHF中电子的数目为 |
C.pH=1的 溶液中 溶液中 的数目为 的数目为 |
D.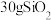 中含有的Si-O键数目为 中含有的Si-O键数目为 |
您最近半年使用:0次
解题方法
8 . 室温下,将0.05molNaHCO3固体溶于水配成100mL溶液,向溶液中加入下列物质,结论错误的是
| 选项 | 加入的物质 | 结论 |
| A | 50mL H2SO4溶液 H2SO4溶液 | 反应结束后, |
| B | 0.025molNa2O | 溶液中 增大 增大 |
| C | 50mL Ba(OH)2溶液 Ba(OH)2溶液 | 离子方程式为 |
| D | 0.05molNa2CO3固体 | 溶液中部分离子浓度关系: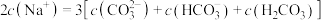 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.标准状况下,22.4L 中分子的数目为 中分子的数目为 |
B.1L 的水溶液中所含原子的数目为 的水溶液中所含原子的数目为 |
C.电解足量饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为 |
D.1mol 和 和 的混合气体中所含碳原子的数目为 的混合气体中所含碳原子的数目为 |
您最近半年使用:0次
10 . 请按要求填空:
(1)12.4g Na2X含有0.4mol Na+,Na2X的摩尔质量为___________ 。
(2)相同状况下,一定体积的气态氢化物H2X的质量是等体积NH3的2倍。则X的相对原子质量为___________ 。
(3)气态化合物A的化学式可以表示为OxFy,已知同温同压下10mL A受热完全分解生成15mL O2和10mL F2,则A的化学式为___________ 。
(4)0.5L 0.5mol/L FeCl3溶液中的Cl-的物质的量浓度为___________ 。
(5)质量分数为98%,密度为1.84g·cm-3的某浓硫酸,溶质的物质的量浓度为___________ 。
(6)a个X原子的总质量为b g,则X的相对原子质量可表示为___________ 。
(1)12.4g Na2X含有0.4mol Na+,Na2X的摩尔质量为
(2)相同状况下,一定体积的气态氢化物H2X的质量是等体积NH3的2倍。则X的相对原子质量为
(3)气态化合物A的化学式可以表示为OxFy,已知同温同压下10mL A受热完全分解生成15mL O2和10mL F2,则A的化学式为
(4)0.5L 0.5mol/L FeCl3溶液中的Cl-的物质的量浓度为
(5)质量分数为98%,密度为1.84g·cm-3的某浓硫酸,溶质的物质的量浓度为
(6)a个X原子的总质量为b g,则X的相对原子质量可表示为
您最近半年使用:0次



