名校
解题方法
1 . 黄铜灰渣(含有Cu、Zn、CuO、ZnO及少量FeO、Fe3O4、Fe2O3)生产 溶液的流程如下图所示:
溶液的流程如下图所示:
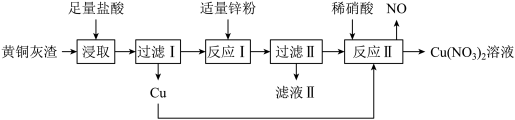
(1)写出“浸取”时Fe3O4反应的离子方程式:_______ 。
(2)过滤Ⅰ后所得滤液中是否含Fe3+,并说明理由:_______ 。
(3)检验“滤液Ⅱ”中由铁元素形成的阳离子的方法是_______ 。
(4)“反应Ⅱ”所用稀硝酸可由质量分数为63%、密度为1.40g·cm-3的浓硝酸稀释获得。
①若要获得100mL1.4mol·L-1的稀硝酸,需要用到浓硝酸的体积为_______ mL。
②NO是一种无色气体,依据信息写出“反应Ⅱ”的化学方程式:_______ 。
 溶液的流程如下图所示:
溶液的流程如下图所示:
(1)写出“浸取”时Fe3O4反应的离子方程式:
(2)过滤Ⅰ后所得滤液中是否含Fe3+,并说明理由:
(3)检验“滤液Ⅱ”中由铁元素形成的阳离子的方法是
(4)“反应Ⅱ”所用稀硝酸可由质量分数为63%、密度为1.40g·cm-3的浓硝酸稀释获得。
①若要获得100mL1.4mol·L-1的稀硝酸,需要用到浓硝酸的体积为
②NO是一种无色气体,依据信息写出“反应Ⅱ”的化学方程式:
您最近一年使用:0次
2022-12-22更新
|
277次组卷
|
4卷引用:黑龙江省 牡丹江市第一高级中学2023-2024学年高一上学期12月月考化学试题
黑龙江省 牡丹江市第一高级中学2023-2024学年高一上学期12月月考化学试题(已下线)江苏省南通市如皋市2022-2023学年高一上学期期中教学质量调研化学试题江苏省盐城市射阳县第二中学2022-2023学年高一上学期11月期中考试化学试题河南省顶级名校2023-2024学年高一上学期12月月考化学试题
名校
2 . 下列说法不正确的是
A.VL  溶液中含 溶液中含 mg,则溶液中 mg,则溶液中 的物质的量浓度为 的物质的量浓度为 |
B.某盐酸密度为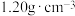 ,质量分数为36.5%,此盐酸物质的量浓度为 ,质量分数为36.5%,此盐酸物质的量浓度为 |
| C.将30%的氨水和10%的氨水等体积混合后,所得溶液的质量分数小于20%(已知氨水的浓度越大,其密度越小) |
D.100g浓度为 的硫酸中加入一定的水稀释成 的硫酸中加入一定的水稀释成 ,则加入水的体积大于100mL(已知硫酸的浓度越大,其密度越大) ,则加入水的体积大于100mL(已知硫酸的浓度越大,其密度越大) |
您最近一年使用:0次
2022-11-30更新
|
482次组卷
|
4卷引用:黑龙江省哈尔滨市第三中学2022-2023学年高一上学期第二次阶段性考试化学试题
名校
3 . Ⅰ.完成下列问题
(1)市售浓盐酸的密度为1.180 g/mL,物质的量浓度为 11.64 mol/L,此浓盐酸的质量分数为_______ ;若将100g此盐酸加水稀释至5.82mol/L,则加入水的质量_______ 100g。(填“大于”、“等于”或“小于”);
Ⅱ.某同学在实验室中用此浓盐酸与MnO2为原料制取纯净干燥的Cl2,装置如下图:
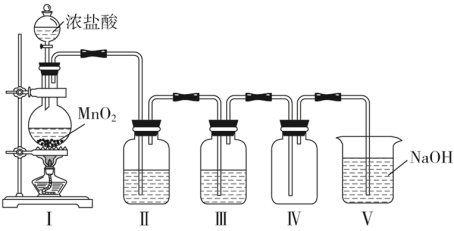
(2)装置Ⅰ中盛装浓盐酸的仪器名称为_______ ;圆底烧瓶中发生反应的离子方程式为_______ ;此反应中HCl体现出性质有_______ 和 _______ 。若生成标准状况下22.4L Cl2,被氧化的HCl分子数是_______ 。
(3)Ⅱ和Ⅲ中盛装的试剂分别是_______ 和_______ 。
(4)氯气的水溶液为氯水,Cl2与H2O反应的离子方程式为_______ ;
(5)如图是数字化实验得到的光照过程中氯水的pH变化情况。对此,下列有关说法正确的是_______
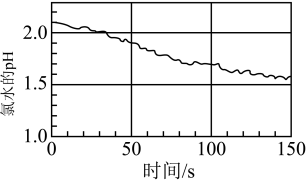
(6)装置Ⅴ中NaOH溶液的作用是吸收尾气,其中发生反应的化学方程式为 _______ 。
(1)市售浓盐酸的密度为1.180 g/mL,物质的量浓度为 11.64 mol/L,此浓盐酸的质量分数为
Ⅱ.某同学在实验室中用此浓盐酸与MnO2为原料制取纯净干燥的Cl2,装置如下图:

(2)装置Ⅰ中盛装浓盐酸的仪器名称为
(3)Ⅱ和Ⅲ中盛装的试剂分别是
(4)氯气的水溶液为氯水,Cl2与H2O反应的离子方程式为
(5)如图是数字化实验得到的光照过程中氯水的pH变化情况。对此,下列有关说法正确的是_______

| A.光照使氯水中的次氯酸分解为盐酸,溶液的酸性增强 |
| B.随着对氯水光照时间的延长,氯水的漂白性将增强 |
| C.随着对氯水光照时间的延长,溶液中Cl-的浓度不断减小 |
| D.随着对氯水光照时间的延长,氯水颜色逐渐变浅 |
您最近一年使用:0次
解题方法
4 . 实验室用14mol/L浓硫酸配制90mL 2.0 mol/L稀硫酸。
(1)量筒量取浓硫酸的体积约是_______ mL。
(2)选用容量瓶的规格是_______(填字母)。
(3)除了上题的容量瓶外,该实验还需要的玻璃仪器有量筒、烧杯、_____ 。
(4)容量瓶上标有_______(填字母,下同)。
①温度 ②浓度 ③容积 ④压强 ⑤刻度线
(5)下列操作会导致所得溶液浓度偏低的是_______。
(1)量筒量取浓硫酸的体积约是
(2)选用容量瓶的规格是_______(填字母)。
| A.50 mL | B.100 mL | C.250 mL | D.500 mL |
(4)容量瓶上标有_______(填字母,下同)。
①温度 ②浓度 ③容积 ④压强 ⑤刻度线
| A.①③⑤ | B.①③④ | C.②④ | D.②④⑤ |
| A.配制中未用蒸馏水洗涤烧杯和玻璃棒 |
| B.定容时俯视容量瓶刻度线 |
| C.稀释后未冷却至室温即转移至容量瓶 |
| D.摇匀后发现液面低于刻度线再加水 |
您最近一年使用:0次
名校
解题方法
5 . 正确的表示和计算溶液的组成和浓度,对生产生活有非常的重要意义,下列关于溶液浓度的说法中正确的是
| A.将1L0.5mol·L-1的盐酸加热浓缩为0.5L,此时盐酸浓度小于1mol·L-1 |
| B.将40g氢氧化钠溶于1L水中,可配制1mol/L的氢氧化钠溶液 |
C.将agNH3完全溶于水,得到VmL溶液,假设该溶液的密度为ρg/mL,溶质的物质的量浓度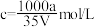 |
D.Al2(SO4)3溶液中含Al3+物质的量浓度为amol·L-1,取0.5VmL溶液稀释到5VmL,则稀释后溶液中SO 的物质的量浓度是0.3amol·L-1 的物质的量浓度是0.3amol·L-1 |
您最近一年使用:0次



