名校
解题方法
1 . 下列离子反应方程式正确的是( )
①稀盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑
②碳酸镁与稀硫酸:MgCO3+2H+=H2O+CO2↑+Mg2+
③碳酸氢钙溶液中加入少量氢氧化钠溶液:Ca2++HCO +OH-=CaCO3↓+H2O
+OH-=CaCO3↓+H2O
④向 溶液中逐滴加入
溶液中逐滴加入 溶液至
溶液至 刚好沉淀完全:H++SO
刚好沉淀完全:H++SO +Ba2++OH-=H2O+BaSO4↓
+Ba2++OH-=H2O+BaSO4↓
⑤向 溶液中滴加
溶液中滴加 溶液至溶液呈中性:2H++SO
溶液至溶液呈中性:2H++SO +Ba2++2OH-=2H2O+BaSO4↓
+Ba2++2OH-=2H2O+BaSO4↓
⑥向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO +OH-=CaCO3↓+H2O。
+OH-=CaCO3↓+H2O。
①稀盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑
②碳酸镁与稀硫酸:MgCO3+2H+=H2O+CO2↑+Mg2+
③碳酸氢钙溶液中加入少量氢氧化钠溶液:Ca2++HCO
 +OH-=CaCO3↓+H2O
+OH-=CaCO3↓+H2O④向
 溶液中逐滴加入
溶液中逐滴加入 溶液至
溶液至 刚好沉淀完全:H++SO
刚好沉淀完全:H++SO +Ba2++OH-=H2O+BaSO4↓
+Ba2++OH-=H2O+BaSO4↓⑤向
 溶液中滴加
溶液中滴加 溶液至溶液呈中性:2H++SO
溶液至溶液呈中性:2H++SO +Ba2++2OH-=2H2O+BaSO4↓
+Ba2++2OH-=2H2O+BaSO4↓⑥向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO
 +OH-=CaCO3↓+H2O。
+OH-=CaCO3↓+H2O。| A.①②③④ | B.②③④⑤ | C.③④⑤⑥ | D.①②③⑤ |
您最近一年使用:0次
2020-10-16更新
|
2773次组卷
|
10卷引用:天津一中2019-2020学年高一上学期期中化学试题
天津一中2019-2020学年高一上学期期中化学试题山西大学附属中学2017-2018学年高一上学期11月期中考试化学试题【全国百强校】黑龙江省双鸭山市第一中学2018-2019学年高一上学期期中考试化学试题河北省张家口市宣化区宣化第一中学2020-2021学年高一上学期10月月考化学试题(已下线)【浙江新东方】HZOMO化学003第二节 离子反应 第2课时 离子反应及其发生条件广东省广州市真光中学2022-2023学年高一上学期阶段测试化学试题湖北省武汉市第十一高级中学2021-2022高一上学期10月月考化学试题河南省安阳市第一中学2022-2023学年高一上学期12月月考化学试题河北省邢台市临西县2023-2024学年高一上学期第一次月考化学试题
名校
解题方法
2 . 下列叙述正确的是( )
A.NaHCO3与石灰水反应,当n(NaHCO3):n[Ca(OH)2]=2:1时, 完全转化为CaCO3 完全转化为CaCO3 |
| B.Fe与稀硝酸反应,当n(Fe):n(HNO3)=1:1时,铁元素在溶液中主要以Fe2+形式存在 |
C.AlCl3 溶液与烧碱溶液反应,当体积比为1:4时,铝元素恰好以 形式存在 形式存在 |
| D.CO2通入石灰水中,当n(CO2):n[Ca(OH)2]=2:3时,能得到澄清溶液 |
您最近一年使用:0次
3 . Ⅰ. 、
、 、
、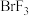 等称之为卤素互化物,
等称之为卤素互化物, 、
、 、
、 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(1)有一种碘的氧化物可以称为碘酸碘,其中碘元素呈 、
、 两种价态,则这种化合物的化学式是
两种价态,则这种化合物的化学式是__________ 。
(2)溴化碘( )具有强氧化性,能与
)具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为
溶液发生反应,发生反应的离子方程式为________ ;
(3)①已知某些离子的还原性强弱顺序为 。现将几滴
。现将几滴 溶液滴入到含少量
溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象_______ ;
②下列物质中,也可以使该溶液红色褪去的是_______ ;
A 新制氯水 B 碘水 C D 盐酸
D 盐酸
(4) 为剧毒物质,处理含有
为剧毒物质,处理含有 的废水常用的方法是:在碱性条件下用
的废水常用的方法是:在碱性条件下用 溶液将
溶液将 氧化为
氧化为 和一种单质气体,该反应的离子方程式为
和一种单质气体,该反应的离子方程式为_________ ;
(5)已知 的电离平衡常数
的电离平衡常数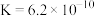 ,
, 的电离平衡常数
的电离平衡常数 ,
, ,则下列离子方程式能发生的是
,则下列离子方程式能发生的是____________ 。
A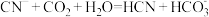 B
B 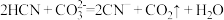
C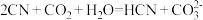 D
D 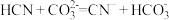
Ⅱ.如下图转化关系: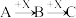
(6)若B为白色胶状不溶物,则A与C反应的离子方程式为_______ 。
(7)若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为______ 。
 、
、 、
、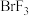 等称之为卤素互化物,
等称之为卤素互化物, 、
、 、
、 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。(1)有一种碘的氧化物可以称为碘酸碘,其中碘元素呈
 、
、 两种价态,则这种化合物的化学式是
两种价态,则这种化合物的化学式是(2)溴化碘(
 )具有强氧化性,能与
)具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为
溶液发生反应,发生反应的离子方程式为(3)①已知某些离子的还原性强弱顺序为
 。现将几滴
。现将几滴 溶液滴入到含少量
溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象②下列物质中,也可以使该溶液红色褪去的是
A 新制氯水 B 碘水 C
 D 盐酸
D 盐酸(4)
 为剧毒物质,处理含有
为剧毒物质,处理含有 的废水常用的方法是:在碱性条件下用
的废水常用的方法是:在碱性条件下用 溶液将
溶液将 氧化为
氧化为 和一种单质气体,该反应的离子方程式为
和一种单质气体,该反应的离子方程式为(5)已知
 的电离平衡常数
的电离平衡常数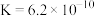 ,
, 的电离平衡常数
的电离平衡常数 ,
, ,则下列离子方程式能发生的是
,则下列离子方程式能发生的是A
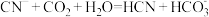 B
B 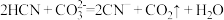
C
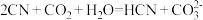 D
D 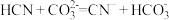
Ⅱ.如下图转化关系:
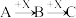
(6)若B为白色胶状不溶物,则A与C反应的离子方程式为
(7)若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为
您最近一年使用:0次
名校
解题方法
4 . 过氧乙酸( )是一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解,其制备愿理为:
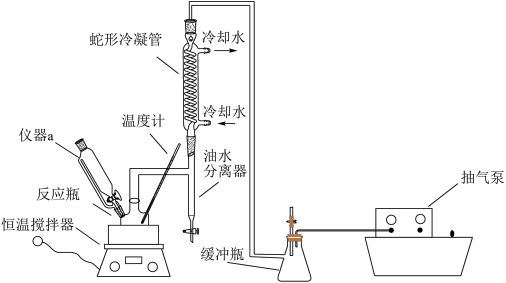
)是一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解,其制备愿理为: ,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率,为减少反应瓶中乙丁酯的损耗,反应开始前,在油水分离器中加满乙酸丁酯,实验装置如下图。
,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率,为减少反应瓶中乙丁酯的损耗,反应开始前,在油水分离器中加满乙酸丁酯,实验装置如下图。
(1)过氧乙酸保存与使用时应注意____ (填标号)。
A.避光 B.低温 C.配制消毒液时应带上橡胶手套 D.储存于密闭的金属容器
(2)仪器a的名称是___ ,在本实验中与使用普通分液漏斗相比的优点是__ ,其中盛放的试剂为__ (填“乙酸”或“双氧水”)
(3)反应体系采用减压的目的是___ 。
(4)过氧乙酸(含有少量 杂质)的含量测定流程如下图。
杂质)的含量测定流程如下图。

①判断 恰好除尽的实验现象是
恰好除尽的实验现象是____ 。
②过氧乙酸被 还原,还原产物之一为乙酸,其离子方程式为
还原,还原产物之一为乙酸,其离子方程式为_____ 。
③若样品体积为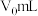 ,加入
,加入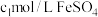 溶液
溶液 ,消耗
,消耗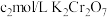 溶液
溶液 ,则过氧乙酸含量为
,则过氧乙酸含量为_____  。
。
(5)判断下列情况对过氧乙酸含量测定结果的影响(填“偏高”、“偏低”或“无影响”)。
①若滴定前无气泡,滴定终点时出现气泡,会使测定结果_____ 。
②若 标准液部分变质,会使测定结果
标准液部分变质,会使测定结果_______ 。
 )是一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解,其制备愿理为:
)是一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解,其制备愿理为: ,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率,为减少反应瓶中乙丁酯的损耗,反应开始前,在油水分离器中加满乙酸丁酯,实验装置如下图。
,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率,为减少反应瓶中乙丁酯的损耗,反应开始前,在油水分离器中加满乙酸丁酯,实验装置如下图。
(1)过氧乙酸保存与使用时应注意
A.避光 B.低温 C.配制消毒液时应带上橡胶手套 D.储存于密闭的金属容器
(2)仪器a的名称是
(3)反应体系采用减压的目的是
(4)过氧乙酸(含有少量
 杂质)的含量测定流程如下图。
杂质)的含量测定流程如下图。
①判断
 恰好除尽的实验现象是
恰好除尽的实验现象是②过氧乙酸被
 还原,还原产物之一为乙酸,其离子方程式为
还原,还原产物之一为乙酸,其离子方程式为③若样品体积为
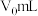 ,加入
,加入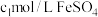 溶液
溶液 ,消耗
,消耗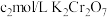 溶液
溶液 ,则过氧乙酸含量为
,则过氧乙酸含量为 。
。(5)判断下列情况对过氧乙酸含量测定结果的影响(填“偏高”、“偏低”或“无影响”)。
①若滴定前无气泡,滴定终点时出现气泡,会使测定结果
②若
 标准液部分变质,会使测定结果
标准液部分变质,会使测定结果
您最近一年使用:0次
名校
解题方法
5 . 下列离子方程式书写及评价合理的是
| 选项 | 离子方程式 | 评价 |
| A |  溶液中加入足量 溶液中加入足量 溶液 溶液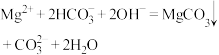 | 正确, 过量,酸式盐与碱完全反应生成正盐和水: 过量,酸式盐与碱完全反应生成正盐和水: |
| B |  的 的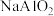 溶液与 溶液与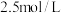 的 的 溶液等体积混合 溶液等体积混合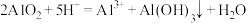 | 正确,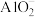 与H按物质的量1:1反应转化为 与H按物质的量1:1反应转化为 ,过量的 ,过量的 再将一半 再将一半 转化为 转化为 |
| C | 将少量的 溶解在过量的稀 溶解在过量的稀 中 中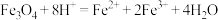 | 正确, 化学式可改写为 化学式可改写为 , , 与 与 ,物质的量之比为1:2 ,物质的量之比为1:2 |
| D | 将 溶液加入到足量的 溶液加入到足量的 溶液中 溶液中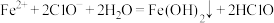 | 错误, 与 与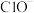 发生氧化还原反应:2Fe2++ClO-+5H2O=2Fe(OH)3↓+Cl-+4H+ 发生氧化还原反应:2Fe2++ClO-+5H2O=2Fe(OH)3↓+Cl-+4H+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-05-12更新
|
630次组卷
|
7卷引用:天津塘沽一中2020届高三3月网上测试化学试题
天津塘沽一中2020届高三3月网上测试化学试题天津市塘沽一中2020届高三第二次模拟考试化学试题2016届湖北省华中师大第一附属中学高三上期中理综化学试卷湖北省华中师范大学第一附属中学2017-2018学年高二上学期期中考试化学试题湖南省长沙市长郡中学2019届高三下学期第六次月考化学试题(已下线)微专题04 突破离子方程式书写正误判断中的“六大陷阱”-备战2022年高考化学考点微专题(已下线)微专题05 破解与量有关离子方程式书写的四型和四法-备战2022年高考化学考点微专题
2013·辽宁·模拟预测
名校
解题方法
6 . 固体A的化学式为NH5,其所有原子的最外电子层结构都符合相应稀有气体元素原子的最外电子层结构,则下列有关说法不正确的是( )
| A.1 mol NH5中含有5NA个N—H键(设NA表示阿伏加 德罗常数的值) |
| B.NH5中既有共价键又有离子键 |
C.NH5的电子式为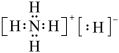 |
| D.NH5与水反应的离子方程式为NH4++H-+H2O=NH3·H2O+H2↑ |
您最近一年使用:0次
2020-03-26更新
|
1073次组卷
|
22卷引用:天津市七校(静海一中、宝坻一中、杨村一中等)2020届高三上学期期中联考化学试题
天津市七校(静海一中、宝坻一中、杨村一中等)2020届高三上学期期中联考化学试题天津市第八中学2021届高三上学期第三次统练化学试题(已下线)2013届辽宁省东北育才双语学校高三第五次模拟化学试卷(已下线)2014高考化学名师知识点精编 专题6原子结构化学键练习卷2014-2015学年黑龙江省龙东南四校高一下学期期末联考化学试卷2015-2016学年吉林省前郭县五中高一下学期第一次月考化学试卷2015-2016学年四川省成都市新都一中高一下4月月考化学试卷2017届重庆市巴蜀中学高三上学期开学考试化学试卷2017届河北省定州中学高三上第三次月考化学试卷2016-2017学年辽宁省实验中学北校高一3月月考化学试卷2016-2017学年重庆市南川区三校高一下学期期中考试化学试卷黑龙江省鹤岗第一中学2016-2017学年高一下学期期中考试化学试卷黑龙江省肇东市第一中学2016-2017学年高一下学期期中考试化学试题安徽省定远重点中学2017-2018学年高一下学期教学段考化学试题【全国百强校】安徽省合肥市第一六八中学2018-2019学年高一下学期期中考试化学试题山西省运城市永济涑北中学2019-2020学年高一下学期3月月考化学试题吉林省长春外国语学校2020-2021学年高二上学期期初考试化学试题(已下线)4.3.1 离子键(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)4.3.1 离子键-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)(已下线)练习8 化学键2020-2021学年【补习教材·寒假作业】高一化学(人教版2019)河南省驻马店经济开发区高级中学2020-2021学年下第一次月考化学试题福建省龙岩市武平县第一中学2020-2021学年高二下学期化学月考试题
解题方法
7 . 常温下,下列各组离子一定能在指定溶液中大量共存的是
A.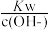 =10-12mol/L的溶液中: =10-12mol/L的溶液中: 、 、 、 、 、 、 |
B.使甲基橙变黄的溶液中: 、 、 、 、 、 、 |
C.由水电离出的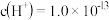  的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.使KSCN显红色的溶液中: 、 、 、 、 、 、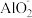 |
您最近一年使用:0次
2020-02-07更新
|
476次组卷
|
2卷引用:夯基提能2020届高三化学选择题对题专练——选修4化学反应原理—— 盐类水解的的规律、影响因素及应用
名校
解题方法
8 . 下列指定反应的离子方程式正确的是

A.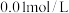 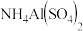 溶液与 溶液与   溶液等体积混合 溶液等体积混合 |
B.溴化亚铁溶液中通少量的氯气: |
C.过量的铁粉溶于稀硝酸: |
D.用浓盐酸酸化的  溶液与 溶液与  反应,证明 反应,证明  具有还原性: 具有还原性: |
您最近一年使用:0次
2019-12-26更新
|
279次组卷
|
2卷引用:天津一中2020届高三第二次月考化学试题
名校
解题方法
9 . 某无色透明溶液中可能大量存在Ag+、Mg2+、Fe3+、Na+、Cl-、CO32-、OH-和NO3-中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是______ ,有关的离子方程式______ 。
(3)取(2)中的滤液,加入过量的稀氨水(NH3·H2O),出现白色沉淀,说明原溶液中肯定有______ ,有关的离子方程式为______ 。
(4)综上所述,原溶液中一定存在的离子有______ ,可能存在的离子是______ 。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的稀氨水(NH3·H2O),出现白色沉淀,说明原溶液中肯定有
(4)综上所述,原溶液中一定存在的离子有
您最近一年使用:0次
2019-10-18更新
|
1048次组卷
|
7卷引用:江苏省海安高级中学2019-2020学年高一10月月考化学试题
10 . 按要求填空。
(1)①石墨②盐酸③胆矾④KOH固体⑤Fe⑥氨水⑦乙醇⑧醋酸⑨NaCl溶液⑩CO2⑪熔融BaSO4,能导电的是_____________ 电解质是_____________
(2)写出下列物质的电离方程式:①NaHSO4_________ ,②NaHCO3______ 。
(3)写出下列反应的离子方程式:①氢氧化铜与稀盐酸反应________ ,②氢氧化钡与稀硫酸反应________ ,③碳酸钙与硝酸反应_________________ ,④氧化铁与稀盐酸反应__________________ 。
(1)①石墨②盐酸③胆矾④KOH固体⑤Fe⑥氨水⑦乙醇⑧醋酸⑨NaCl溶液⑩CO2⑪熔融BaSO4,能导电的是
(2)写出下列物质的电离方程式:①NaHSO4
(3)写出下列反应的离子方程式:①氢氧化铜与稀盐酸反应
您最近一年使用:0次
2019-10-14更新
|
1053次组卷
|
2卷引用:天津市四合庄中学2019-2020学年高一上学期第一次月考化学试题



