1 . 使用硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]滴定法可以测定青铜中铬元素的含量。实验步骤如下:
步骤1:称量硫酸亚铁铵晶[(NH4)2Fe(SO4)2·6H2O]溶于稀硫酸,加水稀释配成1000 mL0.0200 mol/L (NH4)2Fe(SO4)2标准溶液。
步骤2:称取1.00 g青铜样品于250 mL锥形瓶中,加入适量稀硝酸使其完全溶解,再加入适量过二硫酸铵[(NH4)2S2O8]溶液,加热煮沸,使样品中的铬元素完全转化为H2CrO4,冷却后加蒸馏水配制成250 mL溶液,摇匀。
步骤3:取25 mL上述溶液置于锥形瓶中,加入硫酸酸化,滴入4滴N-苯代邻氨基苯甲酸指示剂,用(NH4)2Fe(SO4)2标准溶液满淀至终点。重复上述操作3次。测得消耗(NH4)2Fe(SO4)2标准溶液的体积分别为18.90 mL、17.97 mL、18.03 mL。发生反应的离子方程式为:H2CrO4+Fe2++H+→Cr3++Fe3++H2O (未配平)
下列说法不正确的是
步骤1:称量硫酸亚铁铵晶[(NH4)2Fe(SO4)2·6H2O]溶于稀硫酸,加水稀释配成1000 mL0.0200 mol/L (NH4)2Fe(SO4)2标准溶液。
步骤2:称取1.00 g青铜样品于250 mL锥形瓶中,加入适量稀硝酸使其完全溶解,再加入适量过二硫酸铵[(NH4)2S2O8]溶液,加热煮沸,使样品中的铬元素完全转化为H2CrO4,冷却后加蒸馏水配制成250 mL溶液,摇匀。
步骤3:取25 mL上述溶液置于锥形瓶中,加入硫酸酸化,滴入4滴N-苯代邻氨基苯甲酸指示剂,用(NH4)2Fe(SO4)2标准溶液满淀至终点。重复上述操作3次。测得消耗(NH4)2Fe(SO4)2标准溶液的体积分别为18.90 mL、17.97 mL、18.03 mL。发生反应的离子方程式为:H2CrO4+Fe2++H+→Cr3++Fe3++H2O (未配平)
下列说法不正确的是
| A.在“步骤1”中,用到的玻璃仪器有1000 mL容量瓶、烧杯、玻璃棒、胶头滴管 |
B.在“步骤2”中,铜与硝酸反应的离子方程式为:3Cu+2 +8H+=3Cu2++2NO↑+4H2O +8H+=3Cu2++2NO↑+4H2O |
| C.青铜中铬元素的质量分数为6.344% |
| D.实验中,如果盛放(NH4)2Fe(SO4)2标准溶液的滴定管没有润洗,则测量结果将偏大 |
您最近一年使用:0次
名校
2 . 下列化学反应表示正确的是
A.BeO与NaOH溶液反应: |
B.镁的燃烧热为610kJ/mol,镁的燃烧: ; ; |
C.向Mg(HCO3)2溶液中滴加足量NaOH溶液: |
D.用酸性KMnO4测定CaC2O4的含量: |
您最近一年使用:0次
3 . 室温下,将H2C2O4溶液和NaOH溶液按一定比例混合,可用于测定溶液中钙的含量。测定原理是①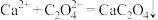 ②
② ,③用稀硫酸酸化的KMnO4溶液滴定②中H2C2O4。已知:室温下
,③用稀硫酸酸化的KMnO4溶液滴定②中H2C2O4。已知:室温下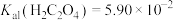 ,
,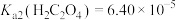 ,
,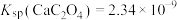 。下列说法正确的是
。下列说法正确的是
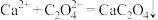 ②
② ,③用稀硫酸酸化的KMnO4溶液滴定②中H2C2O4。已知:室温下
,③用稀硫酸酸化的KMnO4溶液滴定②中H2C2O4。已知:室温下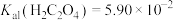 ,
,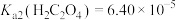 ,
,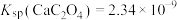 。下列说法正确的是
。下列说法正确的是A. NaHC2O4溶液中: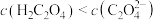 |
B.NaOH完全转化为 时,溶液中: 时,溶液中: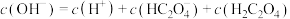 |
C.①中反应静置后的上层清液中: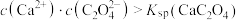 |
D.③发生反应的离子方程式为: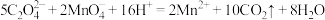 |
您最近一年使用:0次
2022-11-04更新
|
314次组卷
|
2卷引用:江苏省苏州市2022-2023学年高三上学期期中调研化学试题
4 . 海洋中的水资源、化学资源和生物资源具有十分巨大的开发潜力。海水中O、H、Cl、Na、Mg、S、Ca、K、Br、Sr、C、B、F等13种元素的总含量超过99%。以传统海水制盐工业为基础可制取镁、钾、溴及其他化工产品。以海水(主要含 、
、 、
、 、
、 、
、 等)和食盐为原料可制备多种化工产品。下列相关反应的离子方程式
等)和食盐为原料可制备多种化工产品。下列相关反应的离子方程式不正确 的是
 、
、 、
、 、
、 、
、 等)和食盐为原料可制备多种化工产品。下列相关反应的离子方程式
等)和食盐为原料可制备多种化工产品。下列相关反应的离子方程式A.向海水中加入石灰乳沉淀镁离子: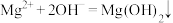 |
B.向海水中通入氯气提取溴单质: |
C.向海水中加入碳酸钠溶液沉淀钙离子: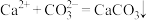 |
D.电解饱和食盐水制取氯气、氢气和烧碱: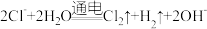 |
您最近一年使用:0次
21-22高三上·江苏·阶段练习
名校
5 . 利用废电池铜帽(Cu、Zn总含量约为99%)回收Cu并制备ZnO的部分实验过程如图所示,下列说法不正确的是




| A.铜溶解时的离子方程式为Cu+H2O2+2H+=Cu2++2H2O |
| B.可用加热的方法除去过量的H2O2 |
| C.调pH=2的目的是为了生成Cu(OH)2沉淀 |
| D.1个铜晶胞(如图所示)中含4个Cu原子 |
您最近一年使用:0次



