名校
解题方法
1 . 钒的氧化物(如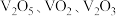 等,均难溶于水)在光储材料等领域有广泛应用。在800℃下,
等,均难溶于水)在光储材料等领域有广泛应用。在800℃下, 和焦炭反应可生成
和焦炭反应可生成 和
和 ,同时得到
,同时得到 气体。反应体系中钒氧化物的质量分数(%)随n(焦炭):
气体。反应体系中钒氧化物的质量分数(%)随n(焦炭):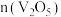 的变化关系如图。下列说法
的变化关系如图。下列说法不 正确的是
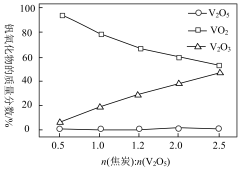
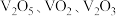 等,均难溶于水)在光储材料等领域有广泛应用。在800℃下,
等,均难溶于水)在光储材料等领域有广泛应用。在800℃下, 和焦炭反应可生成
和焦炭反应可生成 和
和 ,同时得到
,同时得到 气体。反应体系中钒氧化物的质量分数(%)随n(焦炭):
气体。反应体系中钒氧化物的质量分数(%)随n(焦炭):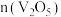 的变化关系如图。下列说法
的变化关系如图。下列说法
A.该条件下 的氧化性强于 的氧化性强于 和 和 |
B.铝还原 制钒的反应属于置换反应 制钒的反应属于置换反应 |
C.参加反应的n(焦炭):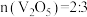 时,反应所得 时,反应所得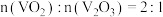 |
D.碳的用量越大,还原产物中 含量越低 含量越低 |
您最近一年使用:0次
2023-07-16更新
|
486次组卷
|
6卷引用:江苏省徐州市等3地2022-2023学年高一上学期期末考试化学试题
江苏省徐州市等3地2022-2023学年高一上学期期末考试化学试题江苏省南通市海安市2022-2023学年高一上学期期末考试化学试题(已下线)题型04 氧化还原反应方程式的配平及其计算-学易金卷:备战2023-2024学年高一化学期末真题分类汇编(江苏专用)江苏省苏州市工业园区星海实验高级中学2023-2024学年高一上学期12月调研化学试题江苏省苏州市吴江中学2023-2024学年高一上学期12月月考化学试题(1卷)江苏省苏州市黄埭中学2023-2024学年高一上学期12月月考化学试题
2 . 地球海洋是巨大的物质资源宝库,有待于人们进一步开发、利用和保护。氯化钠在海水中的质量分数为2.72%,是海水中含量最多的盐。从远古时代开始,人们就掌握了从海水中获取食盐的方法。近代以来,随着科学技术和化学工业的发展,人们在工业上以氯化钠为原料进一步制备金属钠、氯气、烧碱、碳酸氢钠和碳酸钠,并以氯气、烧碱等为原料进一步从海洋中提取出溴、碘、镁。这些海洋化工产品为化学工业生产体系输送了大量的基础原料,为人类的可持续发展做出了重要贡献。下列提取海洋资源的方法不正确 的是
| A.将海水蒸发结晶得到氯化钠晶体 | B.利用熟石灰从海水中沉淀氢氧化镁 |
| C.在海带浸取液中通入氯气制备碘 | D.利用空气从浓缩的海水中氧化出溴 |
您最近一年使用:0次
3 . 地球海洋是巨大的物质资源宝库,有待于人们进一步开发、利用和保护。氯化钠在海水中的质量分数为2.72%,是海水中含量最多的盐。从远古时代开始,人们就掌握了从海水中获取食盐的方法。近代以来,随着科学技术和化学工业的发展,人们在工业上以氯化钠为原料进一步制备金属钠、氯气、烧碱、碳酸氢钠和碳酸钠,并以氯气、烧碱等为原料进一步从海洋中提取出溴、碘、镁。这些海洋化工产品为化学工业生产体系输送了大量的基础原料,为人类的可持续发展做出了重要贡献。用下列装置模拟侯氏制碱法的部分工艺。下列对于该实验方案的说法不正确 的是
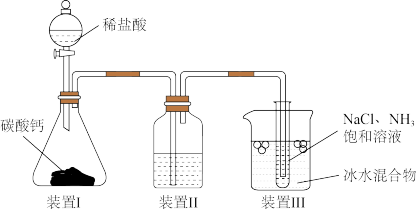

A.装置Ⅰ中使用小颗粒 可加快气体生成 可加快气体生成 |
B.装置Ⅱ中的试剂可使用饱和 溶液 溶液 |
C.装置Ⅲ中使用冰水可促进 析出 析出 |
D.侯氏制碱法可以实现 的循环利用 的循环利用 |
您最近一年使用:0次
解题方法
4 . 地球海洋是巨大的物质资源宝库,有待于人们进一步开发、利用和保护。氯化钠在海水中的质量分数为2.72%,是海水中含量最多的盐。从远古时代开始,人们就掌握了从海水中获取食盐的方法。近代以来,随着科学技术和化学工业的发展,人们在工业上以氯化钠为原料进一步制备金属钠、氯气、烧碱、碳酸氢钠和碳酸钠,并以氯气、烧碱等为原料进一步从海洋中提取出溴、碘、镁。这些海洋化工产品为化学工业生产体系输送了大量的基础原料,为人类的可持续发展做出了重要贡献。实验小组利用食盐、 和水等进行氯系消毒剂的制备。下列反应的离子方程式
和水等进行氯系消毒剂的制备。下列反应的离子方程式不正确 的是
 和水等进行氯系消毒剂的制备。下列反应的离子方程式
和水等进行氯系消毒剂的制备。下列反应的离子方程式A.电解饱和食盐水制氯气和碱: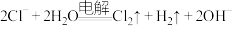 |
B.氯气和水反应制备次氯酸: |
C.氯气和碳酸钠溶液反应制备氯酸钠: |
D.氯酸钠和浓盐酸反应制备二氧化氯: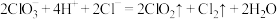 |
您最近一年使用:0次
5 . 使用硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]滴定法可以测定青铜中铬元素的含量。实验步骤如下:
步骤1:称量硫酸亚铁铵晶[(NH4)2Fe(SO4)2·6H2O]溶于稀硫酸,加水稀释配成1000 mL0.0200 mol/L (NH4)2Fe(SO4)2标准溶液。
步骤2:称取1.00 g青铜样品于250 mL锥形瓶中,加入适量稀硝酸使其完全溶解,再加入适量过二硫酸铵[(NH4)2S2O8]溶液,加热煮沸,使样品中的铬元素完全转化为H2CrO4,冷却后加蒸馏水配制成250 mL溶液,摇匀。
步骤3:取25 mL上述溶液置于锥形瓶中,加入硫酸酸化,滴入4滴N-苯代邻氨基苯甲酸指示剂,用(NH4)2Fe(SO4)2标准溶液满淀至终点。重复上述操作3次。测得消耗(NH4)2Fe(SO4)2标准溶液的体积分别为18.90 mL、17.97 mL、18.03 mL。发生反应的离子方程式为:H2CrO4+Fe2++H+→Cr3++Fe3++H2O (未配平)
下列说法不正确的是
步骤1:称量硫酸亚铁铵晶[(NH4)2Fe(SO4)2·6H2O]溶于稀硫酸,加水稀释配成1000 mL0.0200 mol/L (NH4)2Fe(SO4)2标准溶液。
步骤2:称取1.00 g青铜样品于250 mL锥形瓶中,加入适量稀硝酸使其完全溶解,再加入适量过二硫酸铵[(NH4)2S2O8]溶液,加热煮沸,使样品中的铬元素完全转化为H2CrO4,冷却后加蒸馏水配制成250 mL溶液,摇匀。
步骤3:取25 mL上述溶液置于锥形瓶中,加入硫酸酸化,滴入4滴N-苯代邻氨基苯甲酸指示剂,用(NH4)2Fe(SO4)2标准溶液满淀至终点。重复上述操作3次。测得消耗(NH4)2Fe(SO4)2标准溶液的体积分别为18.90 mL、17.97 mL、18.03 mL。发生反应的离子方程式为:H2CrO4+Fe2++H+→Cr3++Fe3++H2O (未配平)
下列说法不正确的是
| A.在“步骤1”中,用到的玻璃仪器有1000 mL容量瓶、烧杯、玻璃棒、胶头滴管 |
B.在“步骤2”中,铜与硝酸反应的离子方程式为:3Cu+2 +8H+=3Cu2++2NO↑+4H2O +8H+=3Cu2++2NO↑+4H2O |
| C.青铜中铬元素的质量分数为6.344% |
| D.实验中,如果盛放(NH4)2Fe(SO4)2标准溶液的滴定管没有润洗,则测量结果将偏大 |
您最近一年使用:0次
解题方法
6 . 短周期主族元素X、Y、Z、W原子序数依次增大,Ⅹ是空气中含量最多的元素,Y是海水中质量分数最大的元素,Z元素原子是短周期原子半径最大的,W与X属于同一主族。下列说法正确的是( )
| A.原子半径:W>Z>Y | B.由Y、Z组成的化合物中均不含共价键 |
| C.X的最高价氧化物对应水化物的酸性比W的强 | D.X的简单气态氢化物的热稳定性比Y的强 |
您最近一年使用:0次
解题方法
7 . 下列有关某些常见有机物的说法不 正确的是
A. 分子中所有碳原子共直线 分子中所有碳原子共直线 |
| B.所有碳氢化合物中,甲烷中碳的质量分数最低 |
C.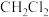 只表示一种物质 只表示一种物质 |
| D.乙烯和乙炔都能发生加成反应和加聚反应 |
您最近一年使用:0次
名校
解题方法
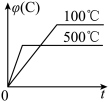
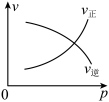
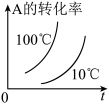
8 . 如图所示的各图中,表示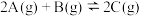
 这个可逆反应的正确图像的是[
这个可逆反应的正确图像的是[ 表示C的质量分数,p表示气体压强,c表示浓度]
表示C的质量分数,p表示气体压强,c表示浓度]
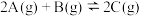
 这个可逆反应的正确图像的是[
这个可逆反应的正确图像的是[ 表示C的质量分数,p表示气体压强,c表示浓度]
表示C的质量分数,p表示气体压强,c表示浓度]
|
|
|
|
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 .  和
和 在生产、生活和科学研究中有着广泛的应用。工业上常用接触法制备硫酸,过程如下:将硫黄或其他含硫矿物在沸腾炉中与氧气反应生成
在生产、生活和科学研究中有着广泛的应用。工业上常用接触法制备硫酸,过程如下:将硫黄或其他含硫矿物在沸腾炉中与氧气反应生成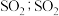 在
在 催化作用下与空气中的
催化作用下与空气中的 在接触室中发生可逆反应,生成的
在接触室中发生可逆反应,生成的 在吸收塔中用
在吸收塔中用 的浓硫酸吸收得到发烟硫酸
的浓硫酸吸收得到发烟硫酸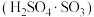 。下列与硫酸相关的实验能达到目的是
。下列与硫酸相关的实验能达到目的是
 和
和 在生产、生活和科学研究中有着广泛的应用。工业上常用接触法制备硫酸,过程如下:将硫黄或其他含硫矿物在沸腾炉中与氧气反应生成
在生产、生活和科学研究中有着广泛的应用。工业上常用接触法制备硫酸,过程如下:将硫黄或其他含硫矿物在沸腾炉中与氧气反应生成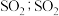 在
在 催化作用下与空气中的
催化作用下与空气中的 在接触室中发生可逆反应,生成的
在接触室中发生可逆反应,生成的 在吸收塔中用
在吸收塔中用 的浓硫酸吸收得到发烟硫酸
的浓硫酸吸收得到发烟硫酸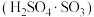 。下列与硫酸相关的实验能达到目的是
。下列与硫酸相关的实验能达到目的是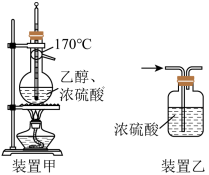
| A.装置甲可用于实验室制备乙烯气体 |
B.装置乙可用于去除乙烯中混有的 气体 气体 |
C.常温下,可使用浓硫酸和铁片反应制取 |
D.向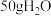 中加入 中加入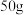 发烟硫酸,可配成 发烟硫酸,可配成 质量分数为 质量分数为 的硫酸溶液 的硫酸溶液 |
您最近一年使用:0次
名校
10 . 实验室测定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,实验装置示意图如下,下列说法正确的是
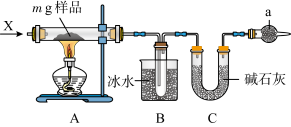

| A.X气体可以是空气,反应前和反应后均需通一段时间空气 |
B.装置B、C之间缺少 的干燥装置 的干燥装置 |
| C.a装置内应装碱石灰,目的是为了尾气处理 |
| D.没有a装置会导致所测碳酸钠的质量分数偏高 |
您最近一年使用:0次