名校
1 . 某种胃药的有效成分为碳酸钙.某实验小组为测定其中碳酸钙的含量.取10粒药片(0.1g/粒)研碎后溶解.加入25.00mL NaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:
NaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:
(1)配制500mL 的NaOH溶液,需要NaOH的质量是
的NaOH溶液,需要NaOH的质量是____________ 。
(2)药片中碳酸钙的质量分数_________ 。(写出计算过程)
 NaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:
NaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
V(NaOH)/mL | 13.00 | 12.90 | 11.40 | 13.10 |
 的NaOH溶液,需要NaOH的质量是
的NaOH溶液,需要NaOH的质量是(2)药片中碳酸钙的质量分数
您最近一年使用:0次
名校
解题方法
2 . 抗原检测盒中T线处是使用的胶体金(Au)标记物,一种从被FeS2包裹的含金矿物中提金的工艺流程如下:
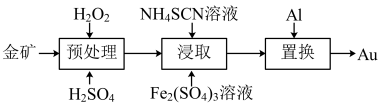
(1)①“预处理”时,FeS2被氧化为Fe2(SO4)3,写出该反应的离子方程式_______ 。
②研究发现H2O2在Fe2+的催化作用下产生具有强氧化能力的中间体·OH,·OH将金表面的FeS2氧化溶出。FeS2溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大,FeS2溶出率逐渐提高的主要原因是_______ 。

(2)“置换”时需维持无氧环境,其主要原因是_______ 。
(3)测定样品中Au的含量:准确称取0.1000g试样,加入王水,将Au转化成具有强氧化性的氯金酸(HAuCl4),在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量0.4000mol·L-1 FeSO4溶液30.00mL,将HAuCl4完全还原为Au:滴加二苯胺磺酸钠作指示剂,用0.1000mol·L-1 K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液18.00mL。
已知: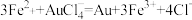

计算样品中金的质量分数(写出计算过程)_______ 。

(1)①“预处理”时,FeS2被氧化为Fe2(SO4)3,写出该反应的离子方程式
②研究发现H2O2在Fe2+的催化作用下产生具有强氧化能力的中间体·OH,·OH将金表面的FeS2氧化溶出。FeS2溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大,FeS2溶出率逐渐提高的主要原因是

(2)“置换”时需维持无氧环境,其主要原因是
(3)测定样品中Au的含量:准确称取0.1000g试样,加入王水,将Au转化成具有强氧化性的氯金酸(HAuCl4),在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量0.4000mol·L-1 FeSO4溶液30.00mL,将HAuCl4完全还原为Au:滴加二苯胺磺酸钠作指示剂,用0.1000mol·L-1 K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液18.00mL。
已知:
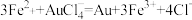

计算样品中金的质量分数(写出计算过程)
您最近一年使用:0次
3 . 水合肼(N2H4·H2O)是一种精细化工原料,常用于医药、农药、染料、航天等领域。实验室模拟尿素法制备N2H4·H2O流程图如图所示。
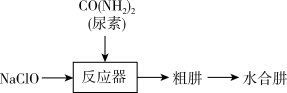
已知:①N2H4·H2O具有强还原性,易被氧化成N2。
②N2H4·H2O+H2SO4+6NaHCO3+2I2=N2↑+6CO2+Na2SO4+4NaI+7H2O
(1)CO(NH2)2(尿素)是常见的化肥,其在土壤中水解生成碳酸铵或碳酸氢铵,写出其水解生成碳酸氢铵的化学方程式_______ 。
(2)制备过程中NaClO溶液不能过量,其可能的原因是_______ 。
(3)水合肼(N2H4·H2O)产品含量测定步骤:将1.000g样品配制成100mL溶液,取5mL溶液于锥形瓶中,加入30mL水,再加入适量稀硫酸及NaHCO3固体,用0.1000mol·L-1标准碘溶液滴定至终点,消耗16.8mL,计算该产品中水合肼的质量分数_______ (写出计算过程,结果保留1位小数)。

已知:①N2H4·H2O具有强还原性,易被氧化成N2。
②N2H4·H2O+H2SO4+6NaHCO3+2I2=N2↑+6CO2+Na2SO4+4NaI+7H2O
(1)CO(NH2)2(尿素)是常见的化肥,其在土壤中水解生成碳酸铵或碳酸氢铵,写出其水解生成碳酸氢铵的化学方程式
(2)制备过程中NaClO溶液不能过量,其可能的原因是
(3)水合肼(N2H4·H2O)产品含量测定步骤:将1.000g样品配制成100mL溶液,取5mL溶液于锥形瓶中,加入30mL水,再加入适量稀硫酸及NaHCO3固体,用0.1000mol·L-1标准碘溶液滴定至终点,消耗16.8mL,计算该产品中水合肼的质量分数
您最近一年使用:0次
4 . CH4、CH3OH、CO等都是重要的能源,也是重要的化工原料。
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成CO和液态水时放出38kJ热量,则该条件下反应的热化学反应方程式___________ 。
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
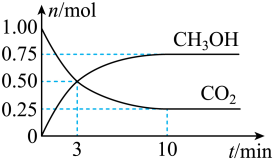
①从反应开始到平衡,CO2的平均反应速率v(CO2)=___________ 。
②达到平衡时,H2的转化率为___________ 。
(3)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g) CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成CO和液态水时放出38kJ热量,则该条件下反应的热化学反应方程式
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=
②达到平衡时,H2的转化率为
(3)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g)
 CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
您最近一年使用:0次
名校
5 . 某感光材料主要成分为KBr和KI,测定其中KBr含量的方法如下:
①称取试样1.000 g,溶解后制备成200.0 mL溶液。
②取50 mL上述溶液,用Br2水将I-氧化成IO ,除去过量Br2,加入过量KI,酸化溶液,加入指示剂,以0.100 0 mol·L-1 Na2S2O3溶液滴定析出的I2,终点时消耗30 mL。(已知:I2 + 2Na2S2O3 = Na2S2O4 + 2NaI )
,除去过量Br2,加入过量KI,酸化溶液,加入指示剂,以0.100 0 mol·L-1 Na2S2O3溶液滴定析出的I2,终点时消耗30 mL。(已知:I2 + 2Na2S2O3 = Na2S2O4 + 2NaI )
③另取50.00 mL试液,酸化后加入足量K2Cr2O7溶液处理,将释放出的I2和Br2蒸馏收集于含有过量KI的溶液中,反应完全后,加入指示剂,以0.100 0 mol·L-1的Na2S2O3溶液滴定其中的I2至终点,消耗15.00 mL 。
(1)写出第②步中用Br2水氧化I-的离子方程式:_______ 。
(2)第②步若未除去过量的Br2,对KBr含量测定结果的影响是_______ (填“偏大”“偏小”或“无影响”)。
(3)计算试样中KBr的质量分数_______ (写出计算过程)。
①称取试样1.000 g,溶解后制备成200.0 mL溶液。
②取50 mL上述溶液,用Br2水将I-氧化成IO
 ,除去过量Br2,加入过量KI,酸化溶液,加入指示剂,以0.100 0 mol·L-1 Na2S2O3溶液滴定析出的I2,终点时消耗30 mL。(已知:I2 + 2Na2S2O3 = Na2S2O4 + 2NaI )
,除去过量Br2,加入过量KI,酸化溶液,加入指示剂,以0.100 0 mol·L-1 Na2S2O3溶液滴定析出的I2,终点时消耗30 mL。(已知:I2 + 2Na2S2O3 = Na2S2O4 + 2NaI )③另取50.00 mL试液,酸化后加入足量K2Cr2O7溶液处理,将释放出的I2和Br2蒸馏收集于含有过量KI的溶液中,反应完全后,加入指示剂,以0.100 0 mol·L-1的Na2S2O3溶液滴定其中的I2至终点,消耗15.00 mL 。
(1)写出第②步中用Br2水氧化I-的离子方程式:
(2)第②步若未除去过量的Br2,对KBr含量测定结果的影响是
(3)计算试样中KBr的质量分数
您最近一年使用:0次
6 . KI和KBr都具有感光性,可以用来制作感光材料。某感光材料主要成分为KBr和KI,测定其中KBr含量的方法如下:
①称取试样1.000 g,溶解后制备成200.0 mL溶液。
②取50 mL上述溶液,用Br2水将I-氧化成IO3-,除去过量Br2,加入过量KI,酸化溶液,加入指示剂,以0.100 0 mol·L-1 Na2S2O3溶液滴定析出的I2,终点时消耗30 mL。
③另取50.00 mL试液,酸化后加入足量K2Cr2O7溶液处理,将释放出的I2和Br2蒸馏收集于含有过量KI的溶液中,反应完全后,加入指示剂,以0.100 0 mol·L-1的Na2S2O3溶液滴定其中的I2至终点,消耗15.00 mL 。
(1)写出第②步中用Br2水氧化I-的离子方程式:________ 。
(2)第②步除去过量Br2最简单的物理方法是________ ;若未除去过量的Br2,对KBr含量测定结果的影响是________ (填“偏大”“偏小”或“无影响”)。
(3)计算试样中KBr的质量分数_______ (写出计算过程)。
①称取试样1.000 g,溶解后制备成200.0 mL溶液。
②取50 mL上述溶液,用Br2水将I-氧化成IO3-,除去过量Br2,加入过量KI,酸化溶液,加入指示剂,以0.100 0 mol·L-1 Na2S2O3溶液滴定析出的I2,终点时消耗30 mL。
③另取50.00 mL试液,酸化后加入足量K2Cr2O7溶液处理,将释放出的I2和Br2蒸馏收集于含有过量KI的溶液中,反应完全后,加入指示剂,以0.100 0 mol·L-1的Na2S2O3溶液滴定其中的I2至终点,消耗15.00 mL 。
(1)写出第②步中用Br2水氧化I-的离子方程式:
(2)第②步除去过量Br2最简单的物理方法是
(3)计算试样中KBr的质量分数
您最近一年使用:0次
2020-05-16更新
|
370次组卷
|
3卷引用:江苏省南通市2020届高三第二次模拟考试(5月) 化学 试题
江苏省南通市2020届高三第二次模拟考试(5月) 化学 试题江苏省启东市2020届高三下学期阶段调研测试化学试题(已下线)第24讲 水的电离和溶液的pH(练)-2023年高考化学一轮复习讲练测(全国通用)
名校
7 . 以碳酸镁(含少量 )为原料制取硫酸镁晶体,并测定
)为原料制取硫酸镁晶体,并测定 含量:将原料完全溶于一定量的稀硫酸中,加足量的
含量:将原料完全溶于一定量的稀硫酸中,加足量的 后用
后用 调节溶液的
调节溶液的 ,静置后过滤,除去滤渣,将滤液结晶得硫酸镁晶体。
,静置后过滤,除去滤渣,将滤液结晶得硫酸镁晶体。
(1)
 的稀硫酸至少能溶解原料的质量为
的稀硫酸至少能溶解原料的质量为______ 。
(2)加 调节
调节 促进
促进 水解,写出总反应的离子方程式为
水解,写出总反应的离子方程式为______ 。
(3)已知: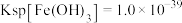 ,
,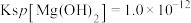 。室温下,若溶液中
。室温下,若溶液中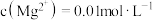 ,欲使溶液中的
,欲使溶液中的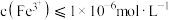 ,需调节溶液
,需调节溶液 范围为
范围为______ 。
(4)常采用下列方法测定结晶硫酸镁中 的含量:
的含量:
已知:①在 为9~10时,
为9~10时, 、
、 均能与
均能与 形成配合物
形成配合物
②在 为5~6时,
为5~6时, 除了与
除了与 反应,还能将
反应,还能将 与
与 形成的配合物中的
形成的配合物中的 “置换”出来:
“置换”出来: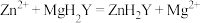
步骤1:准确称取得到的硫酸镁晶体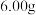 加入过量的
加入过量的 ,配成
,配成
 在9~10之间溶液
在9~10之间溶液
步骤2:准确移取 溶液
溶液 于锥形瓶中,用
于锥形瓶中,用 标准溶液滴定,滴定到终点,消耗标准溶液的体积为
标准溶液滴定,滴定到终点,消耗标准溶液的体积为
步骤3:准确移取 溶液
溶液 于另一只锥形瓶中,调节
于另一只锥形瓶中,调节 在5~6;用
在5~6;用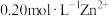 标准溶液滴定,滴定至终点,消耗
标准溶液滴定,滴定至终点,消耗 标准溶液的体积为
标准溶液的体积为 。
。
计算该结晶硫酸镁中 的质量分数(请给出计算过程)。
的质量分数(请给出计算过程)。____________ 。
 )为原料制取硫酸镁晶体,并测定
)为原料制取硫酸镁晶体,并测定 含量:将原料完全溶于一定量的稀硫酸中,加足量的
含量:将原料完全溶于一定量的稀硫酸中,加足量的 后用
后用 调节溶液的
调节溶液的 ,静置后过滤,除去滤渣,将滤液结晶得硫酸镁晶体。
,静置后过滤,除去滤渣,将滤液结晶得硫酸镁晶体。(1)

 的稀硫酸至少能溶解原料的质量为
的稀硫酸至少能溶解原料的质量为(2)加
 调节
调节 促进
促进 水解,写出总反应的离子方程式为
水解,写出总反应的离子方程式为(3)已知:
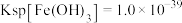 ,
,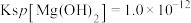 。室温下,若溶液中
。室温下,若溶液中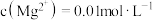 ,欲使溶液中的
,欲使溶液中的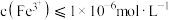 ,需调节溶液
,需调节溶液 范围为
范围为(4)常采用下列方法测定结晶硫酸镁中
 的含量:
的含量:已知:①在
 为9~10时,
为9~10时, 、
、 均能与
均能与 形成配合物
形成配合物②在
 为5~6时,
为5~6时, 除了与
除了与 反应,还能将
反应,还能将 与
与 形成的配合物中的
形成的配合物中的 “置换”出来:
“置换”出来: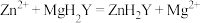
步骤1:准确称取得到的硫酸镁晶体
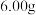 加入过量的
加入过量的 ,配成
,配成
 在9~10之间溶液
在9~10之间溶液
步骤2:准确移取
 溶液
溶液 于锥形瓶中,用
于锥形瓶中,用 标准溶液滴定,滴定到终点,消耗标准溶液的体积为
标准溶液滴定,滴定到终点,消耗标准溶液的体积为
步骤3:准确移取
 溶液
溶液 于另一只锥形瓶中,调节
于另一只锥形瓶中,调节 在5~6;用
在5~6;用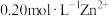 标准溶液滴定,滴定至终点,消耗
标准溶液滴定,滴定至终点,消耗 标准溶液的体积为
标准溶液的体积为 。
。计算该结晶硫酸镁中
 的质量分数(请给出计算过程)。
的质量分数(请给出计算过程)。
您最近一年使用:0次
8 . 某铝合金中含有元素:铝、镁、铜、碳,为测定该合金中铝的含量。
Ⅰ 甲同学设计如下实验:
(1)称取样品a g(精确到0.1 g),溶于足量稀盐酸,过滤。
(2)向步骤(1)所得滤液中加入过量的氢氧化钠溶液,过滤并洗涤滤渣。有关反应的离子方程式是_________________________________ 、____________________________________________ 。
(3)向步骤(2)所得滤液中通入过量的二氧化碳气体,过滤并洗涤滤渣。有关反应的离子方程式是_________________________________ 、____________________________________________ 。
(4)将步骤(3)所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为b g。有关反应的化学方程式是_________________________________ 。原样品中铝的质量分数是__________ 。
Ⅱ 乙同学认为也可以向一定质量的样品中直接加足量氢氧化钠溶液充分反应后,将剩余固体过滤、洗涤、干燥后称量,即可计算该合金中铝的含量。有关反应的离子方程式是____________________________________________ 。
Ⅰ 甲同学设计如下实验:
(1)称取样品a g(精确到0.1 g),溶于足量稀盐酸,过滤。
(2)向步骤(1)所得滤液中加入过量的氢氧化钠溶液,过滤并洗涤滤渣。有关反应的离子方程式是
(3)向步骤(2)所得滤液中通入过量的二氧化碳气体,过滤并洗涤滤渣。有关反应的离子方程式是
(4)将步骤(3)所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为b g。有关反应的化学方程式是
Ⅱ 乙同学认为也可以向一定质量的样品中直接加足量氢氧化钠溶液充分反应后,将剩余固体过滤、洗涤、干燥后称量,即可计算该合金中铝的含量。有关反应的离子方程式是
您最近一年使用:0次
名校
9 . 实验室模拟用工业废弃固体(含有Cu2S、Al2O3、Fe2O3、SiO2等)制取粗铜、绿矾(FeSO4·7H2O)和明矾[KAl(SO4)2·12H2O]的操作流程如下:
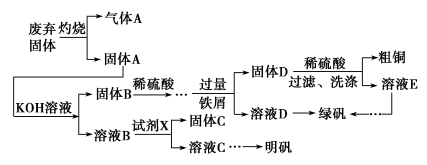
(1)试剂X是________________________________________ (写化学式)。
(2)配平下列方程式:
______MnO4-+______SO2+______H2O===______Mn2++______SO42-+______H+______________
(3)为了分析产品(绿矾)中铁元素的含量,某同学称取20.0 g样品配成100 mL溶液,移取至锥形瓶中,用1.000×10-1 mol·L-1的KMnO4标准溶液进行滴定(MnO 被还原为Mn2+)。若两者正好反应时消耗KMnO4标准溶液的体积为100.00 mL,则该产品中铁元素的质量分数为
被还原为Mn2+)。若两者正好反应时消耗KMnO4标准溶液的体积为100.00 mL,则该产品中铁元素的质量分数为___________ 。(写出解题过程)

(1)试剂X是
(2)配平下列方程式:
______MnO4-+______SO2+______H2O===______Mn2++______SO42-+______H+
(3)为了分析产品(绿矾)中铁元素的含量,某同学称取20.0 g样品配成100 mL溶液,移取至锥形瓶中,用1.000×10-1 mol·L-1的KMnO4标准溶液进行滴定(MnO
 被还原为Mn2+)。若两者正好反应时消耗KMnO4标准溶液的体积为100.00 mL,则该产品中铁元素的质量分数为
被还原为Mn2+)。若两者正好反应时消耗KMnO4标准溶液的体积为100.00 mL,则该产品中铁元素的质量分数为
您最近一年使用:0次
10 . (1)同分异构现象在有机化合物中是非常普遍的。下列各组化合物:
①CH3CH2CH2CH3和(CH3)2CHCH3; ②CH3CH2OH和CH3CH2CH2OH;
③CH3COOCH2CH3和CH3CH2CH2COOH; ④CH3CH=CHCH3和CH3CH2CH=CH2;
⑤ 和
和 。其中互为同分异构体的是
。其中互为同分异构体的是______________________ (填序号)。
(2)下列5种有机化合物:乙酸乙酯(CH3COOCH2CH3)、苯酚( )、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH)。
)、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH)。
①其中能与Na2CO3溶液反应产生气泡的是______________________ 。
②其中能与FeCl3溶液发生显色反应的是________________________ 。
③其中能发生银镜反应的是________________________ 。
④写出乙酸乙酯碱性条件水解反应的化学方程式____________________________ 。
(3)①蛋白质是维持生命的重要物质,它是由_____________________ 通过缩聚反应生成的一类高分子化合物;氨基酸因分子中含有的官能团是____________________ 和____________________ ,而具有__________________ 性。
②2008年,三鹿婴幼儿奶粉由于人为添加三聚氰胺,导致长期食用该奶粉的部分婴幼儿出现肾结石病。三聚氰胺的结构简式如下图所示。

请你预测三聚氰胺在核磁共振氢谱图(1H核磁共振谱图)中会出现____________________ 个峰;三聚氰 胺中氮元素的质量分数为______________________ (结果用百分数表示,并保留一位小数),添加三聚氰胺会使食品中蛋白质的含量虚高。
①CH3CH2CH2CH3和(CH3)2CHCH3; ②CH3CH2OH和CH3CH2CH2OH;
③CH3COOCH2CH3和CH3CH2CH2COOH; ④CH3CH=CHCH3和CH3CH2CH=CH2;
⑤
 和
和 。其中互为同分异构体的是
。其中互为同分异构体的是(2)下列5种有机化合物:乙酸乙酯(CH3COOCH2CH3)、苯酚(
 )、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH)。
)、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH)。①其中能与Na2CO3溶液反应产生气泡的是
②其中能与FeCl3溶液发生显色反应的是
③其中能发生银镜反应的是
④写出乙酸乙酯碱性条件水解反应的化学方程式
(3)①蛋白质是维持生命的重要物质,它是由
②2008年,三鹿婴幼儿奶粉由于人为添加三聚氰胺,导致长期食用该奶粉的部分婴幼儿出现肾结石病。三聚氰胺的结构简式如下图所示。

请你预测三聚氰胺在核磁共振氢谱图(1H核磁共振谱图)中会出现
您最近一年使用:0次



