名校
解题方法
1 . 工业上,以硫铁矿(主要成分为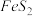 )为原料采用接触法制备硫酸。硫酸厂烧渣含
)为原料采用接触法制备硫酸。硫酸厂烧渣含 、
、 、
、 、
、 等,用过量的浓盐酸溶解烧渣,经过滤,得到滤液可再利用。在上述“滤液”中,下列离子组能大量共存的是
等,用过量的浓盐酸溶解烧渣,经过滤,得到滤液可再利用。在上述“滤液”中,下列离子组能大量共存的是
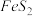 )为原料采用接触法制备硫酸。硫酸厂烧渣含
)为原料采用接触法制备硫酸。硫酸厂烧渣含 、
、 、
、 、
、 等,用过量的浓盐酸溶解烧渣,经过滤,得到滤液可再利用。在上述“滤液”中,下列离子组能大量共存的是
等,用过量的浓盐酸溶解烧渣,经过滤,得到滤液可再利用。在上述“滤液”中,下列离子组能大量共存的是A.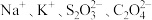 | B. |
C. | D.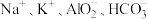 |
您最近一年使用:0次
解题方法
2 . 某溶液Q中含有如表所示离子中的5种离子,且离子浓度均为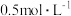 (不考虑水的电离与离子水解)。现向溶液Q中加入足量稀氢溴酸,有单一气体R产生,经分析,反应前后阴离子种类不变。
(不考虑水的电离与离子水解)。现向溶液Q中加入足量稀氢溴酸,有单一气体R产生,经分析,反应前后阴离子种类不变。
已知 在酸性溶液中会发生歧化反应。请回答下列问题:
在酸性溶液中会发生歧化反应。请回答下列问题:
(1)由“加入足量稀氢溴酸,……”“反应前后阴离子种类不变”推知:溶液Q中一定不含的阴离子有_______ (填数字)种。
(2)综合推断,溶液Q中一定含有的阳离子有_______ (填离子符号,下同)。产生气体R的反应中,原溶液中过量的离子是_______ 。
(3)一定量溶液Q与氯气缓慢反应,反应后的溶液分为3份,分别进行以下操作,实验现象如图:

①铜粉参与的反应中,氧化产物是_______ (填离子符号)。
②当 时,向溶液Q中通入氯气时发生反应的离子方程式为
时,向溶液Q中通入氯气时发生反应的离子方程式为_______ ;假设不考虑 与
与 的反应,则根据实验现象可推算出V的范围为
的反应,则根据实验现象可推算出V的范围为_______ 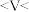
_______ 。
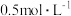 (不考虑水的电离与离子水解)。现向溶液Q中加入足量稀氢溴酸,有单一气体R产生,经分析,反应前后阴离子种类不变。
(不考虑水的电离与离子水解)。现向溶液Q中加入足量稀氢溴酸,有单一气体R产生,经分析,反应前后阴离子种类不变。| 阳离子 | 阴离子 |
  |   |
 在酸性溶液中会发生歧化反应。请回答下列问题:
在酸性溶液中会发生歧化反应。请回答下列问题:(1)由“加入足量稀氢溴酸,……”“反应前后阴离子种类不变”推知:溶液Q中一定不含的阴离子有
(2)综合推断,溶液Q中一定含有的阳离子有
(3)一定量溶液Q与氯气缓慢反应,反应后的溶液分为3份,分别进行以下操作,实验现象如图:

①铜粉参与的反应中,氧化产物是
②当
 时,向溶液Q中通入氯气时发生反应的离子方程式为
时,向溶液Q中通入氯气时发生反应的离子方程式为 与
与 的反应,则根据实验现象可推算出V的范围为
的反应,则根据实验现象可推算出V的范围为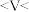
您最近一年使用:0次
3 . 某黄色溶液中可能含有大量 、OH-、S2-、I-、
、OH-、S2-、I-、 、Ca2+、
、Ca2+、 、Fe3+、Ba2+、K+、H+中的若干种(不考虑水的电离)。下列分析中正确的是
、Fe3+、Ba2+、K+、H+中的若干种(不考虑水的电离)。下列分析中正确的是
 、OH-、S2-、I-、
、OH-、S2-、I-、 、Ca2+、
、Ca2+、 、Fe3+、Ba2+、K+、H+中的若干种(不考虑水的电离)。下列分析中正确的是
、Fe3+、Ba2+、K+、H+中的若干种(不考虑水的电离)。下列分析中正确的是| A.溶液中至多5种离子 | B. 、K+至少含有一种 、K+至少含有一种 |
| C.溶液一定显酸性,可能含I- | D.无法判断溶液中是否大量含有Ca2+ |
您最近一年使用:0次
2022-10-01更新
|
298次组卷
|
4卷引用:河南省洛阳市2022-2023学年高三上学期9月联考化学试题
名校
4 . 氯酸镁[Mg(ClO3)]常做催熟剂、除草剂等。实验室利用卤块(主要成分为MgCl2•6H2O,含有MgSO4、FeCl2等杂质)制备少量Mg(ClO3)2的工艺流程如图:
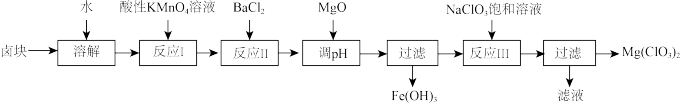
部分氢氧化物开始沉淀及沉淀完全的pH如表所示:
下列说法正确的是

部分氢氧化物开始沉淀及沉淀完全的pH如表所示:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 8.9 |
| 沉淀完全的pH | 3.2 | 9.7 | 10.9 |
A.反应I的离子方程式为MnO +5Fe2++4H2O=Mn2++5Fe3++8OH- +5Fe2++4H2O=Mn2++5Fe3++8OH- |
B.反应II后溶液中大量存在的离子是Mg2+、Ba2+、Fe3+、SO 、Cl- 、Cl- |
| C.调pH时应控制溶液的pH在1.5~3.2 |
| D.反应III属于复分解反应,能够发生的原因是因为生成溶解度相对较小的Mg(ClO3)2 |
您最近一年使用:0次
5 . 某无色、澄清溶液中可能含有Na+、Cl-、 、
、 、Fe3+、OH-、
、Fe3+、OH-、 中的几种,依次进行下列实验,观察到的现象如下:
中的几种,依次进行下列实验,观察到的现象如下:
已知:2Al+2OH-+2H2O=2 +3H2↑。
+3H2↑。
(1)不需要通过实验就能判断原溶液中肯定没有_______ 离子,肯定有_______ 离子。
(2)写出Ⅲ中发生的反应的离子方程式_______ 。
(3)原溶液中可能存在_______ 离子,验证溶液中是否存在此离子的实验方法_______ 。
(4)若(2)中的离子不存在,则溶液中一定存在的阴离子_______ 。
 、
、 、Fe3+、OH-、
、Fe3+、OH-、 中的几种,依次进行下列实验,观察到的现象如下:
中的几种,依次进行下列实验,观察到的现象如下:已知:2Al+2OH-+2H2O=2
 +3H2↑。
+3H2↑。| 步骤 | 操作 | 现象 |
| Ⅰ | 取少量溶液,向其中加入适量铝粉 | 有气体生成 |
| Ⅱ | 另取少量溶液,向其中滴加足量BaCl2溶液 | 有白色沉淀生成 |
| Ⅲ | 向Ⅱ中滴加足量稀盐酸 | 沉淀部分溶解 |
(2)写出Ⅲ中发生的反应的离子方程式
(3)原溶液中可能存在
(4)若(2)中的离子不存在,则溶液中一定存在的阴离子
您最近一年使用:0次
2022-09-10更新
|
228次组卷
|
2卷引用:辽宁省实验中学2022-2023学年高二上学期第一次月考化学试题
解题方法
6 . 回答下列问题
(1)用自来水配制硝酸银溶液会产生浑浊现象,说明自来水中有__________ (微粒符号表示)。
(2)某反应后的溶液中有 。已知
。已知 在反应中得到电子,该反应的离子方程式
在反应中得到电子,该反应的离子方程式_____________ (不用配平)。
(3)某工业废水经检测显酸性,且废水中含有较多的 ,则于该废水中的不可能大量存在是(选
,则于该废水中的不可能大量存在是(选 )
)____________ ;若将该废水调节至碱性,原废水中__________ 的离子会减少。
(1)用自来水配制硝酸银溶液会产生浑浊现象,说明自来水中有
(2)某反应后的溶液中有
 。已知
。已知 在反应中得到电子,该反应的离子方程式
在反应中得到电子,该反应的离子方程式(3)某工业废水经检测显酸性,且废水中含有较多的
 ,则于该废水中的不可能大量存在是(选
,则于该废水中的不可能大量存在是(选 )
)
您最近一年使用:0次
解题方法
7 . 某溶液中含有K+、Na+、Fe2+、Fe3+、 、OH-、
、OH-、 、
、 中的几种,且溶液中各离子的浓度相等。将其均分为两份,向其中一份中加入氯化钡溶液,生成不溶于酸的沉淀;向另一份中加入适量稀盐酸,生成无色无味气体,后该气体变为红棕色。下列说法不正确的是
中的几种,且溶液中各离子的浓度相等。将其均分为两份,向其中一份中加入氯化钡溶液,生成不溶于酸的沉淀;向另一份中加入适量稀盐酸,生成无色无味气体,后该气体变为红棕色。下列说法不正确的是
 、OH-、
、OH-、 、
、 中的几种,且溶液中各离子的浓度相等。将其均分为两份,向其中一份中加入氯化钡溶液,生成不溶于酸的沉淀;向另一份中加入适量稀盐酸,生成无色无味气体,后该气体变为红棕色。下列说法不正确的是
中的几种,且溶液中各离子的浓度相等。将其均分为两份,向其中一份中加入氯化钡溶液,生成不溶于酸的沉淀;向另一份中加入适量稀盐酸,生成无色无味气体,后该气体变为红棕色。下列说法不正确的是A.该溶液中不可能有 |
B.生成无色无味气体的方程式是: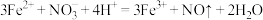 |
| C.借助焰色试验观察到黄色火焰,就可以确定该溶液成分 |
| D.只借助铁氰化钾,洁净铂丝,酒精灯,烧杯,玻璃棒,胶头滴管,也可以判断该溶液成分 |
您最近一年使用:0次
8 . 某澄清溶液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 离子中的几种,且每种离子物质的量浓度均为0.1mol/L,对该溶液进行如下试验,对应操作与现象如下:
离子中的几种,且每种离子物质的量浓度均为0.1mol/L,对该溶液进行如下试验,对应操作与现象如下:
实验①:取少量溶液滴加几滴石蕊试液,溶液变红色;
实验②:取少量溶液,加入铁屑,产生无色气泡,在试管口变红棕色;
实验③:取100mL溶液,滴加足量 溶液,产生2.33g沉淀。
溶液,产生2.33g沉淀。
下列说法正确的是
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 离子中的几种,且每种离子物质的量浓度均为0.1mol/L,对该溶液进行如下试验,对应操作与现象如下:
离子中的几种,且每种离子物质的量浓度均为0.1mol/L,对该溶液进行如下试验,对应操作与现象如下:实验①:取少量溶液滴加几滴石蕊试液,溶液变红色;
实验②:取少量溶液,加入铁屑,产生无色气泡,在试管口变红棕色;
实验③:取100mL溶液,滴加足量
 溶液,产生2.33g沉淀。
溶液,产生2.33g沉淀。下列说法正确的是
A.无法确定 和 和 的存在 的存在 | B.肯定存在的有 、 、 、 、 、 、 、 、 |
C.肯定不存在的有 、 、 、 、 | D. 肯定不存在 肯定不存在 |
您最近一年使用:0次
2022高三·全国·专题练习
9 . 无色澄清透明的溶液中:Fe3+、Mg2+、Br-、Cl-。(__)
您最近一年使用:0次
2022高三·全国·专题练习
解题方法
10 . c(SCN-)=1 mol·L-1的溶液中可能大量存在Fe3+、K+、Cl-、SO 。(__)
。(__)
 。(__)
。(__)
您最近一年使用:0次



