名校
1 . 按要求回答下列问题
(1)在无色透明的强酸性溶液中能大量共存的离子组是_______ 。
①.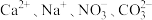
②.
③.
④.
⑤.Fe3+、K+、Cl-、S2-
⑥.Ag+、Na+、 、
、
⑦.Na+、Al3+、 、Cl-
、Cl-
⑧.Ba2+、 、C1-、CH3COO-
、C1-、CH3COO-
(2)①用单线桥表示反应电子转移的方向和数目: ,被氧化和被还原元素的物质的个数比
,被氧化和被还原元素的物质的个数比_______ 。
②用双线桥表示反应电子转移的方向和数目_______ 。
2Na2O2+2H2O=4NaOH+O2↑
反应每生成1个O2转移的电子数目为_______ 。
(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:将这6种物质分别填入下面对应的横线上,组成一个配平 的化学方程式:_______ 。
_______+_______+H2SO4→_______+_______+_______(填化学式)
(1)在无色透明的强酸性溶液中能大量共存的离子组是
①.
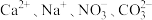
②.

③.

④.

⑤.Fe3+、K+、Cl-、S2-
⑥.Ag+、Na+、
 、
、
⑦.Na+、Al3+、
 、Cl-
、Cl-⑧.Ba2+、
 、C1-、CH3COO-
、C1-、CH3COO-(2)①用单线桥表示反应电子转移的方向和数目:
 ,被氧化和被还原元素的物质的个数比
,被氧化和被还原元素的物质的个数比②用双线桥表示反应电子转移的方向和数目
2Na2O2+2H2O=4NaOH+O2↑
反应每生成1个O2转移的电子数目为
(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:将这6种物质分别填入下面对应的横线上,组成一个
_______+_______+H2SO4→_______+_______+_______(填化学式)
您最近一年使用:0次
名校
2 . 常温下,对下列离子或分子组中在溶液中能否大量共存的判断和解释均正确的
| 选项 | 离子或分子 | 判断和解释 |
| A | 加入铝片能生成H2的溶液中:K+、 、 、 、I- 、I- | 可能共存 |
| B | K+、H+、 、H2O2、 、H2O2、 | 不能;因为:6H++2 +3H2O2﹦2Mn2++4O2↑+6H2O +3H2O2﹦2Mn2++4O2↑+6H2O |
| C | 新制氯水中:Al3+、Mg2+、 、 、 | 能;阴、阳离子之间不反应,且都不和氯水发生反应 |
| D | pH=7的溶液:Fe3+、K+、Cl-、 | 不能;因为pH=7时,Fe3+会变成氢氧化铁沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-07更新
|
273次组卷
|
2卷引用:湖南省益阳市箴言中学2021-2022学年高三上学期第三次模拟考试(11月)化学试题
解题方法
3 . 下列叙述正确的是
A.在c(Cu2+)= 1 mol·L-1的透明溶液中,Fe2+、Al3+、Cl-、SO 可能大量共存 可能大量共存 |
| B.氯气溶于水的离子方程式: Cl2+ H2O=2H++Cl- +C1O- |
| C.0.5 mol NO2 溶于水形成1 L溶液,可得到0.5 mol·L-1的硝酸溶液 |
| D.Cl2在水中溶解度较小,所以不能做喷泉实验 |
您最近一年使用:0次
名校
4 .  在强酸性和强碱性溶液中均不能大量共存。(_______)
在强酸性和强碱性溶液中均不能大量共存。(_______)
 在强酸性和强碱性溶液中均不能大量共存。(_______)
在强酸性和强碱性溶液中均不能大量共存。(_______)
您最近一年使用:0次
解题方法
5 . 工业上利用空气催化氧化法除电石渣浆上层清液中的S2-,并制取石膏的过程如图。下列说法正确的是
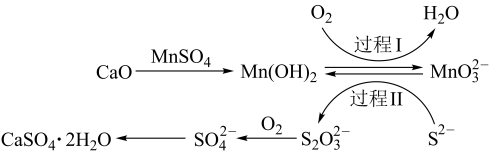

A.在能使甲基橙变红的溶液中,S2-、 均不能大量存在 均不能大量存在 |
B.过程I发生反应的离子方程式为O2+2Mn(OH)2=2MnO +4H+ +4H+ |
| C.该空气催化氧化法除S2-的过程中,Mn(OH)2作催化剂 |
| D.经过程I、过程II反应后的溶液的pH比原溶液的pH小 |
您最近一年使用:0次
名校
解题方法
6 . 铁及其化合物在生产生活中应用广泛。下列有关铁的化合物的叙述正确的是
A.用FeCl3溶液刻蚀铜板: |
B.将氧化铁加入HI溶液中发生反应: |
| C.向含1 molFeBr2的溶液中通入1 mol Cl2充分反应转移2 mol电子 |
D.含有 Fe2+的溶液中大量存在H+、Mg2+、Cl-、 |
您最近一年使用:0次
2021-12-13更新
|
843次组卷
|
3卷引用:湖南省长沙市第一中学中长郡中学名校联考联合体2021-2022学年高一上学期12月联考化学试题
名校
7 . 下列说法中正确的是
A.某酸性溶液中: 、 、 、 、 、 、 能大量共存 能大量共存 |
B.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 能大量共存 能大量共存 |
C.某透明溶液中: 、 、 、 、 、 、 可能大量共存 可能大量共存 |
D.取少量某溶液,向其中加入盐酸酸化的 溶液,观察到有白色沉淀生成,则证明该溶液中含有 溶液,观察到有白色沉淀生成,则证明该溶液中含有 |
您最近一年使用:0次
2021-12-12更新
|
739次组卷
|
4卷引用:辽宁省名校联盟2021-2022学年高一上学期12月联合考试化学试题
21-22高三上·江苏·期中
解题方法
8 . 室温下,通过下列实验探究某84消毒液(主要成分为NaClO和NaCl)的性质。
实验1:少量稀消毒液中加入饱和Ag2SO4溶液,产生白色沉淀
实验2:少量稀消毒液中加入0.2mol·L-1CH3COOH溶液,光照后管壁有气泡
实验3:少量稀消毒液中加入0.2 mol·L-1FeSO4酸性溶液和KSCN溶液,溶液变红
实验4:少量稀消毒液中加入0.2 mol·L-1AlCl3溶液,产生白色沉淀
下列说法正确的是
实验1:少量稀消毒液中加入饱和Ag2SO4溶液,产生白色沉淀
实验2:少量稀消毒液中加入0.2mol·L-1CH3COOH溶液,光照后管壁有气泡
实验3:少量稀消毒液中加入0.2 mol·L-1FeSO4酸性溶液和KSCN溶液,溶液变红
实验4:少量稀消毒液中加入0.2 mol·L-1AlCl3溶液,产生白色沉淀
下列说法正确的是
| A.实验1中两溶液混合时有;c(Ag+)·c(Cl-)<Ksp(AgCl) |
| B.实验2中管壁中气泡成分只有一种单质气体 |
| C.实验3中发生反应的离子方程式有:ClO- +2Fe2++2H+= 2Fe3++ H2O+Cl- |
| D.实验4中反应后溶液中大量存在的离子有:Na+、ClO-、A13+、Cl-、H+ |
您最近一年使用:0次
名校
解题方法
9 . 某强酸性透明溶液中可能含有 、
、 、
、 、
、 、
、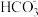 、
、 中的几种。为了确定其组成,现做以下实验:
中的几种。为了确定其组成,现做以下实验:
①取该溶液 ,加入足量的
,加入足量的 溶液,加热,得到标况下
溶液,加热,得到标况下 气体;同时产生红褐色沉淀,过滤,洗涤,干燥得到
气体;同时产生红褐色沉淀,过滤,洗涤,干燥得到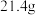 固体。
固体。
②向上述滤液中加入足量的 溶液,产生白色沉淀,过滤,洗涤,干燥得到
溶液,产生白色沉淀,过滤,洗涤,干燥得到 固体。
固体。
已知:含 的盐与强碱混合后,加热可以产生
的盐与强碱混合后,加热可以产生 。
。
(1)该溶液中一定含有___________ ;可能含有___________ ,可以用定性分析操作___________ 来进行检验。若含有,现象是:___________ 。
(2)计算:该 溶液中,若
溶液中,若 ,则
,则
___________ 。
(3)已知 与
与 在溶液中“相遇”时会产生红褐色沉淀和无色气泡,写出相应的离子方程式
在溶液中“相遇”时会产生红褐色沉淀和无色气泡,写出相应的离子方程式___________ ;当某溶液 中大量存在
中大量存在 时,
时, 溶液中不可能大量含有
溶液中不可能大量含有___________ 。
a. b.
b.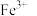 c.
c. d.
d. e.
e.
 、
、 、
、 、
、 、
、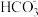 、
、 中的几种。为了确定其组成,现做以下实验:
中的几种。为了确定其组成,现做以下实验:①取该溶液
 ,加入足量的
,加入足量的 溶液,加热,得到标况下
溶液,加热,得到标况下 气体;同时产生红褐色沉淀,过滤,洗涤,干燥得到
气体;同时产生红褐色沉淀,过滤,洗涤,干燥得到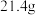 固体。
固体。②向上述滤液中加入足量的
 溶液,产生白色沉淀,过滤,洗涤,干燥得到
溶液,产生白色沉淀,过滤,洗涤,干燥得到 固体。
固体。已知:含
 的盐与强碱混合后,加热可以产生
的盐与强碱混合后,加热可以产生 。
。(1)该溶液中一定含有
(2)计算:该
 溶液中,若
溶液中,若 ,则
,则
(3)已知
 与
与 在溶液中“相遇”时会产生红褐色沉淀和无色气泡,写出相应的离子方程式
在溶液中“相遇”时会产生红褐色沉淀和无色气泡,写出相应的离子方程式 中大量存在
中大量存在 时,
时, 溶液中不可能大量含有
溶液中不可能大量含有a.
 b.
b.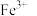 c.
c. d.
d. e.
e.
您最近一年使用:0次
2021-11-21更新
|
263次组卷
|
2卷引用:湖北省鄂东南省级示范高中教育教学改革联盟学校2021-2022学年高一上学期期中联考化学试题
10 . 某化学小组对当地化工厂排出的废水成分进行研究,经检测,废水呈酸性,且其中含有大量 、
、 、
、 、
、 、
、 。除去废水样品中的
。除去废水样品中的 和
和 ,回收NaCl、
,回收NaCl、 的实验流程如下。
的实验流程如下。

已知:NaCl、 在不同温度下的溶解度如下(g/100g水)。
在不同温度下的溶解度如下(g/100g水)。
回答下列问题:
(1)下列离子一定不能大量存在于该废水中的是___________(填标号)
(2)蓝色沉淀的成分是___________ (填化学式,下同);试剂c为___________ ,“操作2”需用到的玻璃仪器主要有烧杯、___________ 。
(3)向“溶液2”中加入盐酸,发生反应的离子方程式为___________ 。
(4)“溶液3”中溶质为NaCl、 ,操作3为___________(填编号)。
,操作3为___________(填编号)。
 、
、 、
、 、
、 、
、 。除去废水样品中的
。除去废水样品中的 和
和 ,回收NaCl、
,回收NaCl、 的实验流程如下。
的实验流程如下。
已知:NaCl、
 在不同温度下的溶解度如下(g/100g水)。
在不同温度下的溶解度如下(g/100g水)。| 温度物质 |  | NaCl |
| 10℃ | 80.5 | 35.7 |
| 100℃ | 175 | 39.1 |
(1)下列离子一定不能大量存在于该废水中的是___________(填标号)
A. | B. | C. | D. |
(3)向“溶液2”中加入盐酸,发生反应的离子方程式为
(4)“溶液3”中溶质为NaCl、
 ,操作3为___________(填编号)。
,操作3为___________(填编号)。| A.蒸发结晶 | B.蒸发浓缩、趁热过滤 | C.冷却结晶 | D.蒸发浓缩、冷却结晶 |
您最近一年使用:0次



