名校
1 . 某无色溶液可能含有 、
、 、
、 、
、 、
、 、
、 中的一种或几种离子。
中的一种或几种离子。
①向此溶液中滴加稀盐酸无明显现象。
②取少量①的溶液加入少量的Na2SO4溶液,有白色沉淀产生。
③取②的上层清液并加入过量的NaOH溶液,无明显现象。
(1)原溶液中一定含有的离子是_______ ,一定不含有的离子是_____ ,不能确定是否含有的离子是_______ ,可以用______ 检验此离子。
(2)②中反应的离子方程式为__________ 。
 、
、 、
、 、
、 、
、 、
、 中的一种或几种离子。
中的一种或几种离子。①向此溶液中滴加稀盐酸无明显现象。
②取少量①的溶液加入少量的Na2SO4溶液,有白色沉淀产生。
③取②的上层清液并加入过量的NaOH溶液,无明显现象。
(1)原溶液中一定含有的离子是
(2)②中反应的离子方程式为
您最近一年使用:0次
解题方法
2 . 利用分类法研究化学物质可系统、全面认识物质的性质。
Ⅰ.下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、 、
、 、CuO
、CuO
②HCl、 、
、 、
、
③NaOH、 、KOH、
、KOH、
(1)三种物质依次是(填化学式):①___________ ;②___________ ;③___________ 。
Ⅱ.有一无色酸性溶液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中一种或几种,已知:
中一种或几种,已知: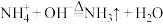 ,
, 为有刺激性气味的气体,为确定其成分,做如下实验:
为有刺激性气味的气体,为确定其成分,做如下实验:
①取部分溶液,加入足量 固体,产生无色无味的气体和白色沉淀;
固体,产生无色无味的气体和白色沉淀;
②另取部分溶液,加入过量的 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;
③取反应②后的部分溶液,加入硝酸酸化的硝酸银溶液,有白色沉淀生成。
(2)则原溶液中一定含有的离子是___________ ,一定不含有的离子是___________ 。
(3)写出①中 与水反应的离子方程式
与水反应的离子方程式___________ 。
Ⅲ.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有 、
、 、
、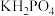 、
、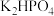 等。已知
等。已知 (次磷酸)与足量的NaOH反应只生成一种盐
(次磷酸)与足量的NaOH反应只生成一种盐 ,
, 水溶液中存在
水溶液中存在 分子。
分子。
(4) 属于
属于___________ 酸; 为盐
为盐___________ (填序号)。
①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(5)写出 溶液与足量NaOH溶液反应的离子方程式
溶液与足量NaOH溶液反应的离子方程式___________ 。
(6) 可将溶液中的
可将溶液中的 转化为银,自身变为
转化为银,自身变为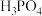 ,可用于化学镀银。利用
,可用于化学镀银。利用 进行化学镀银的反应中,氧化剂与还原剂的个数比为
进行化学镀银的反应中,氧化剂与还原剂的个数比为___________ 。
Ⅰ.下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、
 、
、 、CuO
、CuO②HCl、
 、
、 、
、
③NaOH、
 、KOH、
、KOH、
(1)三种物质依次是(填化学式):①
Ⅱ.有一无色酸性溶液中可能含有
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中一种或几种,已知:
中一种或几种,已知: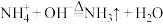 ,
, 为有刺激性气味的气体,为确定其成分,做如下实验:
为有刺激性气味的气体,为确定其成分,做如下实验:①取部分溶液,加入足量
 固体,产生无色无味的气体和白色沉淀;
固体,产生无色无味的气体和白色沉淀;②另取部分溶液,加入过量的
 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;③取反应②后的部分溶液,加入硝酸酸化的硝酸银溶液,有白色沉淀生成。
(2)则原溶液中一定含有的离子是
(3)写出①中
 与水反应的离子方程式
与水反应的离子方程式Ⅲ.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有
 、
、 、
、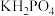 、
、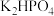 等。已知
等。已知 (次磷酸)与足量的NaOH反应只生成一种盐
(次磷酸)与足量的NaOH反应只生成一种盐 ,
, 水溶液中存在
水溶液中存在 分子。
分子。(4)
 属于
属于 为盐
为盐①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(5)写出
 溶液与足量NaOH溶液反应的离子方程式
溶液与足量NaOH溶液反应的离子方程式(6)
 可将溶液中的
可将溶液中的 转化为银,自身变为
转化为银,自身变为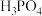 ,可用于化学镀银。利用
,可用于化学镀银。利用 进行化学镀银的反应中,氧化剂与还原剂的个数比为
进行化学镀银的反应中,氧化剂与还原剂的个数比为
您最近一年使用:0次
3 . 沈阳市位于辽宁省东北部,是中国重要的工业城市之一、随着城市的不断发展和人口的增加,污水处理厂的作用也愈加重要。在垃圾清理、路面施工以及工厂废水排放等方面都会产生大量的废水。某Y形河流上游两旁有甲、乙两个化工厂,其位置如图所示。经某化学课外活动小组检测,已知它们排放的工业废水中,共含 ,
, 、
、 ,
, ,
, ,
, 六种离子。若甲、乙两厂分别含有不同的三种离子,请回答下列问题:
六种离子。若甲、乙两厂分别含有不同的三种离子,请回答下列问题:
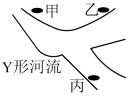
(1)经该小组检测,甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是___________ (填离子符号)。
(2)该小组认为,乙厂的废水中含有另外三种离子,如果加适量的___________ (填“活性炭”“硫酸亚铁”或“铁粉”),不但可以回收其中的一种金属,达到变废为宝的目的,还可以降低重金属离子污染,这个过程用离子方程式表示为___________ 。
(3)该小组有一个设想,建议甲厂和乙厂联合起来,把废水按适当比例混合,这样可以使废水中的___________ (填离子符号)结合转化为沉淀。再在丙地建立一个灌溉站,将过滤后的河水用来浇灌农田。他们的理由是经过滤后的废水主要含___________ (填化学式),可以促进农作物的生长,你认为他们的方案是否可行,并写出理由:___________ 。
 ,
, 、
、 ,
, ,
, ,
, 六种离子。若甲、乙两厂分别含有不同的三种离子,请回答下列问题:
六种离子。若甲、乙两厂分别含有不同的三种离子,请回答下列问题:
(1)经该小组检测,甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是
(2)该小组认为,乙厂的废水中含有另外三种离子,如果加适量的
(3)该小组有一个设想,建议甲厂和乙厂联合起来,把废水按适当比例混合,这样可以使废水中的
您最近一年使用:0次
4 . 某校化学兴趣小组同学猜想自来水中可能含有大量Cu2+、Ca2+、Mg2+和某些阴离子,从而进行了三组实验:
①取适量自来水于试管中,滴加足量的NaOH溶液,产生白色沉淀;
②过滤后取滤液于试管中,滴加足量的Na2CO3溶液,又有白色沉淀生成;
③另取适量自来水于试管中,滴加足量稀硝酸后再滴加AgNO3溶液,也产生白色沉淀。
请回答以下问题:
(1)不用做实验就可排除的离子是___________ 。
(2)通过实验可初步确定自来水中___________ (填“含有”或“不含有”)大量Ca2+、Mg2+;判断依据的离子方程式有___________ 。
(3)自来水中所含阴离子可以确定有___________ ,理由是___________ 。
(4)确定实验②中滴加的Na2CO3溶液已过量的检验方法是___________ 。
①取适量自来水于试管中,滴加足量的NaOH溶液,产生白色沉淀;
②过滤后取滤液于试管中,滴加足量的Na2CO3溶液,又有白色沉淀生成;
③另取适量自来水于试管中,滴加足量稀硝酸后再滴加AgNO3溶液,也产生白色沉淀。
请回答以下问题:
(1)不用做实验就可排除的离子是
(2)通过实验可初步确定自来水中
(3)自来水中所含阴离子可以确定有
(4)确定实验②中滴加的Na2CO3溶液已过量的检验方法是
您最近一年使用:0次
2023-10-08更新
|
160次组卷
|
19卷引用:辽宁省朝阳市柳城高中2019-2020学年高一上学期期中考试化学试题
辽宁省朝阳市柳城高中2019-2020学年高一上学期期中考试化学试题第2章《元素与物质世界》期中复习检测试卷2019年10月16日《每日一题》2019-2020学年高一化学人教必修1——常见离子的检验步步为赢 高一化学寒假作业:作业七 阶段检测(二)天津市西青区2019-2020学年高一上学期期末考试化学试题广东省揭阳市第三中学2020-2021学年高一上学期第一次阶段考化学试题(已下线)【浙江新东方】39天津市东丽区2020-2021学年高一上学期期末考试化学试题(已下线)专题3 从海水中获得的化学物质 综合评价-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)湖南师范大学附属中学2020-2021学年高一下学期期末考试化学试题天津市西青区杨柳青第一中学2021-2022学年高一下学期期末适应性测试化学试题云南省昆明市第十中学2021-2022学年高一上学期10月月考化学试题广东省梅州市兴宁市叶塘中学2021-2022学年高一上学期摸底考试化学试题贵州省贵阳市花溪第六中学2022-2023学年高一上学期期中考试化学试题安徽亳州市利辛县启明中学2022-2023学年高一上学期期末考试化学试题陕西省商洛市洛南中学2022-2023学年高一上学期12月月考化学试题甘肃省兰州市教育局第四片区联考2023-2024学年高一上学期期中考试化学试题新疆石河子第一中学2023-2024学年高一上学期9月月考化学试题(已下线)BBWYhjhx1001.pdf
名校
解题方法
5 . 经检测,某化工厂排出的废水呈酸性,且其中含有大量  、
、 、
、 、
、 、
、 。回答下列问题:
。回答下列问题:
(1)下列离子中,能大量存在于该废水中的是_______ 填标号
填标号
(2)取 该废水于烧杯,逐滴加入
该废水于烧杯,逐滴加入 溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是
溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是 、
、____  用离子符号表示
用离子符号表示 。
。
(3)某化学社团小组成员欲除去废水样品中的 和
和 ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图:

 试剂
试剂 为
为_______  写化学式
写化学式 ;溶液
;溶液 所含溶质离子有
所含溶质离子有 、
、________ 。
 “分离操作”的名称是
“分离操作”的名称是______ ,需用到的玻璃仪器主要有______ 。
 向“白色沉淀
向“白色沉淀 ”中加入足量盐酸,发生反应的离子方程式为
”中加入足量盐酸,发生反应的离子方程式为______ 。
 、
、 、
、 、
、 、
、 。回答下列问题:
。回答下列问题:(1)下列离子中,能大量存在于该废水中的是_______
 填标号
填标号
A. | B. | C. | D. |
 该废水于烧杯,逐滴加入
该废水于烧杯,逐滴加入 溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是
溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是 、
、 用离子符号表示
用离子符号表示 。
。(3)某化学社团小组成员欲除去废水样品中的
 和
和 ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图:
 试剂
试剂 为
为 写化学式
写化学式 ;溶液
;溶液 所含溶质离子有
所含溶质离子有 、
、 “分离操作”的名称是
“分离操作”的名称是 向“白色沉淀
向“白色沉淀 ”中加入足量盐酸,发生反应的离子方程式为
”中加入足量盐酸,发生反应的离子方程式为
您最近一年使用:0次
2023-07-30更新
|
531次组卷
|
8卷引用:辽宁省实验中学2021-2022学年高一上学期11月期中阶段测试化学试题
6 . 现有失去标签的氯化钙、硝酸银、盐酸、碳酸钠的四种无色溶液,为了测定四种溶液各是什么?将它们随意编号为A、B、C、D后,按下表进行实验。产生的现象如表所示:
回答下列问题:
(1)A、C溶液中分散质的化学式:A:___________ ;C:___________ 。
(2)写出实验顺序②③中有关的离子反应方程式。
②___________ 。
③___________ 。
(3)写出下列反应的离子方程式:向NaHSO4溶液逐滴加Ba(OH)2溶液至SO 刚好沉淀完全:
刚好沉淀完全:___________ 。
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 没有现象发生 |
| ② | B+D | 有气体放出 |
| ③ | B+C | 有沉淀生成 |
| ④ | A+D | 有沉淀生成 |
(1)A、C溶液中分散质的化学式:A:
(2)写出实验顺序②③中有关的离子反应方程式。
②
③
(3)写出下列反应的离子方程式:向NaHSO4溶液逐滴加Ba(OH)2溶液至SO
 刚好沉淀完全:
刚好沉淀完全:
您最近一年使用:0次
7 . 请回答下列问题:
(1)应对新冠肺炎疫情,“84消毒液”是生活中常用的消毒剂。某化学小组配制了500mL“84消毒液”,并在试剂瓶上贴上如图所示标签。
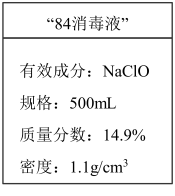
①该“84消毒液”有效成分的物质的量浓度为_______  。
。
②下列说法正确的有_______ 。
A.配制过程只需要四种仪器即可完成
B.容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制
C.所配得的NaClO消毒液在空气中光照,久置后溶液中的NaClO的物质的量浓度减小
D.上下颠倒摇匀后发现溶液凹液面低于刻度线,应再加水至刻度线
E.定容时,若加水超过刻度线,应重新配制溶液
F.定容时,若俯视刻度线,会使所配制溶液浓度偏低
③“消毒液”中氯元素的存在形态与溶液pH的关系如表:
请写出pH降低时产生氯气的离子方程式_______ 。
(2)下列各组物质相互混合反应后,最终有白色沉淀生成的是_______ (填序号)。
①金属钠投入到 溶液中
溶液中
② 和足量稀盐酸溶液混合
和足量稀盐酸溶液混合
③少量 投入过量
投入过量 溶液中
溶液中
④氯化钙溶液中通入少量的
⑤向饱和 溶液中通入足量
溶液中通入足量
⑥向 溶液中通入足量
溶液中通入足量 溶液
溶液
(3)汽车剧烈碰撞时安全气囊中发生如下反应: ,若氧化产物比还原产物多19.6g,则反应生成的
,若氧化产物比还原产物多19.6g,则反应生成的 在标况下的体积为
在标况下的体积为_______ L。
(4)某溶液可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种离子,已知各离子的物质的量浓度均相等,进行如下实验:
中的几种离子,已知各离子的物质的量浓度均相等,进行如下实验:
Ⅰ.取少量该溶液,加入足量稀硫酸,无明显现象。
Ⅱ.取实验Ⅰ反应后的溶液,加入足量浓NaOH溶液,最终得到红褐色沉淀,并伴有刺激性气味气体产生(该气体为 )。
)。
①该溶液中肯定存在的离子有_______ 。
②若取原溶液进行焰色试验,焰色显黄色,则溶液中一定存在的离子有_______ 种。
(1)应对新冠肺炎疫情,“84消毒液”是生活中常用的消毒剂。某化学小组配制了500mL“84消毒液”,并在试剂瓶上贴上如图所示标签。

①该“84消毒液”有效成分的物质的量浓度为
 。
。②下列说法正确的有
A.配制过程只需要四种仪器即可完成
B.容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制
C.所配得的NaClO消毒液在空气中光照,久置后溶液中的NaClO的物质的量浓度减小
D.上下颠倒摇匀后发现溶液凹液面低于刻度线,应再加水至刻度线
E.定容时,若加水超过刻度线,应重新配制溶液
F.定容时,若俯视刻度线,会使所配制溶液浓度偏低
③“消毒液”中氯元素的存在形态与溶液pH的关系如表:
| 溶液pH | >9 | 5~6 | 4~5 | 2~3 | <2 |
| 主要成分 | NaClO | HCl与NaClO(少量) | HCl与 (少量) (少量) | HClO与 |  |
(2)下列各组物质相互混合反应后,最终有白色沉淀生成的是
①金属钠投入到
 溶液中
溶液中②
 和足量稀盐酸溶液混合
和足量稀盐酸溶液混合③少量
 投入过量
投入过量 溶液中
溶液中④氯化钙溶液中通入少量的

⑤向饱和
 溶液中通入足量
溶液中通入足量
⑥向
 溶液中通入足量
溶液中通入足量 溶液
溶液(3)汽车剧烈碰撞时安全气囊中发生如下反应:
 ,若氧化产物比还原产物多19.6g,则反应生成的
,若氧化产物比还原产物多19.6g,则反应生成的 在标况下的体积为
在标况下的体积为(4)某溶液可能含有
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种离子,已知各离子的物质的量浓度均相等,进行如下实验:
中的几种离子,已知各离子的物质的量浓度均相等,进行如下实验:Ⅰ.取少量该溶液,加入足量稀硫酸,无明显现象。
Ⅱ.取实验Ⅰ反应后的溶液,加入足量浓NaOH溶液,最终得到红褐色沉淀,并伴有刺激性气味气体产生(该气体为
 )。
)。①该溶液中肯定存在的离子有
②若取原溶液进行焰色试验,焰色显黄色,则溶液中一定存在的离子有
您最近一年使用:0次
2023-01-04更新
|
631次组卷
|
3卷引用:辽宁省重点高中2022-2023学年高一上学期期末联考化学试题
解题方法
8 . 有一瓶100mL的无色透明溶液,只含有Cl-、HCO 、CO
、CO 、SO
、SO 、H+、Na+、Mg2+、K+、Cu2+中的某几种,且它们的物质的量浓度相同。分别取两份10mL该溶液于试管I、II中,做如下实验:
、H+、Na+、Mg2+、K+、Cu2+中的某几种,且它们的物质的量浓度相同。分别取两份10mL该溶液于试管I、II中,做如下实验:
①实验一:试管I中,加入一小块去除表面氧化膜的金属Al,有气泡产生;
②实验二:试管II中,加入足量的NaOH溶液,产生白色沉淀。
回答下列问题:
(1)仅通过观察就可以判断原溶液中不存在的离子是_______ (写离子符号)。
(2)由实验一可知原溶液中一定不含有的离子是_______ (写离子符号)。
(3)根据上述实验可以推出,原溶液中__________________ Cl-、SO ,
,______________ Na+、K+ (填“一定含有”、“一定不含”、“无法确定”)
 、CO
、CO 、SO
、SO 、H+、Na+、Mg2+、K+、Cu2+中的某几种,且它们的物质的量浓度相同。分别取两份10mL该溶液于试管I、II中,做如下实验:
、H+、Na+、Mg2+、K+、Cu2+中的某几种,且它们的物质的量浓度相同。分别取两份10mL该溶液于试管I、II中,做如下实验:①实验一:试管I中,加入一小块去除表面氧化膜的金属Al,有气泡产生;
②实验二:试管II中,加入足量的NaOH溶液,产生白色沉淀。
回答下列问题:
(1)仅通过观察就可以判断原溶液中不存在的离子是
(2)由实验一可知原溶液中一定不含有的离子是
(3)根据上述实验可以推出,原溶液中
 ,
,
您最近一年使用:0次
解题方法
9 . Ⅰ.现有以下物质:①盐酸②液氨③BaCO3固体④熔融 K2SO4⑤氢氧化铁胶体⑥蔗糖⑦CO2⑧NaOH 溶液。按要求回答问题:
(1)属于非电解质的是___________ (填序号),电解质的是___________ (填序号)
(2)⑤的实验室制备方法:向沸水中滴加几滴饱和 FeCl3溶液,加热至液体呈红褐色,停止加热;其化学方程式为___________ 。
Ⅱ.某未知溶液中只可能大量存在下列离子:Na+、Ba2+、 、
、 、Cl-、H+,为探究其组成,某实验小组进行了以下实验:
、Cl-、H+,为探究其组成,某实验小组进行了以下实验:

(3)写出“沉淀2”的化学式___________ ;
(4)“沉淀1”与稀盐酸反应的离子方程式为___________ ;
(5)原溶液中一定大量存在的离子是___________ ,可能存在的离子是___________ 。
(1)属于非电解质的是
(2)⑤的实验室制备方法:向沸水中滴加几滴饱和 FeCl3溶液,加热至液体呈红褐色,停止加热;其化学方程式为
Ⅱ.某未知溶液中只可能大量存在下列离子:Na+、Ba2+、
 、
、 、Cl-、H+,为探究其组成,某实验小组进行了以下实验:
、Cl-、H+,为探究其组成,某实验小组进行了以下实验:
(3)写出“沉淀2”的化学式
(4)“沉淀1”与稀盐酸反应的离子方程式为
(5)原溶液中一定大量存在的离子是
您最近一年使用:0次
2022-12-13更新
|
280次组卷
|
3卷引用:辽宁省辽西联合校2023-2024学年高三上学期期中考试化学试题
名校
解题方法
10 . 现有下列几种物质:
①氯气②蔗糖固体③FeSO4∙7H2O④熔融CaO⑤NaHCO3溶液⑥CO2⑦Ba(OH)2固体
(1)上述物质属于电解质的有___________ (填序号,下同),属于非电解质的有___________ 。
(2)写出少量CO2通入澄清石灰水反应的离子方程式:___________ 。
(3) NaHCO3溶液与NaHSO4溶液反应的离子方程式为:___________ 。
(4)氯气与水反应的离子方程式为:___________ 。
(5)向Ba(OH)2溶液中逐渐加入A溶液时,溶液导电性的变化趋势如图所示:

滴加溶液A至图中曲线最低点时,灯泡熄灭,则溶液A中的溶质是___________(填标号)。
①氯气②蔗糖固体③FeSO4∙7H2O④熔融CaO⑤NaHCO3溶液⑥CO2⑦Ba(OH)2固体
(1)上述物质属于电解质的有
(2)写出少量CO2通入澄清石灰水反应的离子方程式:
(3) NaHCO3溶液与NaHSO4溶液反应的离子方程式为:
(4)氯气与水反应的离子方程式为:
(5)向Ba(OH)2溶液中逐渐加入A溶液时,溶液导电性的变化趋势如图所示:

滴加溶液A至图中曲线最低点时,灯泡熄灭,则溶液A中的溶质是___________(填标号)。
| A.HCl | B. NaHSO4 | C. H2SO4 | D. Na2SO4 |
您最近一年使用:0次



