1 . 回答下列问题:
I.某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是_______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子所发生的离子方程式_______ 。
(3)取(2)中的滤液,加入过量的NaOH出现白色沉淀,说明原溶液中肯定有的该离子所发生的离子方程式为_______ 。
(4)通过以上实验确定原溶液中一定含有的阳离子是_______ ,不能确定的阳离子是_______ 。
(5)原溶液可能大量存在的阴离子是下列的_______。
II.现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
(6)同温同压下,M、N气体的密度之比为_______ 。
(7)相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为_______ 。
I.某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子所发生的离子方程式
(3)取(2)中的滤液,加入过量的NaOH出现白色沉淀,说明原溶液中肯定有的该离子所发生的离子方程式为
(4)通过以上实验确定原溶液中一定含有的阳离子是
(5)原溶液可能大量存在的阴离子是下列的_______。
| A.Cl- | B.NO | C.CO | D.OH- |
II.现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
(6)同温同压下,M、N气体的密度之比为
(7)相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为
您最近一年使用:0次
名校
2 . 按要求完成下列填空。
(1)某无色溶液可能含有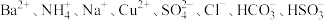 等离子。设计如下实验确定其组成:
等离子。设计如下实验确定其组成:

①加入足量 发生反应的离子方程式有
发生反应的离子方程式有___________ 。
②溶液中一定存在的离子有___________ 。
(2)四甲基氢氧化铵是一种弱碱,常用于极谱分析,以四甲基氯化铵为原料通过电解获取四甲基氢氧化铵,工作原理如图。
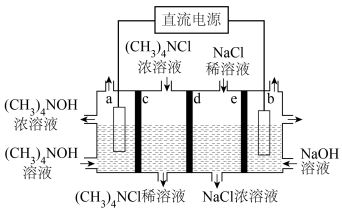
①a极的电极反应式为___________
②c为___________ (“阳离子交换”或“阴离子交换”,下同)膜,d为___________ 膜。
③a、b两极共产生标准状况下3.36L气体,理论可得四甲基氢氧化铵的质量为___________ 。
(1)某无色溶液可能含有
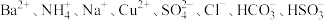 等离子。设计如下实验确定其组成:
等离子。设计如下实验确定其组成:
①加入足量
 发生反应的离子方程式有
发生反应的离子方程式有②溶液中一定存在的离子有
(2)四甲基氢氧化铵是一种弱碱,常用于极谱分析,以四甲基氯化铵为原料通过电解获取四甲基氢氧化铵,工作原理如图。

①a极的电极反应式为
②c为
③a、b两极共产生标准状况下3.36L气体,理论可得四甲基氢氧化铵的质量为
您最近一年使用:0次
名校
解题方法
3 . I.已知下列十种物质①CH3COOH ②Cu ③NO ④干冰 ⑤硫酸 ⑥Ba(OH)2 ⑦Fe(OH)3胶体 ⑧液氨 ⑨稀硝酸 ⑩KAl(SO4)2。根据上述提供的物质,回答下列问题
(1)属于电解质的是___________ (填序号,下同),属于非电解质的是___________
在熔融状态下不导电而在水溶液下导电的电解质是___________
(2)写出KAl(SO4)2的电离方程式___________
Ⅱ.有aA、B、C、D四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别是 、
、 、
、 、
、 中的一种(离子在物质中不重复出现)。
中的一种(离子在物质中不重复出现)。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
(3)A的化学式为___________ ,B的化学式为___________
(4)写出D与足量硫酸溶液反应的离子方程式___________
(5)写出A溶液中阴离子的检验方法___________
(1)属于电解质的是
在熔融状态下不导电而在水溶液下导电的电解质是
(2)写出KAl(SO4)2的电离方程式
Ⅱ.有aA、B、C、D四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别是
 、
、 、
、 、
、 中的一种(离子在物质中不重复出现)。
中的一种(离子在物质中不重复出现)。①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
(3)A的化学式为
(4)写出D与足量硫酸溶液反应的离子方程式
(5)写出A溶液中阴离子的检验方法
您最近一年使用:0次
4 . 有一包白色固体,可能含有 、
、 、KCl、
、KCl、 和无水
和无水 ,按下列步骤做实验:
,按下列步骤做实验:
①将该白色固体溶于水,得到无色溶液;
②向所得的无色溶液中加入足量 溶液,得到白色沉淀,再加稀硝酸,白色沉淀部分溶解并有气泡产生,将气体通入澄清石灰水中,石灰水变浑浊。
溶液,得到白色沉淀,再加稀硝酸,白色沉淀部分溶解并有气泡产生,将气体通入澄清石灰水中,石灰水变浑浊。
回答下列问题:
(1)该白色固体中一定存在的物质是___________ ,一定不存在的物质是___________ ,可能存在的物质是___________ 。
(2)称取该白色固体3.53 g,将其溶于水得到溶液A,在A中加入50 mL未知的 溶液恰好完全反应,过滤得沉淀B,向B中加入足量稀硝酸,充分反应后剩余沉淀2.87g,同时放出0.224 L气体(标准状况)。
溶液恰好完全反应,过滤得沉淀B,向B中加入足量稀硝酸,充分反应后剩余沉淀2.87g,同时放出0.224 L气体(标准状况)。
①该白色固体中 的质量分数为
的质量分数为___________ (保留2位有效数字,下同)。
② 溶液中溶质的物质的量浓度为
溶液中溶质的物质的量浓度为___________ 。
③该白色固体的成分是___________ 。
 、
、 、KCl、
、KCl、 和无水
和无水 ,按下列步骤做实验:
,按下列步骤做实验:①将该白色固体溶于水,得到无色溶液;
②向所得的无色溶液中加入足量
 溶液,得到白色沉淀,再加稀硝酸,白色沉淀部分溶解并有气泡产生,将气体通入澄清石灰水中,石灰水变浑浊。
溶液,得到白色沉淀,再加稀硝酸,白色沉淀部分溶解并有气泡产生,将气体通入澄清石灰水中,石灰水变浑浊。回答下列问题:
(1)该白色固体中一定存在的物质是
(2)称取该白色固体3.53 g,将其溶于水得到溶液A,在A中加入50 mL未知的
 溶液恰好完全反应,过滤得沉淀B,向B中加入足量稀硝酸,充分反应后剩余沉淀2.87g,同时放出0.224 L气体(标准状况)。
溶液恰好完全反应,过滤得沉淀B,向B中加入足量稀硝酸,充分反应后剩余沉淀2.87g,同时放出0.224 L气体(标准状况)。①该白色固体中
 的质量分数为
的质量分数为②
 溶液中溶质的物质的量浓度为
溶液中溶质的物质的量浓度为③该白色固体的成分是
您最近一年使用:0次
2023-11-03更新
|
192次组卷
|
3卷引用: 2023-2024学年高一上学期化学人教版(2019)必修第一册 期末考试练习题
(已下线) 2023-2024学年高一上学期化学人教版(2019)必修第一册 期末考试练习题山东省聊城市临清市第一中学2023-2024学年高一上学期期末模拟考试化学试题甘肃省平凉市静宁县2023-2024学年高三上学期11月月考化学试题
5 . 食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含有少量 、
、 、
、 、
、 等杂质离子,实验室提纯
等杂质离子,实验室提纯 的流程如图。
的流程如图。
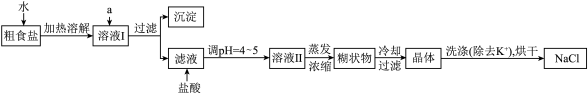
提供的试剂:饱和 溶液、饱和
溶液、饱和 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液、75%的乙醇溶液、四氯化碳
溶液、75%的乙醇溶液、四氯化碳
①欲除去溶液Ⅰ中的 、
、 、
、 ,选出a所代表的试剂,按滴加顺序依次是
,选出a所代表的试剂,按滴加顺序依次是___________ (填字母)。
a. 、
、 、
、 b.
b. 、
、 、
、
c. 、
、 、
、 d.
d. 、
、 、
、
②加盐酸调 的目的是
的目的是___________ 。
③洗涤除去 晶体表面附带的少量
晶体表面附带的少量 ,选用的试剂为
,选用的试剂为___________ 。
(2)某加碘盐中可能含有 、
、 、
、 、
、 、
、 (已知氧化性:
(已知氧化性: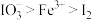 )。某研究小组对该加碘盐进行如下实验,以确定该加碘盐中碘元素的存在形式。取一定量的加碘盐,用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3等份。
)。某研究小组对该加碘盐进行如下实验,以确定该加碘盐中碘元素的存在形式。取一定量的加碘盐,用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3等份。
第一份试液中滴加 溶液后显红色;
溶液后显红色;
第二份试液中加足量 固体,溶液显淡黄色,再加入
固体,溶液显淡黄色,再加入 ,下层溶液显紫红色;
,下层溶液显紫红色;
第三份试液中加入适量 固体后,滴加淀粉试剂,溶液不变色。
固体后,滴加淀粉试剂,溶液不变色。
根据这三次实验,回答下列问题:
①第二份试液中加入足量KI固体后,反应的离子方程式为___________ 、 。
。
②在该加碘盐中,除了 、
、 以外,一定存在的离子是
以外,一定存在的离子是___________ ,一定不存在的离子是___________ 。
③ 作为食盐的加碘剂,在保存过程中由于空气中氧气的作用,容易引起碘的损失。写出潮湿环境下
作为食盐的加碘剂,在保存过程中由于空气中氧气的作用,容易引起碘的损失。写出潮湿环境下 与氧气反应的化学方程式:
与氧气反应的化学方程式:___________ 。对含 较多的食盐(假设不含
较多的食盐(假设不含 ),可选用
),可选用 作为加碘剂。请设计实验方案,检验该加碘盐中的
作为加碘剂。请设计实验方案,检验该加碘盐中的 的方法:
的方法:___________ 。
(1)粗食盐常含有少量
 、
、 、
、 、
、 等杂质离子,实验室提纯
等杂质离子,实验室提纯 的流程如图。
的流程如图。
提供的试剂:饱和
 溶液、饱和
溶液、饱和 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液、75%的乙醇溶液、四氯化碳
溶液、75%的乙醇溶液、四氯化碳①欲除去溶液Ⅰ中的
 、
、 、
、 ,选出a所代表的试剂,按滴加顺序依次是
,选出a所代表的试剂,按滴加顺序依次是a.
 、
、 、
、 b.
b. 、
、 、
、
c.
 、
、 、
、 d.
d. 、
、 、
、
②加盐酸调
 的目的是
的目的是③洗涤除去
 晶体表面附带的少量
晶体表面附带的少量 ,选用的试剂为
,选用的试剂为(2)某加碘盐中可能含有
 、
、 、
、 、
、 、
、 (已知氧化性:
(已知氧化性: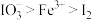 )。某研究小组对该加碘盐进行如下实验,以确定该加碘盐中碘元素的存在形式。取一定量的加碘盐,用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3等份。
)。某研究小组对该加碘盐进行如下实验,以确定该加碘盐中碘元素的存在形式。取一定量的加碘盐,用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3等份。第一份试液中滴加
 溶液后显红色;
溶液后显红色;第二份试液中加足量
 固体,溶液显淡黄色,再加入
固体,溶液显淡黄色,再加入 ,下层溶液显紫红色;
,下层溶液显紫红色;第三份试液中加入适量
 固体后,滴加淀粉试剂,溶液不变色。
固体后,滴加淀粉试剂,溶液不变色。根据这三次实验,回答下列问题:
①第二份试液中加入足量KI固体后,反应的离子方程式为
 。
。②在该加碘盐中,除了
 、
、 以外,一定存在的离子是
以外,一定存在的离子是③
 作为食盐的加碘剂,在保存过程中由于空气中氧气的作用,容易引起碘的损失。写出潮湿环境下
作为食盐的加碘剂,在保存过程中由于空气中氧气的作用,容易引起碘的损失。写出潮湿环境下 与氧气反应的化学方程式:
与氧气反应的化学方程式: 较多的食盐(假设不含
较多的食盐(假设不含 ),可选用
),可选用 作为加碘剂。请设计实验方案,检验该加碘盐中的
作为加碘剂。请设计实验方案,检验该加碘盐中的 的方法:
的方法:
您最近一年使用:0次
名校
解题方法
6 . 经检测,某化工厂排出的废水呈酸性,且其中含有大量  、
、 、
、 、
、 、
、 。回答下列问题:
。回答下列问题:
(1)下列离子中,能大量存在于该废水中的是_______ 填标号
填标号
(2)取 该废水于烧杯,逐滴加入
该废水于烧杯,逐滴加入 溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是
溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是 、
、____  用离子符号表示
用离子符号表示 。
。
(3)某化学社团小组成员欲除去废水样品中的 和
和 ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图:

 试剂
试剂 为
为_______  写化学式
写化学式 ;溶液
;溶液 所含溶质离子有
所含溶质离子有 、
、________ 。
 “分离操作”的名称是
“分离操作”的名称是______ ,需用到的玻璃仪器主要有______ 。
 向“白色沉淀
向“白色沉淀 ”中加入足量盐酸,发生反应的离子方程式为
”中加入足量盐酸,发生反应的离子方程式为______ 。
 、
、 、
、 、
、 、
、 。回答下列问题:
。回答下列问题:(1)下列离子中,能大量存在于该废水中的是_______
 填标号
填标号
A. | B. | C. | D. |
 该废水于烧杯,逐滴加入
该废水于烧杯,逐滴加入 溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是
溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是 、
、 用离子符号表示
用离子符号表示 。
。(3)某化学社团小组成员欲除去废水样品中的
 和
和 ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图:
 试剂
试剂 为
为 写化学式
写化学式 ;溶液
;溶液 所含溶质离子有
所含溶质离子有 、
、 “分离操作”的名称是
“分离操作”的名称是 向“白色沉淀
向“白色沉淀 ”中加入足量盐酸,发生反应的离子方程式为
”中加入足量盐酸,发生反应的离子方程式为
您最近一年使用:0次
2023-07-30更新
|
531次组卷
|
8卷引用:山东省青岛市黄岛区2020-2021学年高一上学期期中考试化学试题
7 . 现有一混合溶液,可能含有以下离子中的几种:Na+、Cu2+、Ba2+、Fe3+、CO 、SO
、SO 、Cl-。取100mL 溶液进行如下实验,回答下列问题。
、Cl-。取100mL 溶液进行如下实验,回答下列问题。

(1)气体I是_______ ,白色沉淀Ⅱ是_______ 。
(2)原溶液一定存在的离子有_______ ,可能存在的离子有_______ 。
(3)原溶液中 Na+浓度至少为_______ mol•L-1
 、SO
、SO 、Cl-。取100mL 溶液进行如下实验,回答下列问题。
、Cl-。取100mL 溶液进行如下实验,回答下列问题。
(1)气体I是
(2)原溶液一定存在的离子有
(3)原溶液中 Na+浓度至少为
您最近一年使用:0次
名校
解题方法
8 . 有一瓶无色溶液只含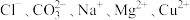 五种离子中的某几种。通过实验:
五种离子中的某几种。通过实验:
①原溶液中加足量 溶液产生白色沉淀;
溶液产生白色沉淀;
②原溶液中加 溶液不产生沉淀;
溶液不产生沉淀;
③原溶液中加 溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
(1)原溶液中一定含有的离子是_______ ,一定不含有的离子是_______ ,可能含有的离子是_______ 。
(2)实验③说明原溶液中含有_______ 。有的同学认为实验③可以省略,你认为是否正确(填“是”或“否”)_______ ,理由是_______ 。
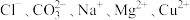 五种离子中的某几种。通过实验:
五种离子中的某几种。通过实验:①原溶液中加足量
 溶液产生白色沉淀;
溶液产生白色沉淀;②原溶液中加
 溶液不产生沉淀;
溶液不产生沉淀;③原溶液中加
 溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。(1)原溶液中一定含有的离子是
(2)实验③说明原溶液中含有
您最近一年使用:0次
解题方法
9 . 化学存在于我们的生活中,我们的衣食住行都和化学密切相关,完成下列问题。
(一)在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。现有一种无色的鲜花营养液,可能由硝酸钙、碳酸钾、硝酸钾、氯化钾中的一种或几种物质组成,为探究其成分,某同学设计并完成了如图所示的实验。

(1)由实验1可确定原营养液中一定没有的物质是_______ (填化学式),写出生成白色沉淀的化学方程式:_______ 。
(2)若测得原营养液中 、
、 的数目之比为2∶1,则原营养液是由
的数目之比为2∶1,则原营养液是由_______ 种溶质配制成的。某同学用氯化钙、硝酸钾、氯化钾配成的营养液中 、
、 、
、 的数目之比为2∶5∶1,则所用硝酸钾和氯化钙的物质的量之比是
的数目之比为2∶5∶1,则所用硝酸钾和氯化钙的物质的量之比是_______ 。
(二)明胶磷酸盐缓冲液可用于肉毒梭菌检样的制备、微生物分离和鉴定等。
(3)明胶是水溶性蛋白质混合物,由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶的水溶液和 溶液共同具备的性质是
溶液共同具备的性质是_______ (填字母)。
a.都不稳定,密封放置会产生沉淀
b.二者均有丁达尔效应
c.分散质粒子可通过滤纸
(4)磷元素的含氧酸有 、
、 (亚磷酸)、
(亚磷酸)、 (次磷酸)等多种酸。已知
(次磷酸)等多种酸。已知 (过量)
(过量)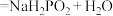 ,
, 属于
属于_______ (填“正盐”或“酸式盐”)。已知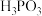 属于二元弱酸,写出它与足量NaOH溶液反应的离子方程式
属于二元弱酸,写出它与足量NaOH溶液反应的离子方程式_______ 。
(一)在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。现有一种无色的鲜花营养液,可能由硝酸钙、碳酸钾、硝酸钾、氯化钾中的一种或几种物质组成,为探究其成分,某同学设计并完成了如图所示的实验。

(1)由实验1可确定原营养液中一定没有的物质是
(2)若测得原营养液中
 、
、 的数目之比为2∶1,则原营养液是由
的数目之比为2∶1,则原营养液是由 、
、 、
、 的数目之比为2∶5∶1,则所用硝酸钾和氯化钙的物质的量之比是
的数目之比为2∶5∶1,则所用硝酸钾和氯化钙的物质的量之比是(二)明胶磷酸盐缓冲液可用于肉毒梭菌检样的制备、微生物分离和鉴定等。
(3)明胶是水溶性蛋白质混合物,由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶的水溶液和
 溶液共同具备的性质是
溶液共同具备的性质是a.都不稳定,密封放置会产生沉淀
b.二者均有丁达尔效应
c.分散质粒子可通过滤纸
(4)磷元素的含氧酸有
 、
、 (亚磷酸)、
(亚磷酸)、 (次磷酸)等多种酸。已知
(次磷酸)等多种酸。已知 (过量)
(过量)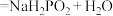 ,
, 属于
属于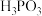 属于二元弱酸,写出它与足量NaOH溶液反应的离子方程式
属于二元弱酸,写出它与足量NaOH溶液反应的离子方程式
您最近一年使用:0次
名校
解题方法
10 . 电解质溶于水时会发生电离产生自由移动的离子,电导率变化一定程度上可以反映溶液中自由移动的离子浓度变化。在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。回答下列问题。
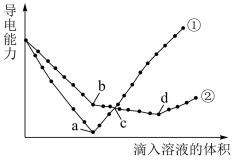
(1)NaHSO4在水溶液中的电离方程式是_______ ;NaHSO4属于“酸”、“碱”、“盐”中的_______ ;图中代表滴加NaHSO4溶液的变化曲线是_______ (填“①”或“②”)。
(2)曲线①中a点导电能力最弱的原因是_______ ;(用离子方程式表示),b点溶液中大量存在的离子是_______ 。
(3)c点两溶液中H+浓度:①_______ ②(填“>”、“<”或“=”,下同);d点对应的溶液显_______ (填“酸性”、“中性”、“碱性”)。
(4)曲线②中的b、d两点对应所加溶液的体积比为_______ 。

(1)NaHSO4在水溶液中的电离方程式是
(2)曲线①中a点导电能力最弱的原因是
(3)c点两溶液中H+浓度:①
(4)曲线②中的b、d两点对应所加溶液的体积比为
您最近一年使用:0次
2022-11-25更新
|
109次组卷
|
2卷引用:山东省枣庄滕州市第一中学西校2022-2023学年高一上学期第二次线上考试化学试题



