解题方法
1 . 用双氧水氧化法可处理电镀废水中的氰化物(CN-)和有机添加剂。一定pH下H2O2可使CN-转化为无害的 和N2。现向某废水中加入用量为1.02 mL/L的30%H2O2(密度为1.11 g/mL),处理前后CN-的质量浓度如下表所示,已知该废水中的有机添加剂的耗H2O2量为CN-的3倍。此外过量的H2O2需加入焦亚硫酸钠(Na2S2O5)还原除去。请计算需加入焦亚硫酸钠(Na2S2O5)的量为
和N2。现向某废水中加入用量为1.02 mL/L的30%H2O2(密度为1.11 g/mL),处理前后CN-的质量浓度如下表所示,已知该废水中的有机添加剂的耗H2O2量为CN-的3倍。此外过量的H2O2需加入焦亚硫酸钠(Na2S2O5)还原除去。请计算需加入焦亚硫酸钠(Na2S2O5)的量为___________ g/L,(不考虑H2O2的自身分解和溶液体积的变化)写出计算过程。
 和N2。现向某废水中加入用量为1.02 mL/L的30%H2O2(密度为1.11 g/mL),处理前后CN-的质量浓度如下表所示,已知该废水中的有机添加剂的耗H2O2量为CN-的3倍。此外过量的H2O2需加入焦亚硫酸钠(Na2S2O5)还原除去。请计算需加入焦亚硫酸钠(Na2S2O5)的量为
和N2。现向某废水中加入用量为1.02 mL/L的30%H2O2(密度为1.11 g/mL),处理前后CN-的质量浓度如下表所示,已知该废水中的有机添加剂的耗H2O2量为CN-的3倍。此外过量的H2O2需加入焦亚硫酸钠(Na2S2O5)还原除去。请计算需加入焦亚硫酸钠(Na2S2O5)的量为| 质量浓度(mg/L) | 处理前 | 处理后 |
| CN- | 5.41 | 0.21 |
您最近一年使用:0次
解题方法
2 . 汽车尾气排放出的气体主要有 和
和 ,它们污染环境,可用氨气除去,反应的化学方程式为:
,它们污染环境,可用氨气除去,反应的化学方程式为: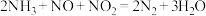 。若反应后得到
。若反应后得到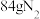 ,理论上需消耗氨气
,理论上需消耗氨气___________ L(标准状况),其中被 氧化的氨气又是
氧化的氨气又是___________  。
。
 和
和 ,它们污染环境,可用氨气除去,反应的化学方程式为:
,它们污染环境,可用氨气除去,反应的化学方程式为: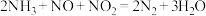 。若反应后得到
。若反应后得到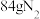 ,理论上需消耗氨气
,理论上需消耗氨气 氧化的氨气又是
氧化的氨气又是 。
。
您最近一年使用:0次
20-21高一上·浙江·期中
解题方法
3 . (1)现有以下物质:①NaCl溶液②干冰③Na2O固体④铜⑤BaSO4固体⑥蔗糖⑦液态HCl⑧熔融状态的KNO3,其中属于电解质的是_______ (填序号,下同),该状态下能导电的是_______ 。
(2)三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术创新必不可少的关键原料之一,可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F。则:上述反应中,氧化剂为_______ ,还原剂为_______ ,氧化剂与还原剂的物质的量之比为_______ ;若反应中有0.5molNH3被氧化,转移电子的数目为_______ 。
(3)某硫酸铝溶液的密度为1.20g·cm-3,其中铝离子的质量分数为5.4%,则300mL该溶液中SO 的物质的量为
的物质的量为_______
(4)标准状况下,将VL的氨气溶于1L的水中(密度为1g·cm-3),得到的溶液密度为ρg·cm-3,试求得到的氨水中溶质NH3的物质的量浓度为_______
(2)三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术创新必不可少的关键原料之一,可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F。则:上述反应中,氧化剂为
(3)某硫酸铝溶液的密度为1.20g·cm-3,其中铝离子的质量分数为5.4%,则300mL该溶液中SO
 的物质的量为
的物质的量为(4)标准状况下,将VL的氨气溶于1L的水中(密度为1g·cm-3),得到的溶液密度为ρg·cm-3,试求得到的氨水中溶质NH3的物质的量浓度为
您最近一年使用:0次



