2024·河北秦皇岛·二模
名校
1 . 实验室可利用反应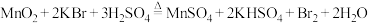 制备
制备 。设
。设 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是
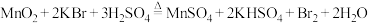 制备
制备 。设
。设 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是A.0℃、101kPa下,11.2L  所含的分子数为0.5 所含的分子数为0.5 |
B.0.1 的 的  溶液中含有的离子数为0.3 溶液中含有的离子数为0.3 |
C.常温常压下,9.8g  和9.8g 和9.8g  中含有的氧原子数均为0.4 中含有的氧原子数均为0.4 |
D.该反应中生成0.2mol  时,转移的电子数为0.2 时,转移的电子数为0.2 |
您最近一年使用:0次
解题方法
2 . 酸性条件下Na2S和Na2SO3发生反应: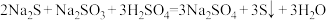 ,下列说法
,下列说法不正确 的是(设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
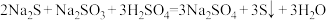 ,下列说法
,下列说法 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)A.生成24gS转移电子的数目为 | B.Na2S是还原剂,发生氧化反应 |
| C.Na2SO4是氧化产物 | D.碱性条件下S2-和 可以大量共存 可以大量共存 |
您最近一年使用:0次
3 . 高铁酸钾是一种新型的消毒剂,可以做到消毒、净水两用。高铁酸钾常用反应3ClO-+2Fe3++10OH-=2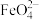 +3Cl-+5H2O制备,下列说法不正确的是
+3Cl-+5H2O制备,下列说法不正确的是
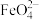 +3Cl-+5H2O制备,下列说法不正确的是
+3Cl-+5H2O制备,下列说法不正确的是A.生成1mol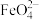 ,转移3mol电子 ,转移3mol电子 |
| B.高铁酸钾可以消毒净水两用是因其有强氧化性且生成胶体 |
| C.高铁酸钾消毒剂不能和洁厕灵混合 |
| D.氧化产物与还原产物物质的量之比为2:5 |
您最近一年使用:0次
名校
4 . 为避免硝酸生产尾气中的氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。后者常采用 作还原剂,其反应之一为:
作还原剂,其反应之一为: ,下列说法不正确的是(
,下列说法不正确的是( 为阿伏加德罗常数)
为阿伏加德罗常数)
 作还原剂,其反应之一为:
作还原剂,其反应之一为: ,下列说法不正确的是(
,下列说法不正确的是( 为阿伏加德罗常数)
为阿伏加德罗常数)| A.氧化产物与还原产物的质量比为3∶4 | B.生成 水转移电子的数目为 水转移电子的数目为 |
C.可使用 溶液吸收氮氧化物 溶液吸收氮氧化物 | D.氮氧化物的排放可形成酸雨 |
您最近一年使用:0次
解题方法
5 . 高铁酸钠是一种高效多功能水处理剂,工业上常采用次氯酸钠(NaClO)氧化法生产,反应原理为:NaClO+Fe(NO3)3+NaOH→Na2FeO4↓+NaCl+NaNO3+H2O(未配平)。若反应消耗了150.00mL 1.00 mol/L NaClO溶液(不考虑其他物质与Fe3+反应),则产物中高铁酸钠理论产量(单位:g)为
| A.8.3 | B.33.2 | C.16.6 | D.24.9 |
您最近一年使用:0次
名校
6 . 常温下,关于反应 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.该反应的还原产物是 |
B.每生成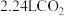 ,反应共转移 ,反应共转移 电子 电子 |
C.氧化剂与还原剂的物质的量之比为 |
D.该反应体现了 单质的氧化性 单质的氧化性 |
您最近一年使用:0次
7 . 关于反应 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.上述反应中 发生还原反应,氧化产物与还原产物物质的量之比为 发生还原反应,氧化产物与还原产物物质的量之比为 |
B. 属于 属于 区元素,气态 区元素,气态 比气态 比气态 更难再失去1个电子 更难再失去1个电子 |
C. 、双氧水、明矾都是生活中常见的消毒剂 、双氧水、明矾都是生活中常见的消毒剂 |
D.生成标准状况下的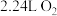 时,转移 时,转移 电子 电子 |
您最近一年使用:0次
8 . 由一种阳离子与两种酸根阴离子组成的盐称为混盐, 是一种常见的混盐。下列说法不正确的是
是一种常见的混盐。下列说法不正确的是
 是一种常见的混盐。下列说法不正确的是
是一种常见的混盐。下列说法不正确的是A. 有较强的氧化性 有较强的氧化性 |
B. 有类似于漂白粉的性质,也是混合物 有类似于漂白粉的性质,也是混合物 |
C.由氯气为原料,每生成 ,转移的电子为1mol ,转移的电子为1mol |
D. 的溶液中加入足量浓硫酸,可有黄绿色的气体产生 的溶液中加入足量浓硫酸,可有黄绿色的气体产生 |
您最近一年使用:0次
2024-03-08更新
|
62次组卷
|
2卷引用:浙江省杭州市长河高级中学2023-2024学年高一上学期期末考试化学试题
解题方法
9 . 向 的
的 溶液中加入足量铜粉,充分反应,被还原的
溶液中加入足量铜粉,充分反应,被还原的 的物质的量
的物质的量
 的
的 溶液中加入足量铜粉,充分反应,被还原的
溶液中加入足量铜粉,充分反应,被还原的 的物质的量
的物质的量| A.等于1.8mol | B.小于0.9mol |
| C.等于0.9mol | D.在0.9mol和1.8mol之间 |
您最近一年使用:0次
解题方法
10 .  常用作橡胶的硫化剂,各原子最外层均达到8电子稳定结构,与水极易反应:
常用作橡胶的硫化剂,各原子最外层均达到8电子稳定结构,与水极易反应: (未配平),下列说法
(未配平),下列说法不正确 的是
 常用作橡胶的硫化剂,各原子最外层均达到8电子稳定结构,与水极易反应:
常用作橡胶的硫化剂,各原子最外层均达到8电子稳定结构,与水极易反应: (未配平),下列说法
(未配平),下列说法A. 中氯元素化合价: 中氯元素化合价: |
B. 中存在非极性共价键和极性共价键数目比为 中存在非极性共价键和极性共价键数目比为 |
C. 与水反应时,氧化产物与还原产物的物质的量之比为 与水反应时,氧化产物与还原产物的物质的量之比为 |
D.若产生 单质 单质 ,转移电子数为 ,转移电子数为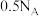 |
您最近一年使用:0次



