解题方法
1 . 向 含
含 和
和 混合溶液中加入一定量锌粉,反应过程中各离子的物质的量与加入锌粉的物质的量关系如图所示。下列说法正确的是
混合溶液中加入一定量锌粉,反应过程中各离子的物质的量与加入锌粉的物质的量关系如图所示。下列说法正确的是
 含
含 和
和 混合溶液中加入一定量锌粉,反应过程中各离子的物质的量与加入锌粉的物质的量关系如图所示。下列说法正确的是
混合溶液中加入一定量锌粉,反应过程中各离子的物质的量与加入锌粉的物质的量关系如图所示。下列说法正确的是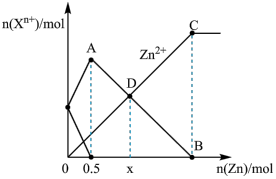
A.起始时, 溶液和 溶液和 溶液的物质的量浓度均为 溶液的物质的量浓度均为 |
B.D点的横坐标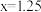 |
C.线段 表示溶液中 表示溶液中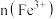 的变化趋势 的变化趋势 |
D.反应至 点时,溶液总质量增加 点时,溶液总质量增加 |
您最近一年使用:0次
解题方法
2 . 在酸性条件下,黄铁矿 催化氧化反应的离子方程式为
催化氧化反应的离子方程式为 。实现该反应的物质间转化如图所示。下列分析错误的是
。实现该反应的物质间转化如图所示。下列分析错误的是
 催化氧化反应的离子方程式为
催化氧化反应的离子方程式为 。实现该反应的物质间转化如图所示。下列分析错误的是
。实现该反应的物质间转化如图所示。下列分析错误的是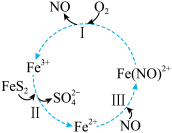
| A.黄铁矿催化氧化中NO作催化剂 |
B.反应Ⅰ的离子方程式为 |
| C.反应Ⅲ是非氧化还原反应 |
D.反应Ⅱ中若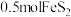 被还原,转移电子的物质的量为 被还原,转移电子的物质的量为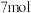 |
您最近一年使用:0次
名校
3 . ClO2和亚氯酸钠(NaClO2)都是广泛使用的漂白剂、消毒剂。高浓度ClO2气体易发生爆炸,在生产、使用时需用其他气体进行稀释。某工厂生产ClO2和NaClO2的工艺流程为:
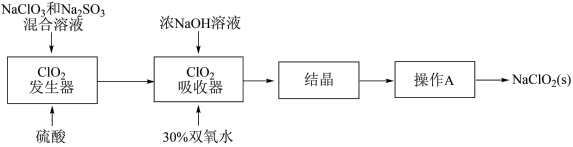
ClO2发生器中反应为NaClO3+Na2SO3+H2SO4→Na2SO4+ClO2↑+H2O(未配平),下列有关该反应的说法中,正确的是

ClO2发生器中反应为NaClO3+Na2SO3+H2SO4→Na2SO4+ClO2↑+H2O(未配平),下列有关该反应的说法中,正确的是
| A.反应中Na2SO3是氧化剂 |
| B.反应中ClO2是氧化产物 |
| C.每生成1个ClO2转移2个电子 |
| D.参加反应的NaClO3和Na2SO3的个数之比为2∶1 |
您最近一年使用:0次
名校
4 . 工业上SO2尾气和Cr2O 可通过Fe3+循环处理吸收,发生如下两个化学反应:SO2+2Fe3++2H2O=SO
可通过Fe3+循环处理吸收,发生如下两个化学反应:SO2+2Fe3++2H2O=SO +2Fe2++4H+,Cr2O
+2Fe2++4H+,Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O,有关说法正确的是
+6Fe2++14H+=2Cr3++6Fe3++7H2O,有关说法正确的是
 可通过Fe3+循环处理吸收,发生如下两个化学反应:SO2+2Fe3++2H2O=SO
可通过Fe3+循环处理吸收,发生如下两个化学反应:SO2+2Fe3++2H2O=SO +2Fe2++4H+,Cr2O
+2Fe2++4H+,Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O,有关说法正确的是
+6Fe2++14H+=2Cr3++6Fe3++7H2O,有关说法正确的是| A.两个反应中Fe2(SO4)3均作还原剂 |
B.氧化性Cr2O >SO2>Fe3+ >SO2>Fe3+ |
C.Cr2O 能将SO2氧化成SO 能将SO2氧化成SO |
D.第二个反应中1个Cr2O 参与反应,转移3个电子 参与反应,转移3个电子 |
您最近一年使用:0次
5 .  溶液和
溶液和 溶液都是临床上常用的外用消毒剂,酸性条件下两者混合会发生反应:
溶液都是临床上常用的外用消毒剂,酸性条件下两者混合会发生反应: 。下列有关判断正确的是
。下列有关判断正确的是
 溶液和
溶液和 溶液都是临床上常用的外用消毒剂,酸性条件下两者混合会发生反应:
溶液都是临床上常用的外用消毒剂,酸性条件下两者混合会发生反应: 。下列有关判断正确的是
。下列有关判断正确的是A.该反应中 作氧化剂 作氧化剂 | B. 的氧化性强于 的氧化性强于 |
C.反应中 发生了还原反应 发生了还原反应 | D.每生成1个 分子时,反应中转移4个电子 分子时,反应中转移4个电子 |
您最近一年使用:0次
解题方法
6 . 化学小组研究发现雾霾微颗粒中硫酸盐的生成可能存在三个阶段的转化,其主要过程如图所示。下列说法错误的是
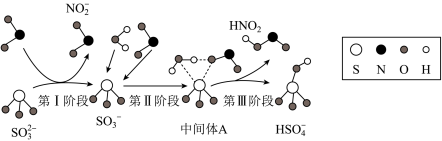
A. 、 、 均为共价化合物 均为共价化合物 |
B. 为转化过程中的氧化剂 为转化过程中的氧化剂 |
C.第Ⅰ阶段反应的化学方程式为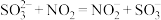 |
D.第Ⅱ、Ⅲ阶段总反应中,每反应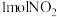 ,转移1mol电子 ,转移1mol电子 |
您最近一年使用:0次
7 . 已知实验室制取氯气的反应原理为: ,据此回答下列问题:
,据此回答下列问题:
(1)①该反应中氧化剂是_(填化学式,下同),被氧化的元素是___________ 元素。氧化剂和还原剂的比例为___________ 。若生成2个 ,转移的电子数目为
,转移的电子数目为___________ 。
②浓盐酸在该反应中表现的性质是___________ (填序号)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)用双线桥法表示该反应电子转移的方向和数目:___________ 。
(3)有一种“地康法”制取氯气的反应原理如下所示:

①反应I的离子方程式为___________ 。
②反应Ⅱ属于___________ 反应。(填四种基本反应类型之一)
 ,据此回答下列问题:
,据此回答下列问题:(1)①该反应中氧化剂是_(填化学式,下同),被氧化的元素是
 ,转移的电子数目为
,转移的电子数目为②浓盐酸在该反应中表现的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)用双线桥法表示该反应电子转移的方向和数目:
(3)有一种“地康法”制取氯气的反应原理如下所示:

①反应I的离子方程式为
②反应Ⅱ属于
您最近一年使用:0次
名校
解题方法
8 . 氮化硅(Si3N4)常用作飞船返回舱耐高温结构材料,可由石英和焦炭在高温的氮气中通过以下反应制备: 。设NA为阿伏加德罗常数的值。下列说法正确的是
。设NA为阿伏加德罗常数的值。下列说法正确的是
 。设NA为阿伏加德罗常数的值。下列说法正确的是
。设NA为阿伏加德罗常数的值。下列说法正确的是| A.SiO2是太阳能电池的主要材料 |
| B.60gSiO2中Si-O共价键的数目为2NA |
| C.14g由N2和CO组成的混合气体含有的电子数为7NA |
| D.上述反应中,每消耗11.2LN2,最多生成0.25 mol Si3N4 |
您最近一年使用:0次
2023-11-01更新
|
264次组卷
|
4卷引用:山西省怀仁市第一中学校2023-2024学年高三上学期第三次月考理综化学试题
解题方法
9 . 已知A、B、C、D、E、F六种常见物质存在如图所示转化关系(部分生成物和反应条件略去)。

(1)若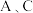 均为氧化物:
均为氧化物:
①若 为单质,向
为单质,向 溶液中滴加
溶液中滴加 溶液,溶液显红色,
溶液,溶液显红色, 为
为___________ (填化学式);写出 的离子方程式:
的离子方程式:___________ 。
②若 是含钠正盐,其水溶液呈碱性,
是含钠正盐,其水溶液呈碱性, 是一种温室气体,写出
是一种温室气体,写出 的一条用途:
的一条用途:___________ ; 的水溶液呈碱性的原因为
的水溶液呈碱性的原因为___________ (用离子方程式表示)。
(2)若 为固体氧化物,
为固体氧化物, 为气体单质,
为气体单质, 进行焰色试验时,火焰呈黄色,写出化合物
进行焰色试验时,火焰呈黄色,写出化合物 的电子式:
的电子式:___________ ;每生成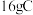 ,转移的电子的物质的量为
,转移的电子的物质的量为___________  。
。
(3)若 为
为 ,写出
,写出 与
与 反应的化学方程式:
反应的化学方程式:___________ 。

(1)若
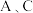 均为氧化物:
均为氧化物:①若
 为单质,向
为单质,向 溶液中滴加
溶液中滴加 溶液,溶液显红色,
溶液,溶液显红色, 为
为 的离子方程式:
的离子方程式:②若
 是含钠正盐,其水溶液呈碱性,
是含钠正盐,其水溶液呈碱性, 是一种温室气体,写出
是一种温室气体,写出 的一条用途:
的一条用途: 的水溶液呈碱性的原因为
的水溶液呈碱性的原因为(2)若
 为固体氧化物,
为固体氧化物, 为气体单质,
为气体单质, 进行焰色试验时,火焰呈黄色,写出化合物
进行焰色试验时,火焰呈黄色,写出化合物 的电子式:
的电子式: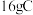 ,转移的电子的物质的量为
,转移的电子的物质的量为 。
。(3)若
 为
为 ,写出
,写出 与
与 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
名校
解题方法
10 .  是一种高效水处理剂,其制备原理之一为
是一种高效水处理剂,其制备原理之一为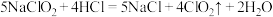 下列有关该反应的说法正确的是
下列有关该反应的说法正确的是
 是一种高效水处理剂,其制备原理之一为
是一种高效水处理剂,其制备原理之一为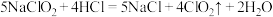 下列有关该反应的说法正确的是
下列有关该反应的说法正确的是A. 为还原剂 为还原剂 | B. 一定不是还原产物 一定不是还原产物 |
C. 中氯元素呈 中氯元素呈 价 价 | D.若生产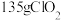 ,则转移 ,则转移 电子 电子 |
您最近一年使用:0次
2023-09-04更新
|
113次组卷
|
4卷引用:山西省部分学校2023-2024学年高三第一联考(月考)化学试题



