1 . 2Na2S2O3+I2=2NaI+Na2S4O6是定量分析中的常用反应。下列关于说法不正确 的是
| A.反应中,I2表现了氧化性 |
| B.反应中,每生成1 mol Na2S4O6,有4 mol e-发生转移 |
| C.Na2S2O3是含有共价键的离子化合物 |
| D.Na2S2O3在空气中放置会变质,产物可能有Na2SO4 |
您最近一年使用:0次
2021-01-22更新
|
984次组卷
|
9卷引用:北京市海淀区2021届高三上学期期末考试化学试题
北京市海淀区2021届高三上学期期末考试化学试题(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)2021年天津高考化学试题变式题1-12北京市中国人民大学附属中学2022届高三下学期第三次适应性练习化学试题山东省潍坊五县市2022-2023学年高三上学期10月质量检测联考化学试题山东省济宁市育才中学2022-2023学年高三10月线上阶段性检测化学试题北京市中国人民大学附属中学2022-2023学年高三上学期统练6化学试题北京工业大学附属中学2022-2023学年高三上学期开学测试化学试题
2 . 某含铬矿石的回收生产中得到BaCrO4的样品,为了测定其中BaCrO4的含量,进行以下实验: =2I−+S4O
=2I−+S4O ;②CrO
;②CrO 的还原产物为Cr3+;③杂质不参与相关反应
的还原产物为Cr3+;③杂质不参与相关反应
1.样品中BaCrO4(摩尔质量为Mg·mol−l)的质量分数为_____ (用字母表示)。
2.若加入的HI溶液过量太多,测定结果会_____。
3.用还原法可以将硝酸厂烟气中的大量氮氧化物(NOx),转化为无害物质。常温下,将NO与H2的混合气体通入Ce(SO4) 2与Ce2 (SO4)3的混合溶液中,其转化过程如图所示。下列说法错误的是_____。
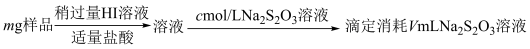
 =2I−+S4O
=2I−+S4O ;②CrO
;②CrO 的还原产物为Cr3+;③杂质不参与相关反应
的还原产物为Cr3+;③杂质不参与相关反应1.样品中BaCrO4(摩尔质量为Mg·mol−l)的质量分数为
2.若加入的HI溶液过量太多,测定结果会_____。
| A.偏高 | B.偏低 | C.无影响 | D.无法确定 |
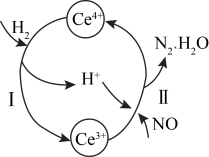
| A.反应I的离子反应方程式为:2Ce4++H2=2Ce3++2H+ |
| B.反应II中氧化剂与还原剂的物质的量之比为1:2 |
| C.反应前溶液中c(Ce4+)一定等于反应后溶液中的c(Ce4+) |
| D.反应过程中混合溶液内Ce3+和Ce4+的总数一定保持不变 |
您最近一年使用:0次
名校
3 . 过氧化钙晶体(CaO2 8H2O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。
8H2O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。
轻质CaCO3粉末 滤液
滤液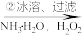 白色结晶体
白色结晶体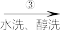 目标产物
目标产物
回答下列问题:
(1)CaO2电子式:_________________ 。
(2)反应①的离子方程式为_________________ ;过滤过程中用到的玻璃仪器有_________ 。
(3)用上述方法制取CaO2 8H2O的化学方程式为
8H2O的化学方程式为___________________________________ 。
(4)操作②温度不宜过高,其可能原因是___________________________________________ 。
(5)实验室常采用以酸为介质,用高锰酸钾溶液测定过氧化钙的含量。其原理为:5CaO2+8H2SO4+2KMnO4=5CaSO4+2MnSO4+5O2 +8H2O+K2SO4
+8H2O+K2SO4
,某同学准确称取ag产品于有塞锥形瓶中,用适量酸溶解,加入cmLbmol L-1的高锰酸钾溶液恰好完全反应,则该样品中过氧化钙的百分含量为
L-1的高锰酸钾溶液恰好完全反应,则该样品中过氧化钙的百分含量为________ (用含a、b、c的代数式表示)。
 8H2O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。
8H2O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。轻质CaCO3粉末
 滤液
滤液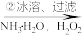 白色结晶体
白色结晶体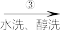 目标产物
目标产物回答下列问题:
(1)CaO2电子式:
(2)反应①的离子方程式为
(3)用上述方法制取CaO2
 8H2O的化学方程式为
8H2O的化学方程式为(4)操作②温度不宜过高,其可能原因是
(5)实验室常采用以酸为介质,用高锰酸钾溶液测定过氧化钙的含量。其原理为:5CaO2+8H2SO4+2KMnO4=5CaSO4+2MnSO4+5O2
 +8H2O+K2SO4
+8H2O+K2SO4,某同学准确称取ag产品于有塞锥形瓶中,用适量酸溶解,加入cmLbmol
 L-1的高锰酸钾溶液恰好完全反应,则该样品中过氧化钙的百分含量为
L-1的高锰酸钾溶液恰好完全反应,则该样品中过氧化钙的百分含量为
您最近一年使用:0次
名校
4 . 以NaCl等为原料制备KClO4的过程如下:
①在无隔膜、微酸性条件下,发生反应:NaCl+H2O—NaClO3+H2↑(未配平)
②在NaClO3溶液中加入KCl发生复分解反应,降温结晶,得KClO3。
③一定条件下反应:4KClO3=3KClO4+KCl,将产物分离得到KClO4。
(1)电解时,产生质量为2.13g NaClO3,同时得到H2的体积为_______ L(标准状况)。
(2)向NaClO3溶液中加入KCl能得到KClO3的原因是________________ 。

(3)该过程制得的KClO4样品中含少量KCl杂质,为测定产品纯度进行如下实验:
准确称取5.689g样品溶于水中,配成250mL溶液,从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使ClO4-全部转化为Cl- (反应为:3 KClO4 +C6H12O6 ═ 6 H2O + 6 CO2↑ + 3 KCl),加入少量K2CrO4溶液作指示剂,用0. 20mol/L AgNO3溶液进行滴定至终点,消耗AgNO3溶液体积21.00mL。滴定达到终点时,产生砖红色Ag2CrO4沉淀。
① 已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.1×10-12,若c(CrO42-)=1.1×10-4mol/L,则此时c(Cl-)=________________ mol/L。
② 计算KClO4样品的纯度(请写出计算过程。)______________________________
①在无隔膜、微酸性条件下,发生反应:NaCl+H2O—NaClO3+H2↑(未配平)
②在NaClO3溶液中加入KCl发生复分解反应,降温结晶,得KClO3。
③一定条件下反应:4KClO3=3KClO4+KCl,将产物分离得到KClO4。
(1)电解时,产生质量为2.13g NaClO3,同时得到H2的体积为
(2)向NaClO3溶液中加入KCl能得到KClO3的原因是

(3)该过程制得的KClO4样品中含少量KCl杂质,为测定产品纯度进行如下实验:
准确称取5.689g样品溶于水中,配成250mL溶液,从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使ClO4-全部转化为Cl- (反应为:3 KClO4 +C6H12O6 ═ 6 H2O + 6 CO2↑ + 3 KCl),加入少量K2CrO4溶液作指示剂,用0. 20mol/L AgNO3溶液进行滴定至终点,消耗AgNO3溶液体积21.00mL。滴定达到终点时,产生砖红色Ag2CrO4沉淀。
① 已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.1×10-12,若c(CrO42-)=1.1×10-4mol/L,则此时c(Cl-)=
② 计算KClO4样品的纯度(请写出计算过程。)
您最近一年使用:0次
2016-12-09更新
|
301次组卷
|
6卷引用:2016届江苏省清江中学高三下学期考前练习化学试卷



