名校
解题方法
1 . 亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下: _______
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下: _______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______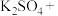 _______
_______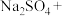 _______
_______
(1)请完成该化学方程式并配平。_______
(2) 中N的化合价为
中N的化合价为_______ ,由N的化合价推测 具有
具有_______ (填“氧化性”、“还原性”或“氧化性、还原性”)。
(3)用上述反应来处理 并不是最佳方法,其原因是
并不是最佳方法,其原因是_______ 。从环保角度来讲,要将 转化为氮气,所用物质的
转化为氮气,所用物质的_______ (填“氧化性”或“还原性”)应该比 更
更_______ (填“强”或“弱”)。
(4)下列方法不能用来区分固体 和
和 的是_______(填序号)。
的是_______(填序号)。
(5) 与
与 反应:
反应: ,若有0.5mol氧化剂被还原,则被氧化的还原剂的物质的量是
,若有0.5mol氧化剂被还原,则被氧化的还原剂的物质的量是_______ mol。
(6)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式_______ 。
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下: _______
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下: _______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______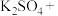 _______
_______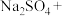 _______
_______
(1)请完成该化学方程式并配平。
(2)
 中N的化合价为
中N的化合价为 具有
具有(3)用上述反应来处理
 并不是最佳方法,其原因是
并不是最佳方法,其原因是 转化为氮气,所用物质的
转化为氮气,所用物质的 更
更(4)下列方法不能用来区分固体
 和
和 的是_______(填序号)。
的是_______(填序号)。| A.分别溶于水并滴加酚酞试液 | B.分别溶于水并滴加 酸化的 酸化的 溶液 溶液 |
| C.分别加强热并收集气体检验 | D.用筷子分别蘸取固体品尝味道 |
 与
与 反应:
反应: ,若有0.5mol氧化剂被还原,则被氧化的还原剂的物质的量是
,若有0.5mol氧化剂被还原,则被氧化的还原剂的物质的量是(6)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式
您最近一年使用:0次
名校
2 . 高铁酸钾( ,极易溶于水,溶液呈紫红色)是一种绿色净水剂,易溶于水。某小组在实验室条件下制备
,极易溶于水,溶液呈紫红色)是一种绿色净水剂,易溶于水。某小组在实验室条件下制备 并探究其性质。回答下列问题:
并探究其性质。回答下列问题:
实验(一)制备
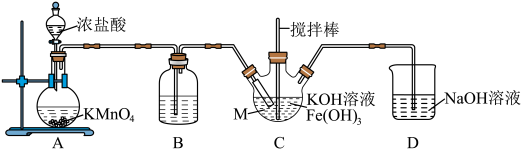
(1)仪器M的名称是_______ ,装置B的作用是_______ 。
(2)装置C中生成 的化学方程式为
的化学方程式为______ 。
(3)实验得知装置C中吸收 的量为装置A中生成
的量为装置A中生成 总量的75%,若装置D中的氧化产物只有0.02mol NaClO,且不考虑其他消耗,则理论上生成
总量的75%,若装置D中的氧化产物只有0.02mol NaClO,且不考虑其他消耗,则理论上生成 的质量为
的质量为_______ g。
实验(二)探究 的性质。
的性质。
Ⅰ.探究 在酸性条件下的稳定性。
在酸性条件下的稳定性。
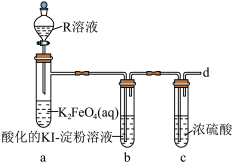
已知:实验中观察到试管b中溶液变为蓝色,试管a中溶液由紫红色变黄色并产生气泡。
(4)R溶液为_______ (填“稀硫酸”或“盐酸”),写出装置a中的离子方程式:______ ,不选择另一种酸的主要原因是_______ 。
(5)设计一种方案检验从d中逸出的气体:_______
Ⅱ.探究在酸性条件下的氧化性。
(6)向 溶液中滴加少量用稀硫酸酸化后的
溶液中滴加少量用稀硫酸酸化后的 溶液,溶液呈紫红色。
溶液,溶液呈紫红色。_______ (填“能”或“不能”)证明氧化性: ,原因是
,原因是_______ (用文字说明)。
 ,极易溶于水,溶液呈紫红色)是一种绿色净水剂,易溶于水。某小组在实验室条件下制备
,极易溶于水,溶液呈紫红色)是一种绿色净水剂,易溶于水。某小组在实验室条件下制备 并探究其性质。回答下列问题:
并探究其性质。回答下列问题:实验(一)制备


(1)仪器M的名称是
(2)装置C中生成
 的化学方程式为
的化学方程式为(3)实验得知装置C中吸收
 的量为装置A中生成
的量为装置A中生成 总量的75%,若装置D中的氧化产物只有0.02mol NaClO,且不考虑其他消耗,则理论上生成
总量的75%,若装置D中的氧化产物只有0.02mol NaClO,且不考虑其他消耗,则理论上生成 的质量为
的质量为实验(二)探究
 的性质。
的性质。Ⅰ.探究
 在酸性条件下的稳定性。
在酸性条件下的稳定性。
已知:实验中观察到试管b中溶液变为蓝色,试管a中溶液由紫红色变黄色并产生气泡。
(4)R溶液为
(5)设计一种方案检验从d中逸出的气体:
Ⅱ.探究在酸性条件下的氧化性。
(6)向
 溶液中滴加少量用稀硫酸酸化后的
溶液中滴加少量用稀硫酸酸化后的 溶液,溶液呈紫红色。
溶液,溶液呈紫红色。 ,原因是
,原因是
您最近一年使用:0次
2023-09-27更新
|
354次组卷
|
11卷引用:青海省海南州贵德高级中学2023-2024学年高三上学期10月月考化学试卷
青海省海南州贵德高级中学2023-2024学年高三上学期10月月考化学试卷河北省邢台市五岳联盟2023-2024学年高三上学期9月月考化学试题河北省部分学校2023-2024学年高三上学期9月月考化学试题河南省2023-2024学年高三上学期一轮复习阶段性检测(三)化学试题河南省驻马店市第一次联考2023-2024学年高三上学期9月月考化学试题江西省部分高中学校2024届高三上学期9月大联考化学试题福建省2023-2024学年高三上学期10月百万大联考化学试题 河南省洛阳市洛宁县第一高级中学2023-2024学年高三上学期阶段性考试(三)化学试题河北省保定部分高中2023-2024学年高三上学期9月月考化学试题福建省福州高新区第一中学(闽侯县第三中学)2023-20024学年高三上学期第一次月考化学试题河南省濮阳市油田第一中学2024届高三上学期第一次考试理科综合化学试题
解题方法
3 . 三氯化锑 用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为
用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为 ,还含有
,还含有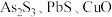 和
和 等)为原料制备
等)为原料制备 的工艺流程如图:
的工艺流程如图:
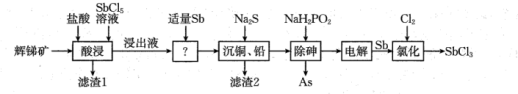
已知:① 具有强氧化性,“浸出液”主要含盐酸和
具有强氧化性,“浸出液”主要含盐酸和 ,还含
,还含 和
和 等杂质;
等杂质;
②常温下,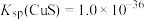 、
、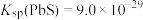 ;
;
③溶液中离子浓度小于或等于 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。
回答下列问题:
(1)除将辉锑矿粉碎外,还能加快辉锑矿“酸浸”速率的措施有_____ (填两条)。
(2)“滤渣1”的主要成分有_____ (填化学式);若在实验室模拟分离“滤渣1”和“浸出液”,需要使用到的硅酸盐仪器有_____ 。
(3)“浸出液”中加入适量 的目的是
的目的是_____ (填化学方程式)。
(4)当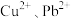 共沉淀时,溶液中
共沉淀时,溶液中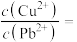
_____ (保留两位有效数字)。
(5)“除砷”时,氧化产物为 ,则
,则 (可溶于水)与
(可溶于水)与 反应的离子方程式为
反应的离子方程式为_____ 。
(6)已知:“电解” 溶液时有
溶液时有 生成。则上述流程中可循环利用的物质有
生成。则上述流程中可循环利用的物质有_____ 。
 用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为
用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为 ,还含有
,还含有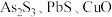 和
和 等)为原料制备
等)为原料制备 的工艺流程如图:
的工艺流程如图:
已知:①
 具有强氧化性,“浸出液”主要含盐酸和
具有强氧化性,“浸出液”主要含盐酸和 ,还含
,还含 和
和 等杂质;
等杂质;②常温下,
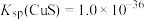 、
、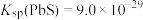 ;
;③溶液中离子浓度小于或等于
 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。回答下列问题:
(1)除将辉锑矿粉碎外,还能加快辉锑矿“酸浸”速率的措施有
(2)“滤渣1”的主要成分有
(3)“浸出液”中加入适量
 的目的是
的目的是(4)当
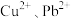 共沉淀时,溶液中
共沉淀时,溶液中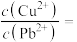
(5)“除砷”时,氧化产物为
 ,则
,则 (可溶于水)与
(可溶于水)与 反应的离子方程式为
反应的离子方程式为(6)已知:“电解”
 溶液时有
溶液时有 生成。则上述流程中可循环利用的物质有
生成。则上述流程中可循环利用的物质有
您最近一年使用:0次



