解题方法
1 . 氮及其化合物在生产、生活中广泛应用。
Ⅰ.氮元素化合价-物质类别关系图如图所示。

(1)图中A可以是__________ (写化学式)。写出一个能够生成B的化学方程式__________ 。
(2)实验室中,检验溶液中是否含有 的操作方法是
的操作方法是__________ 。
(3)水体中硝酸盐含量过高对环境不利,通过电催化法可以将水体中的硝酸盐进行合理转化。写出在中性介质中硝酸盐转化为氮气的阴极电极反应式__________ 。
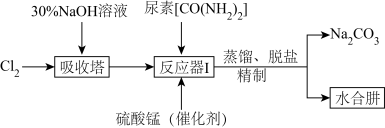
Ⅱ.下图为实验室模拟尿素法制备水合肼( )的流程图:
)的流程图:
已知:① 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 。
。
②一定条件下,碱性NaClO溶液与尿素溶液反应生成 。
。
回答下列问题:
(4)“吸收塔”内发生反应的离子方程式为__________ 。
(5)写出“反应器Ⅰ”中生成水合肼反应的化学方程式为__________ 。
(6)“反应器Ⅰ”要控制NaClO溶液的用量,其主要目的是__________ 。
Ⅰ.氮元素化合价-物质类别关系图如图所示。

(1)图中A可以是
(2)实验室中,检验溶液中是否含有
 的操作方法是
的操作方法是(3)水体中硝酸盐含量过高对环境不利,通过电催化法可以将水体中的硝酸盐进行合理转化。写出在中性介质中硝酸盐转化为氮气的阴极电极反应式
Ⅱ.下图为实验室模拟尿素法制备水合肼(
 )的流程图:
)的流程图:
已知:①
 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 。
。②一定条件下,碱性NaClO溶液与尿素溶液反应生成
 。
。回答下列问题:
(4)“吸收塔”内发生反应的离子方程式为
(5)写出“反应器Ⅰ”中生成水合肼反应的化学方程式为
(6)“反应器Ⅰ”要控制NaClO溶液的用量,其主要目的是
您最近一年使用:0次
解题方法
2 . 在酸性条件下,黄铁矿( ,其中S为~1价)催化氧化的反应转化如图所示。
,其中S为~1价)催化氧化的反应转化如图所示。
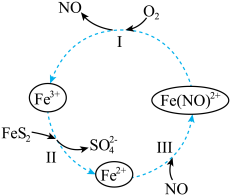
总反应:
(1)分别写出反应Ⅰ、Ⅱ的离子方程式:
①反应Ⅰ:_______ 。
②反应Ⅱ:_______ 。
(2)NO在总反应中的作用是_______ 。
 ,其中S为~1价)催化氧化的反应转化如图所示。
,其中S为~1价)催化氧化的反应转化如图所示。
总反应:

(1)分别写出反应Ⅰ、Ⅱ的离子方程式:
①反应Ⅰ:
②反应Ⅱ:
(2)NO在总反应中的作用是
您最近一年使用:0次
3 . 金属钠及其化合物在人类生产、生活中起着重要作用。诸回答下列问题:
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中加入黄豆粒大小的金属钠,可能观察到的现象是___________(填序号)。
(2)金属钠在氧气中燃烧生成Na2O2,其电子式为___________ ,采用空气和Na为原料可直接制备Na2O2.空气与熔融的金属Na反应前需依次通过的试剂为___________ 、___________ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(3)NaCl的熔点为800.8℃。工业上采用电解熔融的NaCl和CaCl2混合盐制备金属Na,电解的化学方程式为:2NaCl(l)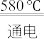 2Na(1)+Cl2(g),加入CaCl2的目的是
2Na(1)+Cl2(g),加入CaCl2的目的是___________ 。
(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应。
 +____ H++_____ Na2O2=____ Mn2++_____ Na+_____ O2↑+____H2O
+____ H++_____ Na2O2=____ Mn2++_____ Na+_____ O2↑+____H2O
①配平上述离子方程式___________ 。
②该反应说明Na2O2具有___________ (选填“氧化性”“还原性"或“漂白性”)。
(5)在密闭容器中,将a mol Na2O2和b mol NaHCO3固体混合物加热至250℃,充分反应后,若剩余固体为Na2CO3和NaOH,排出气体为O2和H2O时,a:b的取值范围为___________ 。
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中加入黄豆粒大小的金属钠,可能观察到的现象是___________(填序号)。
A. | B.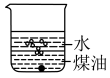 |
C. | D. |
(2)金属钠在氧气中燃烧生成Na2O2,其电子式为
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(3)NaCl的熔点为800.8℃。工业上采用电解熔融的NaCl和CaCl2混合盐制备金属Na,电解的化学方程式为:2NaCl(l)
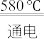 2Na(1)+Cl2(g),加入CaCl2的目的是
2Na(1)+Cl2(g),加入CaCl2的目的是(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应。
 +____ H++_____ Na2O2=____ Mn2++_____ Na+_____ O2↑+____H2O
+____ H++_____ Na2O2=____ Mn2++_____ Na+_____ O2↑+____H2O①配平上述离子方程式
②该反应说明Na2O2具有
(5)在密闭容器中,将a mol Na2O2和b mol NaHCO3固体混合物加热至250℃,充分反应后,若剩余固体为Na2CO3和NaOH,排出气体为O2和H2O时,a:b的取值范围为
您最近一年使用:0次
名校
解题方法
4 . 下列表述的方程式或离子方程式正确的是
A.向NaHS溶液中滴加 溶液: 溶液: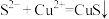 |
B.表示乙醇燃烧热的热化学方程式:  |
C.向酸性 溶液中滴加双氧水: 溶液中滴加双氧水: |
D. 溶液与过量NaOH溶液混合: 溶液与过量NaOH溶液混合: |
您最近一年使用:0次
名校
解题方法
5 . 下列化学反应对应的离子方程式表示正确的是
| A.Fe(OH)2溶于稀硝酸Fe(OH)2+2H+=Fe2++2H2O |
B.NH4HCO3溶于过量的NaOH溶液中:HCO +OH-=CO +OH-=CO +H2O +H2O |
C.KAl(SO4)2中滴加Ba(OH)2使SO 恰好完全沉淀:2Al3++3SO 恰好完全沉淀:2Al3++3SO +3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ +3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| D.FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2 |
您最近一年使用:0次
名校
解题方法
6 . 铬酸钠( )是一种无机化合物,主要用于墨水、涂料、颜料,金属缓蚀剂以及鞣革和印染等。碱性亚铬酸钠溶液(
)是一种无机化合物,主要用于墨水、涂料、颜料,金属缓蚀剂以及鞣革和印染等。碱性亚铬酸钠溶液( )与过氧化氢溶液反应生成黄色的铬酸钠(
)与过氧化氢溶液反应生成黄色的铬酸钠( ),其反应离子方程式为
),其反应离子方程式为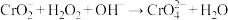 (未配平),下列叙述正确的是
(未配平),下列叙述正确的是
 )是一种无机化合物,主要用于墨水、涂料、颜料,金属缓蚀剂以及鞣革和印染等。碱性亚铬酸钠溶液(
)是一种无机化合物,主要用于墨水、涂料、颜料,金属缓蚀剂以及鞣革和印染等。碱性亚铬酸钠溶液( )与过氧化氢溶液反应生成黄色的铬酸钠(
)与过氧化氢溶液反应生成黄色的铬酸钠( ),其反应离子方程式为
),其反应离子方程式为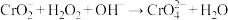 (未配平),下列叙述正确的是
(未配平),下列叙述正确的是| A.反应物中Cr元素的化合价为+4 |
B. 是还原剂 是还原剂 |
| C.该反应中氧化剂和还原剂的物质的量之比为2∶3 |
| D.生成2mol水分子时,转移3mol电子 |
您最近一年使用:0次
2023-08-20更新
|
362次组卷
|
2卷引用:湖南省张家界市慈利县第一中学2023-2024学年高三上学期第二次月考化学试卷
名校
7 .  是一种新型水处理剂,工业制备它的原理可表示为
是一种新型水处理剂,工业制备它的原理可表示为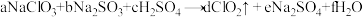 ,则
,则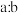 为
为
 是一种新型水处理剂,工业制备它的原理可表示为
是一种新型水处理剂,工业制备它的原理可表示为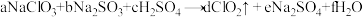 ,则
,则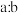 为
为A. | B. | C. | D. |
您最近一年使用:0次
2023-08-02更新
|
213次组卷
|
3卷引用:江西省泰和中学2022-2023学年高三下学期7月暑期考试化学试题
20-21高一上·陕西汉中·期末
8 . 化学与人类生产、生活密切相关,按要求回答下列问题。
(1)工业上制造光导纤维的基本原料是_______ (填化学式)。
(2)钠的化合物中,可用作潜水艇中供氧剂的是_______ ,其与 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(3)饮用水质量是关系人类健康的重要问题。暴雨过后,井水混浊无法饮用。为了能让井水变澄清,可向井水中投入_______(填字母)。
(4)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是_______ (填化学式)。
(5)新型陶瓷氮化铝可用氧化铝高温还原法制备: (未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目
(未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目_______ 。若反应中共转移 个电子,则产生
个电子,则产生 气体的体积为
气体的体积为_______ L(标准状况下)。
(1)工业上制造光导纤维的基本原料是
(2)钠的化合物中,可用作潜水艇中供氧剂的是
 发生反应的化学方程式为
发生反应的化学方程式为(3)饮用水质量是关系人类健康的重要问题。暴雨过后,井水混浊无法饮用。为了能让井水变澄清,可向井水中投入_______(填字母)。
A. | B. | C. | D. |
(5)新型陶瓷氮化铝可用氧化铝高温还原法制备:
 (未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目
(未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目 个电子,则产生
个电子,则产生 气体的体积为
气体的体积为
您最近一年使用:0次
2023-07-31更新
|
361次组卷
|
4卷引用:结构与性质
(已下线)结构与性质陕西省汉中市2020-2021学年高一上学期期末考试化学试题(已下线)期末测试卷02-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册) 2023-2024学年高一上学期化学人教版(2019)必修第一册 期末综合测试题(一)
名校
解题方法
9 . 下图是实验室中制取 的流程图,已知
的流程图,已知  显墨绿色,下列说法错误的是
显墨绿色,下列说法错误的是

 的流程图,已知
的流程图,已知  显墨绿色,下列说法错误的是
显墨绿色,下列说法错误的是
| A.第①步在铁坩埚中进行,第⑥步中加热浓缩在蒸发皿中进行 |
B.第②步中 作还原剂,第③步分批浸取可提高浸取率 作还原剂,第③步分批浸取可提高浸取率 |
C.第④步通 发生反应: 发生反应: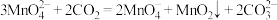 ,当有43.5g沉淀生成,反应中转移的电子数为NA个 ,当有43.5g沉淀生成,反应中转移的电子数为NA个 |
D.第⑤步加热趁热过滤,说明 的溶解度随温度变化较大 的溶解度随温度变化较大 |
您最近一年使用:0次
10 . 用反渗透法将海水淡化,剩余的浓缩液(主要含 、
、 、
、 、
、 、
、 等离子),可加工获得其他产品。某学习小组模拟工业生产流程进行实验。下列说法正确的是
等离子),可加工获得其他产品。某学习小组模拟工业生产流程进行实验。下列说法正确的是

 、
、 、
、 、
、 、
、 等离子),可加工获得其他产品。某学习小组模拟工业生产流程进行实验。下列说法正确的是
等离子),可加工获得其他产品。某学习小组模拟工业生产流程进行实验。下列说法正确的是
A.粗盐提纯中,加入试剂的顺序依次为 、 、 、NaOH、盐酸 、NaOH、盐酸 |
B.固体B主要成分为 |
C.反应III的离子方程式为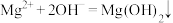 |
| D.反应IV可选用还原剂焦炭 |
您最近一年使用:0次



