解题方法
1 .  是化工合成中最重要的镍源,工业上以金属镍废料(含Fe、Ca、Mg等杂质)为原料生产
是化工合成中最重要的镍源,工业上以金属镍废料(含Fe、Ca、Mg等杂质)为原料生产 ,继而生产
,继而生产 的工艺流程如下:
的工艺流程如下:
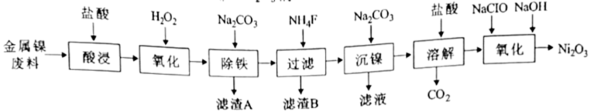
已知:①相关金属离子生成氢氧化物沉淀的pH如下表:
②当溶液中某离子浓度 ,可认为该离子已完全沉淀;
,可认为该离子已完全沉淀;
(1)“酸浸”时,需将金属镍废料粉碎的目的是________________ ;
(2)“除铁”过程中,应调节溶液pH的范围为_____________ ;
(3)滤渣B的主要成分是氟化钙和氟化镁,写出生成氟化钙的化学反应方程式___________ ;
(4)在“沉镍”操作中,若溶液中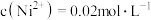 ,向其中加入等体积的
,向其中加入等体积的 溶液,使
溶液,使 沉淀完全,则所加
沉淀完全,则所加 溶液的浓度最小为
溶液的浓度最小为____________ (已知: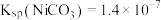 );
);
(5)“氧化”生成 的离子方程式为
的离子方程式为_______________ ;
 是化工合成中最重要的镍源,工业上以金属镍废料(含Fe、Ca、Mg等杂质)为原料生产
是化工合成中最重要的镍源,工业上以金属镍废料(含Fe、Ca、Mg等杂质)为原料生产 ,继而生产
,继而生产 的工艺流程如下:
的工艺流程如下:
已知:①相关金属离子生成氢氧化物沉淀的pH如下表:
氢氧化物 |
|
|
|
开始沉淀的pH | 1.1 | 6.5 | 7.1 |
沉淀完全的pH | 3.2 | 9.7 | 9.2 |
②当溶液中某离子浓度
 ,可认为该离子已完全沉淀;
,可认为该离子已完全沉淀;(1)“酸浸”时,需将金属镍废料粉碎的目的是
(2)“除铁”过程中,应调节溶液pH的范围为
(3)滤渣B的主要成分是氟化钙和氟化镁,写出生成氟化钙的化学反应方程式
(4)在“沉镍”操作中,若溶液中
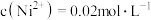 ,向其中加入等体积的
,向其中加入等体积的 溶液,使
溶液,使 沉淀完全,则所加
沉淀完全,则所加 溶液的浓度最小为
溶液的浓度最小为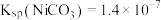 );
);(5)“氧化”生成
 的离子方程式为
的离子方程式为
您最近一年使用:0次
2 . 氧化铬(Cr2O3)可用作有机合成的催化剂。某课题组以铬铁矿为主要原料制备Cr2O3。铬铁矿主要成分为Fe(CrO2)2,还含有Al2O3、SiO2等杂质,工艺流程如图所示。
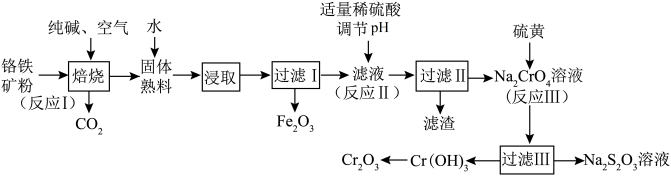
下列说法错误的是

下列说法错误的是
| A.Fe(CrO2)2中Cr元素的化合价为+3 |
| B.“焙烧”时,1 mol Fe(CrO2)2参加反应转移7 mol e− |
| C.图中“滤渣”成分是Al(OH)3 |
D.“反应Ⅲ”的离子方程式为4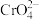 +6S+7H2O === 4Cr(OH)3↓+3 +6S+7H2O === 4Cr(OH)3↓+3 +2OH− +2OH− |
您最近一年使用:0次
名校
解题方法
3 . 钨(74W)是熔点最高的金属,是重要的战略物资。自然界中钨矿石的主要成分是铁和锰的钨酸盐(FeWO4、MnWO4),还含少量Si、P、As的化合物。由黑钨矿冶炼钨的工艺流程如下:

已知:①滤渣I的主要成分是Fe2O3、MnO2。②上述流程中,除最后一步外,其余步骤钨的化合价未变。③常温下钨酸难溶于水。 回答下列问题:
(1)钨酸中钨元素的化合价为_________ ,写出MnWO4在熔融条件下发生碱分解反应生成MnO2的化学方程式___________________________________________ 。
(2)上述流程中向粗钨酸钠溶液中加硫酸调pH=10后,溶液中的杂质阴离子为SiO32-、HAsO32-、HAsO42-、HPO42-等,则“净化”过程中,加入H2O2时发生反应的离子方程式为_______________________________ ,滤渣Ⅱ的主要成分是_________ 。
(3)已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小。图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线。则T1_________ T2(填“>”或“<”)。

将钨酸钠溶液加入石灰乳得到大量钨酸钙,发生反应的离子方程式为_________________ ,T2时该反应的平衡常数为_________________ 。
(4)硬质合金刀具中含碳化钨(WC),利用电解法可以从碳化钨废料中回收钨。电解时,用碳化钨做阳极,不锈钢做阴极,HCl溶液为电解液,阳极析出钨酸并放出CO2。该阳极反应式为_________________ 。

已知:①滤渣I的主要成分是Fe2O3、MnO2。②上述流程中,除最后一步外,其余步骤钨的化合价未变。③常温下钨酸难溶于水。 回答下列问题:
(1)钨酸中钨元素的化合价为
(2)上述流程中向粗钨酸钠溶液中加硫酸调pH=10后,溶液中的杂质阴离子为SiO32-、HAsO32-、HAsO42-、HPO42-等,则“净化”过程中,加入H2O2时发生反应的离子方程式为
(3)已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小。图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线。则T1

将钨酸钠溶液加入石灰乳得到大量钨酸钙,发生反应的离子方程式为
(4)硬质合金刀具中含碳化钨(WC),利用电解法可以从碳化钨废料中回收钨。电解时,用碳化钨做阳极,不锈钢做阴极,HCl溶液为电解液,阳极析出钨酸并放出CO2。该阳极反应式为
您最近一年使用:0次
名校
4 . 据报道,磷酸二氢钾(KH2PO4)大晶体已应用于我国研制的巨型激光器“神光二号”中。利用氟磷灰石(化学式为Ca5P3FO12)制备磷酸二氢钾的工艺流程如下图所示(部分流程步骤已省略):
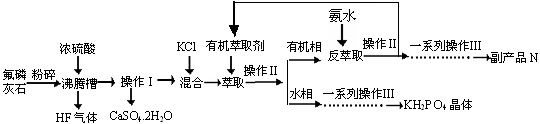
已知萃取的主要反应原理:KCl+H3PO4 KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
请回答下列问题:
(1)流程中将氟磷灰石粉碎的目的是__________________________________ 。
(2)不能使用二氧化硅陶瓷材质的沸腾槽的主要原因是____________ (用化学方程式表示)。
(3)副产品N的化学式是____________ ;在得到KH2PO4晶体的一系列操作Ⅲ,其主要包括____________ 、过滤、洗涤、干燥等。
(4)若用1000kg质量分数为50.4%的氟磷灰石(化学式为Ca5P3FO12,摩尔质量为504g/mol)来制取磷酸二氢钾晶体,其产率为80%,则理论上可生产KH2PO4(摩尔质量为136g/mol)的质量为_______ kg。
(5)电解法制备KH2PO4的装置如图所示.该电解装置中,a 区属于_______ 区(填“阳极”或“阴极”),阴极区的电极反应式是________________ 。
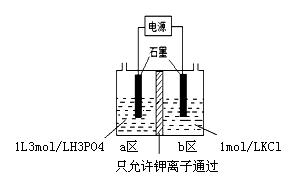
(6)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为________________________________________ 。

已知萃取的主要反应原理:KCl+H3PO4
 KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。请回答下列问题:
(1)流程中将氟磷灰石粉碎的目的是
(2)不能使用二氧化硅陶瓷材质的沸腾槽的主要原因是
(3)副产品N的化学式是
(4)若用1000kg质量分数为50.4%的氟磷灰石(化学式为Ca5P3FO12,摩尔质量为504g/mol)来制取磷酸二氢钾晶体,其产率为80%,则理论上可生产KH2PO4(摩尔质量为136g/mol)的质量为
(5)电解法制备KH2PO4的装置如图所示.该电解装置中,a 区属于

(6)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为
您最近一年使用:0次
2018-05-13更新
|
1519次组卷
|
6卷引用:【校级联考】广东省中山一中、仲元中学等七校2019届高三上学期第二次联考(11月)理科综合化学试题






