名校
1 . 硫、氮等非金属元素在化工生产中扮演着重要角色。
Ⅰ.在学习了硫的转化后,某学生绘制了如图转化关系。
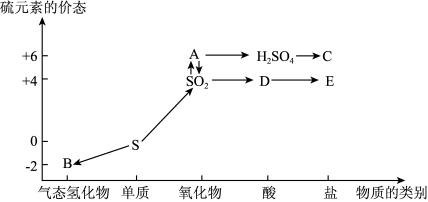
(1)写出 转化为A的化学方程式:
转化为A的化学方程式:_____ 。
(2)下列四种有色溶液与 作用均能褪色,体现
作用均能褪色,体现 还原性的是
还原性的是_____ 。
①品红溶液 ②酸性 溶液 ③碘水 ④滴有酚酞的NaOH溶液
溶液 ③碘水 ④滴有酚酞的NaOH溶液
写出 通入碘水溶液中反应的离子方程式:
通入碘水溶液中反应的离子方程式:_____ 。
(3)工业生产中利用氨水吸收 和
和 ,原理如图所示:
,原理如图所示:
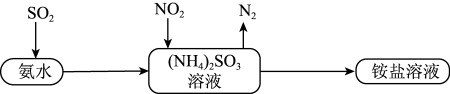
① 被吸收过程的离子方程式是
被吸收过程的离子方程式是_____ 。
②如果将 通入装有
通入装有 、
、 混合溶液的圆底烧瓶中,如下图,可制备大苏打
混合溶液的圆底烧瓶中,如下图,可制备大苏打 ,该反应中仅有硫元素化合价变化,写出反应过程的化学方程式是
,该反应中仅有硫元素化合价变化,写出反应过程的化学方程式是_____ 。

(4)若32.0gCu与一定量的 溶液反应,当Cu反应完时,共产生标准状况下的13.44L气体(NO和
溶液反应,当Cu反应完时,共产生标准状况下的13.44L气体(NO和 ),则消耗的
),则消耗的 溶液中溶质的物质的量为
溶液中溶质的物质的量为_____ 。(相对原子质量Cu:64)
Ⅰ.在学习了硫的转化后,某学生绘制了如图转化关系。

(1)写出
 转化为A的化学方程式:
转化为A的化学方程式:(2)下列四种有色溶液与
 作用均能褪色,体现
作用均能褪色,体现 还原性的是
还原性的是①品红溶液 ②酸性
 溶液 ③碘水 ④滴有酚酞的NaOH溶液
溶液 ③碘水 ④滴有酚酞的NaOH溶液写出
 通入碘水溶液中反应的离子方程式:
通入碘水溶液中反应的离子方程式:(3)工业生产中利用氨水吸收
 和
和 ,原理如图所示:
,原理如图所示:
①
 被吸收过程的离子方程式是
被吸收过程的离子方程式是②如果将
 通入装有
通入装有 、
、 混合溶液的圆底烧瓶中,如下图,可制备大苏打
混合溶液的圆底烧瓶中,如下图,可制备大苏打 ,该反应中仅有硫元素化合价变化,写出反应过程的化学方程式是
,该反应中仅有硫元素化合价变化,写出反应过程的化学方程式是
(4)若32.0gCu与一定量的
 溶液反应,当Cu反应完时,共产生标准状况下的13.44L气体(NO和
溶液反应,当Cu反应完时,共产生标准状况下的13.44L气体(NO和 ),则消耗的
),则消耗的 溶液中溶质的物质的量为
溶液中溶质的物质的量为
您最近一年使用:0次
名校
2 . 硒是一种重要的半导体材料,用富硒铜阳极泥(主要成分为Se、Cu2Se、Ag2Se和银、金等)为原料制备硒的工艺流程如下:
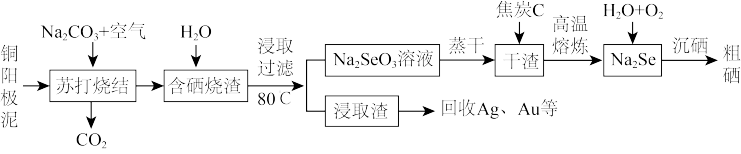
回答下列问题:
(1)试推断34Se在元素周期表中的位置_______ ,据此写出Na2Se的电子式_______ 。
(2)“苏打烧结”时主要发生的化学反应方程式为_______ ;Cu2Se+Na2CO3+2O2=Na2SeO3+CO2+2CuO;Ag2Se+Na2CO3+O2=Na2SeO3+CO2+2Ag。
(3)“含硒烧渣”浸取时需控制温度为80 ℃,则最佳加热方式为_______ ;浸出渣中主要的杂质有_______ 、Ag、Au等。
(4)已知SeO2易溶于水生成H2SeO3,相同温度下,H2SeO3、H2CO3的电离平衡常数如下:
若向Na2CO3溶液中通入过量SeO2,则下列反应的离子方程式正确的是_______。(填字母)
(5)回收硒还可采用另一工艺:即向阳极泥加入浓硫酸,用水吸收生成的SeO2和SO2,试分析此工艺存在的不足之处_______ (答一点即可)。

回答下列问题:
(1)试推断34Se在元素周期表中的位置
(2)“苏打烧结”时主要发生的化学反应方程式为
(3)“含硒烧渣”浸取时需控制温度为80 ℃,则最佳加热方式为
(4)已知SeO2易溶于水生成H2SeO3,相同温度下,H2SeO3、H2CO3的电离平衡常数如下:
| 化学式 | H2SeO3 | H2CO3 |
| 电离平衡常数 | K1=2.7×10-3 K2=2.5×10-8 | K1=4.3×10-7 K2=5.6×10-11 |
A.CO +SeO2 = SeO +SeO2 = SeO +CO2 +CO2 |
B.CO +2SeO2+H2O = 2HSeO +2SeO2+H2O = 2HSeO +CO2 +CO2 |
C.CO +SeO2+H2O = HSeO +SeO2+H2O = HSeO +HCO +HCO |
D.2CO +SeO2+H2O = SeO +SeO2+H2O = SeO +2HCO +2HCO |
您最近一年使用:0次
3 . 分类是认识和研究物质及其变化的一种常用的科学方法。依据物质类别和元素价态,可以对物质的性质进行解释和预测。
Ⅰ、有三种物质: 、
、 、
、
(1)其中氧元素的化合价均为___________ 价。
(2)从氧化剂和还原剂的角度,分析反应中的 作用。请完成下表内容。
作用。请完成下表内容。
(3)由 、
、 的名称可推知
的名称可推知 的名称为
的名称为___________ 。
(4)已知 可与
可与 反应产生
反应产生 ,请写出
,请写出 与水反应的化学方程式
与水反应的化学方程式___________ ,由此可推测 也可做供氧剂。
也可做供氧剂。
II、亚硝酸钠 外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食
外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒。
而中毒。
(5)误食 后可服用维生素
后可服用维生素 解毒。下列分析错误的是___________(填序号)。
解毒。下列分析错误的是___________(填序号)。
(6)我国规定火腿肠中亚硝酸钠添加标准为每千克食品含量不超过150毫克,以此计算,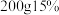 的亚硝酸钠溶液至少可用于生产火腿肠
的亚硝酸钠溶液至少可用于生产火腿肠___________ 千克。
(7)亚硝酸钠在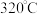 时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。请填写并配平该反应的化学方程式,并用双线桥法标出此反应的电子得失和数目
时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。请填写并配平该反应的化学方程式,并用双线桥法标出此反应的电子得失和数目___________ 。

Ⅰ、有三种物质:
 、
、 、
、
(1)其中氧元素的化合价均为
(2)从氧化剂和还原剂的角度,分析反应中的
 作用。请完成下表内容。
作用。请完成下表内容。| 序号 | 化学反应方程式 | 作用 |
| ① |  | |
| ② |  | |
| ③ | 既作氧化剂,又作还原剂 |
(3)由
 、
、 的名称可推知
的名称可推知 的名称为
的名称为(4)已知
 可与
可与 反应产生
反应产生 ,请写出
,请写出 与水反应的化学方程式
与水反应的化学方程式 也可做供氧剂。
也可做供氧剂。II、亚硝酸钠
 外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食
外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒。
而中毒。(5)误食
 后可服用维生素
后可服用维生素 解毒。下列分析错误的是___________(填序号)。
解毒。下列分析错误的是___________(填序号)。A. 被还原 被还原 | B.维生素 具有还原性 具有还原性 |
C.还原性:维生素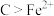 | D. 是还原剂 是还原剂 |
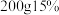 的亚硝酸钠溶液至少可用于生产火腿肠
的亚硝酸钠溶液至少可用于生产火腿肠(7)亚硝酸钠在
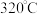 时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。请填写并配平该反应的化学方程式,并用双线桥法标出此反应的电子得失和数目
时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。请填写并配平该反应的化学方程式,并用双线桥法标出此反应的电子得失和数目
您最近一年使用:0次
2022-10-23更新
|
512次组卷
|
2卷引用:广东省中山市2022-2023学年高一上学期期中调研化学试题
4 . 金属钛及其合金密度较小,常温下特别稳定,耐酸碱腐蚀,韧性好,高温下海绵状钛能与氧气反应,是航空、军工、电力等领域的必须金属材料。一种以钛铁矿(主要成份:钛酸亚铁—— )为原料制备金属钛的主要步骤有:
)为原料制备金属钛的主要步骤有:
i.将钛铁矿用浓硫酸溶解,得到含钛化合物和 、
、 的混合溶液
的混合溶液
ii.向步骤i所得的溶液中加入铁粉还原 ,并在273K时析出
,并在273K时析出 晶体以除去铁盐
晶体以除去铁盐
iii.将除去铁盐后的含钛化合物溶液进行一系列处理获得纯净的
iv. 与过量的焦炭、氯气在高温下反应转化为气态
与过量的焦炭、氯气在高温下反应转化为气态 ,然后在充满氩气的容器中用Mg还原,得到海绵状金属钛。
,然后在充满氩气的容器中用Mg还原,得到海绵状金属钛。
回答下列问题
(1) 中Ti元素的化合价为
中Ti元素的化合价为___________ 。
(2)写出步骤ii中向混合溶液加入铁粉时发生反应的离子方程式___________ 。检验加入铁粉后溶液中是否存在 的方法是
的方法是___________ 。
(3)写出步骤iv中 与过量的焦炭、氯气在高温下反应转化为气态
与过量的焦炭、氯气在高温下反应转化为气态 的化学方程式
的化学方程式___________ ,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(4)在氩气中用镁还原出金属钛,氩气的作用是防止___________ 。
 )为原料制备金属钛的主要步骤有:
)为原料制备金属钛的主要步骤有:i.将钛铁矿用浓硫酸溶解,得到含钛化合物和
 、
、 的混合溶液
的混合溶液ii.向步骤i所得的溶液中加入铁粉还原
 ,并在273K时析出
,并在273K时析出 晶体以除去铁盐
晶体以除去铁盐iii.将除去铁盐后的含钛化合物溶液进行一系列处理获得纯净的

iv.
 与过量的焦炭、氯气在高温下反应转化为气态
与过量的焦炭、氯气在高温下反应转化为气态 ,然后在充满氩气的容器中用Mg还原,得到海绵状金属钛。
,然后在充满氩气的容器中用Mg还原,得到海绵状金属钛。回答下列问题
(1)
 中Ti元素的化合价为
中Ti元素的化合价为(2)写出步骤ii中向混合溶液加入铁粉时发生反应的离子方程式
 的方法是
的方法是(3)写出步骤iv中
 与过量的焦炭、氯气在高温下反应转化为气态
与过量的焦炭、氯气在高温下反应转化为气态 的化学方程式
的化学方程式(4)在氩气中用镁还原出金属钛,氩气的作用是防止
您最近一年使用:0次
名校
5 . 按要求填空
(1)我国化学家侯德榜改进国外的纯碱生产工艺,生产流程可简要表示如图
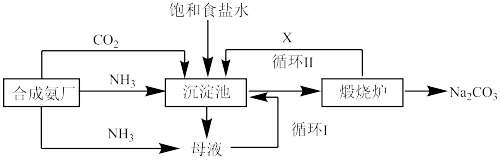
①生产时应往沉淀池中先后通入两种气体,先通入的气体为_______ 上述流程中X物质的化学式_______ 。
②请写出煅烧炉中发生反应的化学反应方程式:_______ 。上述流程中母液中最主要的成分是_______ (填化学式),检验这一组分的阴离子的具体方法是:_______ 。
(2)已知氨气具有还原性,能够和CuO发生氧化还原反应,反应后观察到黑色粉末逐渐变成红色,同时产生了使无水硫酸铜变蓝的物质,还有 一种无污染的气体单质生成,写出该反应的化学方程式:_______
(3)有两瓶无色溶液,分别是K2CO3和NaHCO3,请写出一种能鉴别这两种试剂的方法_______ 。(写出简要操作、现象和结论)
(1)我国化学家侯德榜改进国外的纯碱生产工艺,生产流程可简要表示如图

①生产时应往沉淀池中先后通入两种气体,先通入的气体为
②请写出煅烧炉中发生反应的化学反应方程式:
(2)已知氨气具有还原性,能够和CuO发生氧化还原反应,反应后观察到黑色粉末逐渐变成红色,同时产生了使无水硫酸铜变蓝的物质,还有 一种无污染的气体单质生成,写出该反应的化学方程式:
(3)有两瓶无色溶液,分别是K2CO3和NaHCO3,请写出一种能鉴别这两种试剂的方法
您最近一年使用:0次
名校
6 . 在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图:
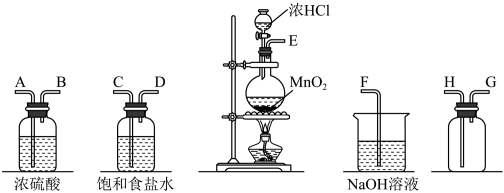
(1)连接上述仪器的正确顺序是(填各接口处的字母): E接_______ ,_______ 接_______ ,B接_______ ,_______ 接F。
(2)上述制备氯气的化学方程式为:_______ 。该反应中浓HCl体现出来的性质:_______ 。
(3)在上述装置中饱和食盐水的作用是_______ , 浓硫酸的作用是_______ 。用离子方程式表示F中NaOH的作用_______ 。
(4)实验中为了检验Cl2有没有收集满,常用湿润的淀粉-KI试纸靠近瓶口,如果Cl2收集满了,可观察到的现象是_______
(5)为了验证氯气的氧化性,将氯气通入Na2SO3溶液中,检验出反应后溶液中含有SO 和Cl-,写出Cl2与Na2SO3反应的离子方程式:
和Cl-,写出Cl2与Na2SO3反应的离子方程式:_______ 。

(1)连接上述仪器的正确顺序是(填各接口处的字母): E接
(2)上述制备氯气的化学方程式为:
(3)在上述装置中饱和食盐水的作用是
(4)实验中为了检验Cl2有没有收集满,常用湿润的淀粉-KI试纸靠近瓶口,如果Cl2收集满了,可观察到的现象是
(5)为了验证氯气的氧化性,将氯气通入Na2SO3溶液中,检验出反应后溶液中含有SO
 和Cl-,写出Cl2与Na2SO3反应的离子方程式:
和Cl-,写出Cl2与Na2SO3反应的离子方程式:
您最近一年使用:0次
名校
7 .  是一种有还原性的气体,可以将
是一种有还原性的气体,可以将 还原为Fe,自身被氧化为
还原为Fe,自身被氧化为 。某学习小组欲制备氨气以还原氧化铁并探究反应产物的成分。
。某学习小组欲制备氨气以还原氧化铁并探究反应产物的成分。
已知:①实验室可用 固体与碱石灰[(NaOH、CaO、
固体与碱石灰[(NaOH、CaO、 的混合物]共热制备氨气。
的混合物]共热制备氨气。
②无水 ——白色粉末,
——白色粉末, 晶体——蓝色晶体
晶体——蓝色晶体
(1)下列各装置中可用于实验室制备氨气的是___________。
(2) 还原
还原 的实验装置如下图:
的实验装置如下图:
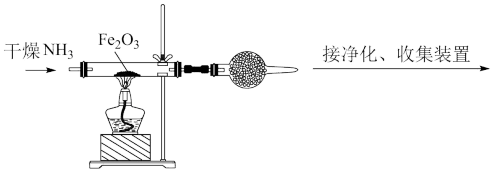
①氨气与氧化铁反应的化学方程式为:___________ 。
②装置右侧干燥管中装有无水硫酸铜,其作用是___________ 。
(3)反应一段时间后试管中固体变为黑色,小组同学为探究黑色固体的成分,进行了如下实验:取反应后黑色固体适量加入足稀盐酸,固体完全溶解,并放出大量气泡。取所得溶液分置于两支试管中,向一支试管中滴入2-3滴KSCN溶液,溶液不变色;向另一支试管中滴加2-3滴酸性 溶液,紫色褪去。
溶液,紫色褪去。
①该小组同学由此确定反应后的黑色固体中不含 ,该结论是否正确?
,该结论是否正确? ___________ (填“是”或“否”);说明你的理由,理由是___________ 。
②假设该反应所得黑色固体的成分只有纯净的铁粉或铁粉与氧化铁的混合物两种可能,请提出一种方案确证之_____________ 。
 是一种有还原性的气体,可以将
是一种有还原性的气体,可以将 还原为Fe,自身被氧化为
还原为Fe,自身被氧化为 。某学习小组欲制备氨气以还原氧化铁并探究反应产物的成分。
。某学习小组欲制备氨气以还原氧化铁并探究反应产物的成分。已知:①实验室可用
 固体与碱石灰[(NaOH、CaO、
固体与碱石灰[(NaOH、CaO、 的混合物]共热制备氨气。
的混合物]共热制备氨气。②无水
 ——白色粉末,
——白色粉末, 晶体——蓝色晶体
晶体——蓝色晶体(1)下列各装置中可用于实验室制备氨气的是___________。
A.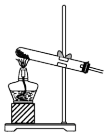 | B. | C.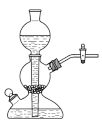 | D.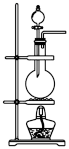 |
 还原
还原 的实验装置如下图:
的实验装置如下图:
①氨气与氧化铁反应的化学方程式为:
②装置右侧干燥管中装有无水硫酸铜,其作用是
(3)反应一段时间后试管中固体变为黑色,小组同学为探究黑色固体的成分,进行了如下实验:取反应后黑色固体适量加入足稀盐酸,固体完全溶解,并放出大量气泡。取所得溶液分置于两支试管中,向一支试管中滴入2-3滴KSCN溶液,溶液不变色;向另一支试管中滴加2-3滴酸性
 溶液,紫色褪去。
溶液,紫色褪去。①该小组同学由此确定反应后的黑色固体中不含
 ,该结论是否正确?
,该结论是否正确? ②假设该反应所得黑色固体的成分只有纯净的铁粉或铁粉与氧化铁的混合物两种可能,请提出一种方案确证之
您最近一年使用:0次
名校
解题方法
8 . 已知NH4CuSO3与足量的10mol·L-1硫酸混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体③溶液呈现蓝色。据此判断下列说法正确的是
| A.反应中硫酸作氧化剂 |
| B.NH4CuSO3中硫元素被氧化 |
| C.刺激性气味的气体是氨气 |
| D.1molNH4CuSO3完全反应转移0.5mol电子 |
您最近一年使用:0次
2021-09-14更新
|
408次组卷
|
93卷引用:广东省中山纪念中学2021届高三上学期第一次月考化学试题
广东省中山纪念中学2021届高三上学期第一次月考化学试题(已下线)江西省重点中学协作体2010届高三第二次联考(化学)(已下线)2011届河南省豫南九校高三上学期第二次联考化学试卷(已下线)2012届黑龙江省牡丹江一中高三上学期期中考试化学试卷(已下线)2012届山东省济宁市邹城二中高三第二次质量检测化学试卷2014届河北衡水中学高三上学期期中考试化学试卷(已下线)2014届黑龙江省佳木斯市第一中学高三第三次调研化学试卷(已下线)2014届河北冀州中学高三上学期期中考试往届化学试卷(已下线)2014高考名师推荐化学氧化还原反应的概念2015届辽宁省抚顺市二中高三上学期期中考试化学试卷2016届河北省衡水中学高三上学期二调化学试卷2016届重庆市万州二中高三上学期9月月考化学试卷2016届山东省潍坊第一中学高三上学期10月月考化学试卷2016届甘肃省天水市第一中学高三上学期期中测试化学试卷2016届山东省青岛市高三上学期期中测试化学试卷2016届江苏省淮安市四星级高中高三上学期10月阶段测化学试卷2016届黑龙江省双鸭山一中高三上学期12月月考化学试卷2015-2016学年湖北省枣阳市第七中学高一上学期期中考试化学试卷2015-2016学年浙江省杭州市五校联盟高三12月月考化学试卷2016届吉林省东北师大附属中学高三上四次模拟化学卷2015-2016学年河南省信阳高级中学高一下开学测化学试卷2016届内蒙古赤峰市宁城县高三下学期第三次统一模拟考试化学试卷2016届内蒙古赤峰二中高三第四次模拟理综化学试卷2016-2017学年河北正定中学高二上开学考试化学卷2017届吉林省松原油田高中高三上第一次阶段测化学卷2017届福建省仙游一中高三上第一次月考化学试卷2017届江西省南昌二中高三上第二次考试化学试卷2017届河北省石家庄辛集中学高三上期中化学试卷2017届河南省周口市淮阳中学高三上10月月考化学试卷2017届内蒙古赤峰市宁城县高三上统一考试化学试卷2017届江西省兴国中学、兴国三中等四校高三上第一次联考化学卷2016-2017学年河北省冀州中学高一上11月月考化学卷2017届辽宁省沈阳东北育才学校高三上期中模拟化学卷2017届江西省兴国中学等四校高三上联考一化学试卷2017届吉林省长春实验中学高三第五次模拟化学卷2016-2017学年湖北省鄂东南省级示范高中高一下学期期中联考化学试卷陕西省西藏民族学院附属中学2017届高三考前冲刺(一)理科综合化学试题辽宁省瓦房店市高级中学2016-2017学年高二下学期期末考试化学试题黑龙江省大庆实验中学2017-2018学年高二上学期开学考试化学试题2018届高三一轮复习化学:微考点11-氧化还原反应的概念江西省临川区第二中学2018届高三上学期第三次月考化学试题湖南省永州市祁阳县第一中学2018届高三10月月考化学试题陕西省西安市长安区第一中学2017-2018学年高一下学期第一次教学质量检测化学试题广西陆川县中学2017-2018学年高一下学期3月月考化学试题【全国百强校】山东师范大学附属中学2017-2018学年高二下学期第八次学分认定(期末)考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期开学阶段性考试(8月)化学试题湖南省湖南师范大学附属中学2019届高三上学期月考(一)化学试题【全国百强校】陕西省陕西师大附属中学2019届高三上学期月考化学试题【全国百强校】湖南省师范大学附属中学2019届高三上学期月考化学试题江西省赣州市会昌中学2019届高三上学期第一次月考(10月)化学试题河北省承德市第一中学2019届高三上学期第三次月考理科综合化学试题山东省商河市第一中学2019届高三上学期11月月考理科综合化学试题山东省滨州市北镇中学2019届高三上学期12月份质量检测化学试题江西省九江市同文中学2019届高三上学期期中考试化学试题山东省济宁市微山县亚马逊中学2019届高三上学期11月月考化学试题江西省上饶市横峰中学2018-2019学年高一下学期开学考试化学试题吉林省东辽五中2020届高三上学期9月月考化学试题江西省临川第二中学2020届高三10月月考化学试题吉林省白城市通榆县第一中学2020届高三上学期第二次月考化学试题山东省济宁市2020届高三10月月考化学试卷山东省济宁市邹城第一中学2020届高三10月月考化学试题甘肃省兰州市第一中学2020届高三上学期9月月考化学试题山东省莱阳市第一中学2020届高三10月月考化学试题吉林省长春市东北师范大学附中2020届高三上学期第一次摸底考试化学试题山东省肥城市泰西中学2019-2020学年高三上学期第一次月考化学试题新疆乌鲁木齐县柴窝堡林场中学2019届高三第三次模拟考试理科综合化学试题陕西省汉中市龙岗学校2019-2020学年高一上学期期中考试化学试题福建省厦门市湖滨中学2020届高三上学期期中考试化学试题四川省宜宾市叙州区第二中学校2019-2020学年高一下学期第一次在线月考化学试题(已下线)【南昌新东方】2018-2019莲塘一中 高三12月 014山东省济宁市汶上圣泽中学2019-2020学年高二下学期第二次检测化学试题(已下线)专题3.4 金属材料及金属矿物的开发利用(练)——2020年高考化学一轮复习讲练测安徽省安庆市2019-2020学年高一下学期期末测试化学试卷吉林省长春外国语学校2020-2021学年高三上学期期初考试化学试题河南省郑州市第一中学2021届高三上学期开学测试化学试题福建省永安市第三中学2021届高三9月月考化学试题吉林省大安市第一中学校2021届高三上学期第二次月考化学试题(已下线)第二章 元素与物质世界(能力提升)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)四川省乐山沫若中学2021届高三上学期第二次理综化学试题江西省高安中学2020-2021学年高一上学期期中考试化学试题四川省射洪中学2019-2020学年高一上期期末英才班能力素质监测化学试题湖南省/(常德市芷兰实验中学2020-2021学年高一上学期第二次月考化学试题河南省信阳高级中学2020-2021学年高一上学期1月月考化学试题福建省莆田第十五中学2020届高三9月月考化学试题(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练云南省昭通市昭阳区第一中学2020-2021学年高一上学期第三次月考化学试题(已下线)【一飞冲天】名家原创卷1河北省廊坊市河北省三河市第一中学2020-2021学年高一下学期第二次阶段考化学试题吉林省大安市第一中学校2021-2022学年高二上学期期初考试化学试题吉林省辉南县第六中学2022届高三上学期第一次月考化学试题 山东省济南市章丘区第四中2022-2023学年高一上学期1月期末线上测试化学试题内蒙古自治区科尔沁左翼中旗实验高级中学2023-2024学年高三上学期11月月考化学试题
解题方法
9 . 黄血盐[亚铁氰化钾,K4Fe(CN)6] 目前广泛用作食品添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为10mg/kg。一种制备黄血盐的工艺如下:

回答下列问题:
(1)步骤I反应的化学方程式为______ 。
(2)步骤IV过滤所得的废液中含量较多的溶质为______ (填化学式)。
(3)步骤V是将难溶的K2CaFe(CN)6与X反应脱钙生成K4Fe(CN)6,所用的试剂X是_____ 。(填名称)
(4)工艺中用到剧毒的HCN溶液,含CN-的废水必须处理后才能排放。
①25℃时Ka(HCN)=6.25×10-10;计算25℃时0.01mol•L-1的HCN溶液的pH=____ (lg2.5=0.4)。
②处理含CN-废水的方法:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN;第二步控制pH为7.5〜8.5,用NaClO溶液完全氧化OCN生成N2和两种盐(其中一种为酸式盐)。
第一步控制强碱性的主要目的是_______ ,第二步反应的离子方程式为______ 。

回答下列问题:
(1)步骤I反应的化学方程式为
(2)步骤IV过滤所得的废液中含量较多的溶质为
(3)步骤V是将难溶的K2CaFe(CN)6与X反应脱钙生成K4Fe(CN)6,所用的试剂X是
(4)工艺中用到剧毒的HCN溶液,含CN-的废水必须处理后才能排放。
①25℃时Ka(HCN)=6.25×10-10;计算25℃时0.01mol•L-1的HCN溶液的pH=
②处理含CN-废水的方法:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN;第二步控制pH为7.5〜8.5,用NaClO溶液完全氧化OCN生成N2和两种盐(其中一种为酸式盐)。
第一步控制强碱性的主要目的是
您最近一年使用:0次
2020-02-01更新
|
188次组卷
|
2卷引用:广东省中山市2019-2020学年高三上学期期末统考化学试题
名校
解题方法
10 . 工业制硫酸的反应原理主要有下列三个反应:
①FeS2(s)+O2(g) Fe2O3(s)+SO2(g);ΔH1
Fe2O3(s)+SO2(g);ΔH1
②2SO2(g)+O2(g) 2SO3(g); ΔH2
2SO3(g); ΔH2
③SO3+H2O=H2SO4
Ⅰ.(1)反应①配平后各物质系数分别为_____ 、______ 、_______ 、______ 。若每生成1molSO2时反应放热426.5kJ,则ΔH1=_______________ 。
(2)工业生产中将FeS2矿石粉碎后投入反应器中反应,这样做的目的是___________ 。
Ⅱ.下表是不同温度和压强下反应②中SO2的转化率
(3)反应②是气体体积缩小的可逆反应,增大压强有利于提高原料转化率,但工业生产中该反应在常压下进行,采用常压生产条件的理由是_______________________ 。
(4)若原料气组成:SO2 7%,O211%,N2 82%,在温度和压强不变的条件下,混合气体体积变为原来的97.2%,则SO2的转化率为_________ 。
Ⅲ.尾气中的二氧化硫对环境造成污染,需要处理后才能排放。常用亚硫酸钠吸收法。
(5)Na2SO3溶液吸收SO2的离子方程式为________________________ ;
(6)常温下,当吸收至pH=6时,吸收液中相关离子浓度关系一定正确的是____ (填序号)
A.c(Na+)+c(H+)>c(SO32-)+c(HSO3-)+c(OH-)
B.c(Na+)=c(SO32-)+c(HSO3-)+C(H2SO3)
C.c(Na+)>c(SO32-)>c(OH-)>c(H+)
D.水电离出c(OH-)=l×l0-8 mol·L-1
①FeS2(s)+O2(g)
 Fe2O3(s)+SO2(g);ΔH1
Fe2O3(s)+SO2(g);ΔH1②2SO2(g)+O2(g)
 2SO3(g); ΔH2
2SO3(g); ΔH2 ③SO3+H2O=H2SO4
Ⅰ.(1)反应①配平后各物质系数分别为
(2)工业生产中将FeS2矿石粉碎后投入反应器中反应,这样做的目的是
Ⅱ.下表是不同温度和压强下反应②中SO2的转化率
| 0.1Mp | 0.5Mp | 1Mp | 10Mp | |
| 400℃ | 99.2 | 99.6 | 99.7 | 99.9 |
| 500℃ | 93.5 | 96.9 | 97.8 | 99.3 |
| 600℃ | 73.7 | 85.8 | 89.5 | 96.4 |
(3)反应②是气体体积缩小的可逆反应,增大压强有利于提高原料转化率,但工业生产中该反应在常压下进行,采用常压生产条件的理由是
(4)若原料气组成:SO2 7%,O211%,N2 82%,在温度和压强不变的条件下,混合气体体积变为原来的97.2%,则SO2的转化率为
Ⅲ.尾气中的二氧化硫对环境造成污染,需要处理后才能排放。常用亚硫酸钠吸收法。
(5)Na2SO3溶液吸收SO2的离子方程式为
(6)常温下,当吸收至pH=6时,吸收液中相关离子浓度关系一定正确的是
A.c(Na+)+c(H+)>c(SO32-)+c(HSO3-)+c(OH-)
B.c(Na+)=c(SO32-)+c(HSO3-)+C(H2SO3)
C.c(Na+)>c(SO32-)>c(OH-)>c(H+)
D.水电离出c(OH-)=l×l0-8 mol·L-1
您最近一年使用:0次
2019-11-30更新
|
96次组卷
|
2卷引用:广东省中山市第一中学2019-2020学年高二上学期第二次段考化学试题



