名校
1 . 酸性条件下, 与
与 按物质的量
按物质的量 恰好完全反应,生成的产物能使淀粉溶液变蓝,请完成下列离子方程式的填空与配平。
恰好完全反应,生成的产物能使淀粉溶液变蓝,请完成下列离子方程式的填空与配平。
( ) H++( ) NO2-+( ) I-→( ) +( ) +( ) H2O
根据上述离子方程式,1摩尔 参与反应则转移的电子数目是
参与反应则转移的电子数目是______ ,反应中被还原的元素是______ 。
 与
与 按物质的量
按物质的量 恰好完全反应,生成的产物能使淀粉溶液变蓝,请完成下列离子方程式的填空与配平。
恰好完全反应,生成的产物能使淀粉溶液变蓝,请完成下列离子方程式的填空与配平。根据上述离子方程式,1摩尔
 参与反应则转移的电子数目是
参与反应则转移的电子数目是
您最近一年使用:0次
2014·上海金山·一模
2 . 二氧化硫和氮氧化物(NOx)是大气的主要污染物,治理环境污染是当前环保工作的重要研究内容之一。
完成下列计算:
(1)石灰石-石膏湿法烟气脱硫工艺技术的原理是:烟气中的二氧化硫与浆液中的碳酸钙以及空气反应生成石膏(CaSO4·2H2O)。某电厂用煤300t(煤中含硫的质量分数为2.5%),若燃烧时煤中的硫全部转化为二氧化硫,用该方法脱硫时有96%的硫转化为石膏,则理论上可得到_________ 吨石膏。
(2)用CH4催化还原NOx,主要产物为N2与CO2。现有1 L NOx(含NO2、NO),用CH4将其还原成N2,消耗同温同压下的CH40.4 L,则混合气体中NO2、NO的物质量之比为____ 。
(3)乙二酸(H2C2O4)的制备有如下反应:
C6H12O6+18HNO3→3H2C2O4+18NO2↑+12H2O
C6H12O6+6HNO3→3H2C2O4+6NO↑+6H2O
上述反应产生的NOx用氧气和水吸收后生成硝酸循环利用,若尾气NOx中n(NO2)︰n(NO)=2︰1,且NOx的吸收转化率为90%。每生产9 kg乙二酸至少需要补充质量分数为63%的硝酸溶液多少千克?____
(4)用碱液吸收法处理某工业尾气(含NOx:NO、NO2和N2O4)的反应为:
2NO2+ 2NaOH→ NaNO2+ NaNO3 + H2O;
NO + NO2+ 2NaOH→ 2NaNO2+ H2O。
当N2O4体积分数为0.2时,处理1mol该NOx,计算生成NaNO3和NaNO2的物质的量(x可作为已知条件使用)。____
完成下列计算:
(1)石灰石-石膏湿法烟气脱硫工艺技术的原理是:烟气中的二氧化硫与浆液中的碳酸钙以及空气反应生成石膏(CaSO4·2H2O)。某电厂用煤300t(煤中含硫的质量分数为2.5%),若燃烧时煤中的硫全部转化为二氧化硫,用该方法脱硫时有96%的硫转化为石膏,则理论上可得到
(2)用CH4催化还原NOx,主要产物为N2与CO2。现有1 L NOx(含NO2、NO),用CH4将其还原成N2,消耗同温同压下的CH40.4 L,则混合气体中NO2、NO的物质量之比为
(3)乙二酸(H2C2O4)的制备有如下反应:
C6H12O6+18HNO3→3H2C2O4+18NO2↑+12H2O
C6H12O6+6HNO3→3H2C2O4+6NO↑+6H2O
上述反应产生的NOx用氧气和水吸收后生成硝酸循环利用,若尾气NOx中n(NO2)︰n(NO)=2︰1,且NOx的吸收转化率为90%。每生产9 kg乙二酸至少需要补充质量分数为63%的硝酸溶液多少千克?
(4)用碱液吸收法处理某工业尾气(含NOx:NO、NO2和N2O4)的反应为:
2NO2+ 2NaOH→ NaNO2+ NaNO3 + H2O;
NO + NO2+ 2NaOH→ 2NaNO2+ H2O。
当N2O4体积分数为0.2时,处理1mol该NOx,计算生成NaNO3和NaNO2的物质的量(x可作为已知条件使用)。
您最近一年使用:0次
名校
3 . 氯化铁和摩尔盐是铁的两种重要盐类,在净水和定量分析等方面具有重要作用。
(1) 用FeCl3溶液腐蚀印刷电路板上的铜,向所得溶液中加入铁粉,对加入铁粉充分反应后的溶液分析合理的是____________ 。
a. 若无固体剩余,则溶液中一定有Fe3+ b. 若有固体存在,则溶液中一定有Fe2+
c. 若溶液中有Cu2+,则一定没有固体析出 d. 若溶液中有Fe2+,则一定有Cu析出
(2)工业上通过氧化酸性FeCl2废液得到含FeCl3的溶液。若酸性FeCl2废液中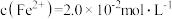 ,
,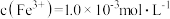 ,
,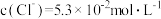 ,则该溶液的
,则该溶液的 约为
约为______ (不考虑水的电离和离子的水解)。
(3)摩尔盐 [(NH4)2Fe(SO4)2•6H2O]在定量分析中常作为基准物质,用来标定重铬酸钾、高锰酸钾等溶液的浓度,在 的该盐的溶液中,离子浓度由大到小的顺序是
的该盐的溶液中,离子浓度由大到小的顺序是____________ 。
(4)摩尔盐与酸性高锰酸钾发生反应: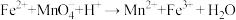
a.配平上述离子方程式:( ) Fe2++( ) MnO4-+( ) H+→( ) Mn2++( ) Fe3++( ) H2O
b.已知摩尔盐相对分子质量为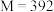 ,取摩尔盐产品
,取摩尔盐产品 (杂质不与高锰酸钾反应),配成
(杂质不与高锰酸钾反应),配成 溶液,取出
溶液,取出 用
用 溶液滴定,消耗
溶液滴定,消耗 溶液
溶液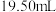 ,则产品中摩尔盐的质量分数为
,则产品中摩尔盐的质量分数为____________ (用小数表示,保留四位小数)。
(1) 用FeCl3溶液腐蚀印刷电路板上的铜,向所得溶液中加入铁粉,对加入铁粉充分反应后的溶液分析合理的是
a. 若无固体剩余,则溶液中一定有Fe3+ b. 若有固体存在,则溶液中一定有Fe2+
c. 若溶液中有Cu2+,则一定没有固体析出 d. 若溶液中有Fe2+,则一定有Cu析出
(2)工业上通过氧化酸性FeCl2废液得到含FeCl3的溶液。若酸性FeCl2废液中
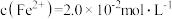 ,
,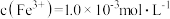 ,
,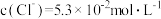 ,则该溶液的
,则该溶液的 约为
约为(3)摩尔盐 [(NH4)2Fe(SO4)2•6H2O]在定量分析中常作为基准物质,用来标定重铬酸钾、高锰酸钾等溶液的浓度,在
 的该盐的溶液中,离子浓度由大到小的顺序是
的该盐的溶液中,离子浓度由大到小的顺序是(4)摩尔盐与酸性高锰酸钾发生反应:
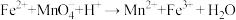
a.配平上述离子方程式:
b.已知摩尔盐相对分子质量为
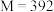 ,取摩尔盐产品
,取摩尔盐产品 (杂质不与高锰酸钾反应),配成
(杂质不与高锰酸钾反应),配成 溶液,取出
溶液,取出 用
用 溶液滴定,消耗
溶液滴定,消耗 溶液
溶液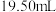 ,则产品中摩尔盐的质量分数为
,则产品中摩尔盐的质量分数为
您最近一年使用:0次
2011·上海长宁·二模
4 . Cu、Cu2O和CuO组成的混合物,加入100mL0.6 mol·L-1HNO3溶液恰好使混合物完全溶解,完全生成硝酸铜、一氧化氮和水。现共收集到224mLNO气体(标准状况)。求:
(1)相同物质的量的Cu、Cu2O和CuO,消耗该浓度硝酸最多的是哪一种物质,写出其与该硝酸反应的离子方程式。________ ,_______________________________ 。
(2)如原混合物中含单质铜0.01moL,则其中Cu2O、CuO的物质的量分别为多少________ ,__________ ?
(3)求混合物中CuO的物质的量可能接近的最大值__________ 。
(1)相同物质的量的Cu、Cu2O和CuO,消耗该浓度硝酸最多的是哪一种物质,写出其与该硝酸反应的离子方程式。
(2)如原混合物中含单质铜0.01moL,则其中Cu2O、CuO的物质的量分别为多少
(3)求混合物中CuO的物质的量可能接近的最大值
您最近一年使用:0次
名校
解题方法
5 . 土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理为:
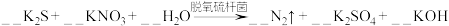 。
。
(1)配平上述反应方程式,并用单线桥标出电子转移的方向和数目___________ 。
(2)被氧化的元素是___________ 。
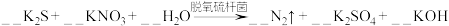 。
。(1)配平上述反应方程式,并用单线桥标出电子转移的方向和数目
(2)被氧化的元素是
您最近一年使用:0次
6 . 硫化钠是用于皮革鞣制的重要化学试剂,可用无水芒硝(Na2SO4)与炭粉在高温下反应而制得,反应方程式如下:Na2SO4+4C →Na2S+ 4CO,Na2SO4+4CO→Na2S+4CO2
(1)现有无水芒硝17.75g,若生成过程中无水芒硝的利用率为80%,则理论上可得到Na2S_____ g,最多生成标况下的CO_____ L。
(2)若在反应过程中生成的Na2S3mol,则消耗的碳单质的物质的量 n的范围是____ mol≤n≤___ mol,若生成等物质的量CO和CO2,则消耗的碳的物质的量为____ mol。
(3)Na2S放置在空气中,会被缓慢氧化成Na2SO4及 Na2SO3,现称取已经部分氧化的硫化钠样品78.40g溶于水中,加入足量盐酸,充分反应后过滤得沉淀19.20g,放出H2S气体2.24L(标准状况)。请计算:78.40g样品中各氧化产物的物质的量(写出必要的计算过程)。_____
(1)现有无水芒硝17.75g,若生成过程中无水芒硝的利用率为80%,则理论上可得到Na2S
(2)若在反应过程中生成的Na2S3mol,则消耗的碳单质的物质的量 n的范围是
(3)Na2S放置在空气中,会被缓慢氧化成Na2SO4及 Na2SO3,现称取已经部分氧化的硫化钠样品78.40g溶于水中,加入足量盐酸,充分反应后过滤得沉淀19.20g,放出H2S气体2.24L(标准状况)。请计算:78.40g样品中各氧化产物的物质的量(写出必要的计算过程)。
您最近一年使用:0次
11-12高二上·上海·期中
7 . 将10g铁粉置于40mL较浓的硝酸中,微热完全反应时,收集到NO2和NO混合气体1792mL(标准状况下),还残留4.4g固体。求:
(1)该反应中被还原的硝酸和未被还原的硝酸的物质的量之比_______ ;
(2)原硝酸的物质的量浓度_______ ;
(3)NO和NO2的体积比_______ ;
(4)写出总的化学方程式_______ 。
(1)该反应中被还原的硝酸和未被还原的硝酸的物质的量之比
(2)原硝酸的物质的量浓度
(3)NO和NO2的体积比
(4)写出总的化学方程式
您最近一年使用:0次
2011·上海嘉定·一模
8 . (1)配平反应的离子方程式:_____ XeO3+____ Mn2++_____ H2O →____ MnO4-+____ Xe↑+___ H+
(2)反应现象为:①有气泡产生,②______________________ 。
(3)发生氧化反应的物质(或微粒)是_______________ 。
(4)将适量的XeO3投入30mL 0.1mol⋅L−1 Mn2+的水溶液中,刚好完全反应。
①此时转移电子_____________ mol。
②将反应后的溶液稀释至90mL,所得溶液的pH=________ 。
(2)反应现象为:①有气泡产生,②
(3)发生氧化反应的物质(或微粒)是
(4)将适量的XeO3投入30mL 0.1mol⋅L−1 Mn2+的水溶液中,刚好完全反应。
①此时转移电子
②将反应后的溶液稀释至90mL,所得溶液的pH=
您最近一年使用:0次
2011·上海长宁·二模
9 . 钾是活泼的碱金属,钾和氧有氧化钾(K2O)、过氧化钾(K2O2)和超氧化钾(KO2)等多种化合物。
⑴钾和硝酸钾反应可制得氧化钾:K+KNO3→K2O+N2(未配平),每生成9.4gK2O消耗的还原剂有___________ g
⑵超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂。写出超氧化钾与二氧化碳反应的化学方程式______________________ ,为了维持气压稳定,可以使用超氧化钾和过氧化钾的混合物使吸收的CO2与生成的O2体积相同(同温同压),则它们的物质的量之比为n(KO2) :n(K2O2)=____________
⑶KO2加热至600℃部分分解得到产物A。6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比_______ 。如果产物A只含有两种化合物,写出所有可能的化学式并计算A中两种化合物的物质的量之比_______ 。
⑴钾和硝酸钾反应可制得氧化钾:K+KNO3→K2O+N2(未配平),每生成9.4gK2O消耗的还原剂有
⑵超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂。写出超氧化钾与二氧化碳反应的化学方程式
⑶KO2加热至600℃部分分解得到产物A。6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比
您最近一年使用:0次



