名校
1 .  、
、 的资源化利用既能解决环保问题,又能提供化工原料,解决能源紧张,具有重要的现实意义和广阔的应用前景。
的资源化利用既能解决环保问题,又能提供化工原料,解决能源紧张,具有重要的现实意义和广阔的应用前景。
(1)利用 可合成多种化工产品。
可合成多种化工产品。
① 与
与 能在催化剂表面反应生成优质气体燃料
能在催化剂表面反应生成优质气体燃料 和
和 ,该反应的化学方程式为
,该反应的化学方程式为__ 。
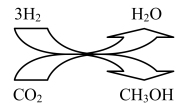
②2021年9月24日我国科学家首次报告了 到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为
到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为___________ 。
(2) 是一种酸性氧化物,可用氨水吸收烟气中的
是一种酸性氧化物,可用氨水吸收烟气中的 。
。
① 属于
属于___________ (填“电解质”或“非电解质”),标准状况下,1体积水约能溶解 体积
体积 ,所得氨水密度为
,所得氨水密度为 ,则该氨水的物质的量浓度为
,则该氨水的物质的量浓度为___________ 。
②氨水吸收少量 ,可生成
,可生成 ,反应的离子方程式为
,反应的离子方程式为___________ 。所得溶液再用 氧化,可制得化肥
氧化,可制得化肥 ,反应的化学方程式为
,反应的化学方程式为___________ 。
 、
、 的资源化利用既能解决环保问题,又能提供化工原料,解决能源紧张,具有重要的现实意义和广阔的应用前景。
的资源化利用既能解决环保问题,又能提供化工原料,解决能源紧张,具有重要的现实意义和广阔的应用前景。(1)利用
 可合成多种化工产品。
可合成多种化工产品。
①
 与
与 能在催化剂表面反应生成优质气体燃料
能在催化剂表面反应生成优质气体燃料 和
和 ,该反应的化学方程式为
,该反应的化学方程式为②2021年9月24日我国科学家首次报告了
 到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为
到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为(2)
 是一种酸性氧化物,可用氨水吸收烟气中的
是一种酸性氧化物,可用氨水吸收烟气中的 。
。①
 属于
属于 体积
体积 ,所得氨水密度为
,所得氨水密度为 ,则该氨水的物质的量浓度为
,则该氨水的物质的量浓度为②氨水吸收少量
 ,可生成
,可生成 ,反应的离子方程式为
,反应的离子方程式为 氧化,可制得化肥
氧化,可制得化肥 ,反应的化学方程式为
,反应的化学方程式为
您最近一年使用:0次
2 . 尿素[CO(NH2)2]的合成与利用,体现了化学科学与技术的不断进步。
(1) 与
与 在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为
在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为___________ 。
(2)电催化法合成尿素
2021年,科学家设计出一种在 催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。
催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。


①甲醛和羟胺( )缩合生成甲胺(
)缩合生成甲胺( )的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了
)的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了___________ 化学键。
②已知在制备和反应过程中,催化剂表面的电子能自发从 端转移到Bi端,
端转移到Bi端, 能成功吸附在Bi端的原因可能是
能成功吸附在Bi端的原因可能是___________ 。
③实际生产时可忽略步骤Ⅲ可能出现的副产物 和
和 ,原因是
,原因是___________ 。
(3)尿素能应用于脱除烟气中的污染物。控制其他条件相同,将混有 、
、 、
、 、
、 和
和 的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测
的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测 、
、 的脱除率
的脱除率 [
[ ]。
]。
①实验测得,烟气中少量 有利于
有利于 的脱除,这是利用了
的脱除,这是利用了 的
的___________ 性。
②当无 存在,且烟气中
存在,且烟气中 与
与 的物质的量浓度相等时,
的物质的量浓度相等时, 达到最大值。该条件下尿素脱除
达到最大值。该条件下尿素脱除 的化学反应方程式为
的化学反应方程式为___________ 。
③当无 存在,且烟气中
存在,且烟气中 超过一定数值时,测得
超过一定数值时,测得 变为负值,其原因是
变为负值,其原因是___________ 。
(1)
 与
与 在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为
在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为(2)电催化法合成尿素
2021年,科学家设计出一种在
 催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。
催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。

①甲醛和羟胺(
 )缩合生成甲胺(
)缩合生成甲胺( )的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了
)的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了②已知在制备和反应过程中,催化剂表面的电子能自发从
 端转移到Bi端,
端转移到Bi端, 能成功吸附在Bi端的原因可能是
能成功吸附在Bi端的原因可能是③实际生产时可忽略步骤Ⅲ可能出现的副产物
 和
和 ,原因是
,原因是(3)尿素能应用于脱除烟气中的污染物。控制其他条件相同,将混有
 、
、 、
、 、
、 和
和 的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测
的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测 、
、 的脱除率
的脱除率 [
[ ]。
]。①实验测得,烟气中少量
 有利于
有利于 的脱除,这是利用了
的脱除,这是利用了 的
的②当无
 存在,且烟气中
存在,且烟气中 与
与 的物质的量浓度相等时,
的物质的量浓度相等时, 达到最大值。该条件下尿素脱除
达到最大值。该条件下尿素脱除 的化学反应方程式为
的化学反应方程式为③当无
 存在,且烟气中
存在,且烟气中 超过一定数值时,测得
超过一定数值时,测得 变为负值,其原因是
变为负值,其原因是
您最近一年使用:0次
2023-10-17更新
|
259次组卷
|
2卷引用:江苏省决胜新高考部分学校2023-2024学年高三上学期10月大联考化学试题
解题方法
3 . 根据文字信息书写相应的方程式。
(1)PH3有剧毒,用硫酸铜溶液吸收,生成物含Cu3P沉淀、磷酸,反应的离子方程式为____ 。
(2)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂。工业上用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得,反应过程中还有CO2等生成,且n(CO2):n(ClO2)=1:2。该反应的化学方程式是____ 。
(3)CuCl难溶于水,常用作有机合成催化剂,实验室以铜矿粉(主要含Cu2S及少量Fe2O3、FeCO3等)为原料制备CuCl的流程如图:
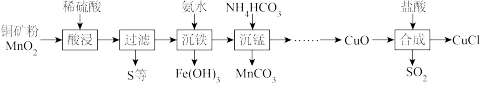
①“酸浸”时,Cu2S所发生反应的离子方程式为____ 。
②“沉锰”时有CO2气体放出,该反应的化学方程式为____ 。
③“合成”反应的化学方程式为____ 。
(1)PH3有剧毒,用硫酸铜溶液吸收,生成物含Cu3P沉淀、磷酸,反应的离子方程式为
(2)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂。工业上用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得,反应过程中还有CO2等生成,且n(CO2):n(ClO2)=1:2。该反应的化学方程式是
(3)CuCl难溶于水,常用作有机合成催化剂,实验室以铜矿粉(主要含Cu2S及少量Fe2O3、FeCO3等)为原料制备CuCl的流程如图:

①“酸浸”时,Cu2S所发生反应的离子方程式为
②“沉锰”时有CO2气体放出,该反应的化学方程式为
③“合成”反应的化学方程式为
您最近一年使用:0次
解题方法
4 . 碘化钠在医疗及食品方面有重要的作用,实验室以NaOH、单质碘和水合肼N2H4•H2O(有还原性)为原料制备碘化钠。回答下列有关问题:
(1)利用下列实验装置制取次氯酸钠和氢氧化钠混合液。
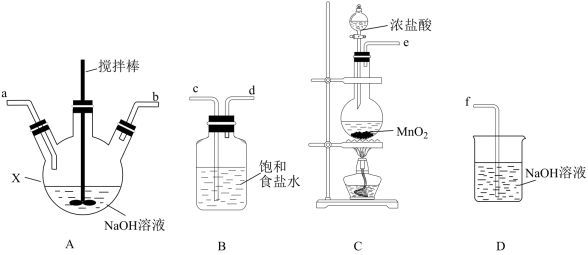
①仪器X的名称是___________ ,导管口连接顺序为___________ (按气流方向,用小写字母表示)。
②若该实验温度控制不当,反应后测得装置A内ClO﹣与ClO 的物质的量之比为5:1,则A中反应的化学方程式是
的物质的量之比为5:1,则A中反应的化学方程式是___________ 。
(2)制备水合肼:反应原理为CO(NH2)2(尿素)+NaClO+NaOH=N2H4•H2O+NaCl+Na2CO3。
①将次氯酸钠和氢氧化钠混合液缓慢滴加到尿素溶液中,边加边搅拌。该操作需严格控制试剂的滴加顺序和滴加速度,原因是___________ 。
②N2H4•H2O一级电离方程式为N2H4•H2O=N2H +OH﹣,其二级电离方程式为
+OH﹣,其二级电离方程式为___________ 。
(3)碘化钠的制备:采用水合肼还原法制取碘化钠固体,其制备流程如图所示。
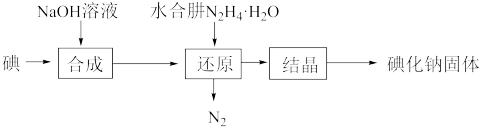
①“还原”过程主要消耗“合成”中生成的副产物IO ,反应的离子方程式是
,反应的离子方程式是___________
②工业上也可用硫化钠或铁屑还原碘酸钠制备碘化钠,“水合肼还原法”的优点是___________ 。
(1)利用下列实验装置制取次氯酸钠和氢氧化钠混合液。

①仪器X的名称是
②若该实验温度控制不当,反应后测得装置A内ClO﹣与ClO
 的物质的量之比为5:1,则A中反应的化学方程式是
的物质的量之比为5:1,则A中反应的化学方程式是(2)制备水合肼:反应原理为CO(NH2)2(尿素)+NaClO+NaOH=N2H4•H2O+NaCl+Na2CO3。
①将次氯酸钠和氢氧化钠混合液缓慢滴加到尿素溶液中,边加边搅拌。该操作需严格控制试剂的滴加顺序和滴加速度,原因是
②N2H4•H2O一级电离方程式为N2H4•H2O=N2H
 +OH﹣,其二级电离方程式为
+OH﹣,其二级电离方程式为(3)碘化钠的制备:采用水合肼还原法制取碘化钠固体,其制备流程如图所示。

①“还原”过程主要消耗“合成”中生成的副产物IO
 ,反应的离子方程式是
,反应的离子方程式是②工业上也可用硫化钠或铁屑还原碘酸钠制备碘化钠,“水合肼还原法”的优点是
您最近一年使用:0次
名校
解题方法
5 . 化学与生活密切相关。下列说法错误的是
| A.雾和霾是气溶胶,PM2.5被认为是造成雾霾天气的“元凶” |
| B.2021年我国科学家以CO2为原料合成淀粉,为缓解温室效应带来新的希望 |
| C.二氧化硫可用作葡萄酒的食品添加剂,用来杀死有害细菌,防止色素被氧化 |
| D.新型水处理剂Na2FeO4利用其强氧化性对病菌和悬浮物进行高效处理 |
您最近一年使用:0次
2022-02-26更新
|
2359次组卷
|
5卷引用:湘豫名校2022届高三1月联考理科综合化学试题
湘豫名校2022届高三1月联考理科综合化学试题(已下线)专项01 化学与STSE-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)广东省茂名高州市校际联盟2021-2022学年高一5月联考化学试题黑龙江省哈尔滨市第九中学校2022届高考最后押题卷(一)化学试题安徽省六安市晓天中学2021-2022学年高一下学期第一次月考化学试题



