1 . 某同学为验证Fe3+的氧化性进行了如下实验:
已知相同条件下AgCl的溶解度小于Ag2SO4.下列说法不正确的是
| 序号 | 操作 | 现象 |
| 实验I | 将2 mL 2 mol∙L−1Fe(NO3)3溶液加入有银镜的试管中 | 银镜消失 |
| 实验II | 将2 mL1 mol∙L−1 Fe2(SO4)3溶液加入有银镜的试管中 | 银镜减少,未消失 |
| 实验III | 将2mL2 mol∙L−1FeCl3溶液加入有银镜的试管中 | 银镜消失 |
| 实验IV | 将2mL 1 mol∙L−1 AgNO3溶液加入到1 mL 1 mol∙L−1 FeSO4溶液中 | 产生白色沉淀,随后有黑色固体产生 |
| A.实验I不能说明Fe3+氧化了Ag |
B.实验II和III说明溶液中存在平衡: Fe3++Ag Fe2++ Ag+ Fe2++ Ag+ |
| C.实验IV中产生白色沉淀,说明Ag+氧化了Fe2+ |
| D.欲证明实验IV中产生了Fe3+,可以取上层清液滴加KSCN溶液 |
您最近一年使用:0次
名校
2 . 双氧水和84消毒液是生活中常用的两种消毒剂,了解物质的性质是科学合理使用化学品的基础和前提,请回答下列问题:
(1)某同学设计如下实验研究H2O2的性质
①从理论上看H2O2既有氧化性又有还原性,原因是___________ 。
②能证明H2O2具有还原性的实验是___________ (填序号),可作为证据的实验现象是___________ (填字母)。
(2)84消毒液的有效成分为NaClO;
①84消毒液不能和洁厕灵(主要成分为较高浓度的盐酸)混用,否则易产生有毒气体,反应的化学方程式为___________ 。
②巴西奥运会期间,由于工作人员将84消毒液与双氧水混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应中氧化性:NaClO___________ H2O2 (填“>”或“<”)。反应的离子反应方程式为___________ 。
(1)某同学设计如下实验研究H2O2的性质
| 序号 | 实验 | 实验现象 |
| ⅰ | 向5% H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ⅱ | 向5% H2O2溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
②能证明H2O2具有还原性的实验是
(2)84消毒液的有效成分为NaClO;
①84消毒液不能和洁厕灵(主要成分为较高浓度的盐酸)混用,否则易产生有毒气体,反应的化学方程式为
②巴西奥运会期间,由于工作人员将84消毒液与双氧水混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应中氧化性:NaClO
您最近一年使用:0次
名校
解题方法
3 . 铁是人类较早使用的金属之一,如图为铁及其化合物的“价—类”二维图。
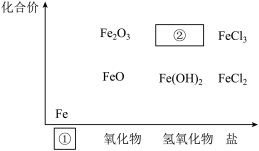
(1)填写二维图缺失的类别①___ 和化学式②___ 。
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:①Cl2②Fe③NaOH④H2SO4⑤AgNO3。从物质类别上看,FeCl3属于___ ,可能与___ 发生反应(填序号);从化合价角度看,Fe3+具有___ 性,可能与___ 发生反应(填序号)。
(3)下列含铁元素物质既有氧化性又有还原性的是___ (用字母代号填)。
A.Fe B.FeCl3 C.FeSO4 D.Fe2O3
(4)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是___ 。
(5)检验溶液中存在Fe3+的试剂是___ ,证明Fe3+存在的现象是___ 。

(1)填写二维图缺失的类别①
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:①Cl2②Fe③NaOH④H2SO4⑤AgNO3。从物质类别上看,FeCl3属于
(3)下列含铁元素物质既有氧化性又有还原性的是
A.Fe B.FeCl3 C.FeSO4 D.Fe2O3
(4)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是
(5)检验溶液中存在Fe3+的试剂是
您最近一年使用:0次
2020-12-07更新
|
335次组卷
|
2卷引用:福建省三明市泰宁县福建省泰宁第一中学2019-2020学年高一上学期第二次阶段考试化学试题
名校
解题方法
4 . 下列实验设计及其对应的离子方程式均正确的是
| A.将氯气溶于水制备次氯酸: Cl2+H2O = 2H+ Cl-+ ClO- |
| B.Na2O2与H2O反应制备O2: Na2O2+H2O = 2Na++ 2OH-+ O2↑ |
C.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO + 6H++ 5H2O2 = 2Mn2++ 5O2↑+ 8H2O + 6H++ 5H2O2 = 2Mn2++ 5O2↑+ 8H2O |
| D.用FeCl3溶液腐蚀铜线路板: Cu+2Fe3+ = Cu2+ +2Fe2+ |
您最近一年使用:0次
名校
5 . 已知:①在无色的MnSO4溶液中滴加过二硫酸铵(NH4)2S2O8溶液,溶液变紫红色;②在酸化的KMnO4溶液中滴加H2O2,产生大量气泡;③在含KSCN的FeSO4溶液中滴加硫酸酸化的H2O2,溶液变血红色。下列有关推断正确的是
| A.反应②中用盐酸酸化KMnO4溶液 |
| B.氧化性:(NH4)2S2O8>KMnO4>H2O2>Fe3+ |
| C.若①中还原产物为SO42-,则氧化剂、还原剂的物质的量之比为2:5 |
| D.在Fe(NO3)2溶液中滴加酸化的H2O2,也可证明H2O2的氧化性比Fe3+的强 |
您最近一年使用:0次
2019-11-03更新
|
124次组卷
|
2卷引用:安徽省全国示范高中名校2020届高三9月联考化学试题
填空题
|
较易(0.85)
|
名校
6 . (1)①在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,这是因为________ ,离子方程式为__________________ 。
②在碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠碱性溶液,发现蓝色逐渐消失,这是因为________ ,离子方程式是__________________ 。
①浓硫酸的氧化性比稀硫酸强____________ 。
②氯化铁溶液中Fe3+的氧化性比硫酸铜溶液中的Cu2+强_____________ 。
③铁的还原性比铜强____________ 。
②在碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠碱性溶液,发现蓝色逐渐消失,这是因为
③对比①和②实验所得的结果,将I2、ClO-、SO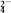 按氧化性由强到弱的顺序排列为
按氧化性由强到弱的顺序排列为
①浓硫酸的氧化性比稀硫酸强
②氯化铁溶液中Fe3+的氧化性比硫酸铜溶液中的Cu2+强
③铁的还原性比铜强
您最近一年使用:0次
7 . 过氧化钠和氢化钠(NaH),广泛应用于工业生产.
(1)氢化钠(NaH)中氢元素的化合价为_____________ .
(2)NaH能与水剧烈反应:NaH+H2O═NaOH+H2↑,该反应中的氧化剂是_________ ,氧化剂与还原剂的物质的量之比是_____________ .
(3)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,该反应的化学方程式为_____________________ .
(4)过氧化钠是呼吸面和防毒面具中氧气的来源,写出过氧化钠与二氧化碳反应的化学方程式______________ ,证明有氧气产生的方法是______________ .
(1)氢化钠(NaH)中氢元素的化合价为
(2)NaH能与水剧烈反应:NaH+H2O═NaOH+H2↑,该反应中的氧化剂是
(3)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,该反应的化学方程式为
(4)过氧化钠是呼吸面和防毒面具中氧气的来源,写出过氧化钠与二氧化碳反应的化学方程式
您最近一年使用:0次
10-11高三上·广东·阶段练习
8 . 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品、用上图中的实验装置进行实验,证明过氧化钠可作供氧剂。
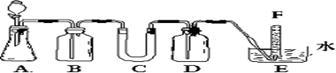
(1)A是实验室制取CO2的装置。写出A中发生反应的离子方程式:_______________ 。
(2)B装置中装有饱和的NaHCO3溶液,其作用是:___________________________ 。
(3)写出过氧化钠与二氧化碳反应的化学方程式:_____________________________ 。
该反应中氧化剂是________ ,还原剂是_________ ,反应过程中氧化剂与还原剂的物质的量之比为_____________ 。

(1)A是实验室制取CO2的装置。写出A中发生反应的离子方程式:
(2)B装置中装有饱和的NaHCO3溶液,其作用是:
(3)写出过氧化钠与二氧化碳反应的化学方程式:
该反应中氧化剂是
您最近一年使用:0次
解题方法
9 . 铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
(1)所含铁元素既有氧化性又有还原性的物质是________(用字母代号填)。
(2)向沸水中逐滴滴加1 mol/L FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是________ nm。
(3)电子工业需要用30 %的FeCl3溶液腐蚀敷在绝缘板上的铜片制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式_____________________ 。某同学对FeCl3腐蚀铜后所得溶液的组成进行测定:取少量待测溶液,滴入KSCN溶液呈红色,则溶液中所含金属阳离子有___________ 。
(4)若要验证该溶液中含有Fe2+,正确的实验方法是___________ (用字母代号填)。
A.向试管中加入试液,滴入KSCN溶液,若显血红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+
(5)欲从废液中回收铜,并重新获得FeCl3溶液设计实验方案如下:
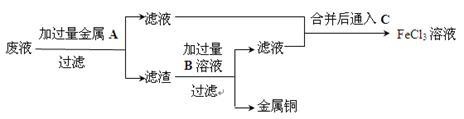
①写出上述实验中有关物质的化学式:A:_____________ ;B:_____________ 。
②写出通入C的化学方程式__________________________________ 。
(1)所含铁元素既有氧化性又有还原性的物质是________(用字母代号填)。
| A.Fe | B.FeCl3 | C.FeSO4 | D.Fe2O3 |
(3)电子工业需要用30 %的FeCl3溶液腐蚀敷在绝缘板上的铜片制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式
(4)若要验证该溶液中含有Fe2+,正确的实验方法是
A.向试管中加入试液,滴入KSCN溶液,若显血红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+
(5)欲从废液中回收铜,并重新获得FeCl3溶液设计实验方案如下:

①写出上述实验中有关物质的化学式:A:
②写出通入C的化学方程式
您最近一年使用:0次
10-11高三上·福建南平·阶段练习
10 . 将 SO2气体与足量 Fe2 (SO4)3溶液完全反应后, 再加入K2Cr2O7溶液, 发生如下两个化学反应: SO2+2Fe3++2H2O= +2Fe2++4H⁺, Cr2O
+2Fe2++4H⁺, Cr2O +6Fe2++14H⁺=2Cr3++6Fe3++7H2O,有关说法正确的是
+6Fe2++14H⁺=2Cr3++6Fe3++7H2O,有关说法正确的是
 +2Fe2++4H⁺, Cr2O
+2Fe2++4H⁺, Cr2O +6Fe2++14H⁺=2Cr3++6Fe3++7H2O,有关说法正确的是
+6Fe2++14H⁺=2Cr3++6Fe3++7H2O,有关说法正确的是A.还原性 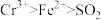 | B.氧化性  |
| C.两个反应中 Fe2(SO4)3均作还原剂 | D.Cr2O 能将 Na2SO3氧化成Na2SO4 能将 Na2SO3氧化成Na2SO4 |
您最近一年使用:0次
2023-10-17更新
|
1154次组卷
|
29卷引用:福建省武夷山一中2011届高三上学期第一次月考物理试题
(已下线)福建省武夷山一中2011届高三上学期第一次月考物理试题江西省南康中学2017-2018学年高一上学期第三次月考化学试题河北省邢台市第一中学2017-2018学年高一下学期开学考试化学试题2018-2019学年人教版高中化学必修一:18-19 章末综合测评2 化学物质及其变化江西省南康中学2018-2019学年高一上学期第三次月考化学试题贵州省剑河县二中2018-2019学年高一上学期期末考试化学试题【校级联考】安徽省六安市毛坦厂中学、金安高级中学2018-2019学年高一上学期期末联考化学试题云南省华宁县第二中学2018-2019学年高一下学期开学考试化学试题【全国百强校】山西省大同市第一中学2018-2019学年高二下学期期中考试化学试题步步为赢 高一化学寒假作业:作业十七 综合评估(一)江西省南康中学2019-2020学年高一上学期12月月考化学试题人教版(2019)高一必修第一册 第一章素养检测(已下线)【浙江新东方】25山东省青岛第五十八中学2020-2021学年高一上学期期中考试化学试题北京市中国人民大学附属中学2018-2019学年高一上学期期中考试化学试题贵州省毕节市金沙县第一中学2020-2021学年高一上学期期末考试化学试题福建省南平市浦城县2021-2022学年高一上学期期中考试化学试题四川省遂宁市射洪中学2021-2022学年高一上学期第三次(12月)月考化学试题四川省成都外国语学校2023-2024学年高一上学期10月月考化学试题宁夏回族自治区银川一中2023-2024学年高一上学期期中考试化学试题云南省昆明市第八中学2023-2024学年高一上学期9月月考化学试卷题辽宁省沈阳市第十五中学2023-2024学年高一上学期10月月考化学试题陕西省安康中学2023-2024学年高一上学期10月月考化学试题四川省广安市华蓥中学2023-2024学年高一上学期12月月考化学试题重庆市黔江中学校2023-2024学年高一上学期11月月考化学试题湖南省娄底市新化县2023-2024学年高一上学期期末考试化学试题模块一 物质及其变化(B卷)广东省吴川市两校2023-2024学年高二上学期期中联考化学试卷武威市第八中学2023年高一上学期期中考试化学试卷



