1 . 研究发现“利用零价铁还原 可脱除地下废水中硝酸盐”,某课外活动小组利用如下装置探究铁粉与
可脱除地下废水中硝酸盐”,某课外活动小组利用如下装置探究铁粉与 溶液的反应。实验步骤有如下五步:
溶液的反应。实验步骤有如下五步:
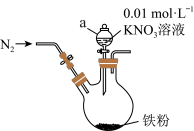
①打开弹簧夹,缓慢通入 ,并保持后续反应均在
,并保持后续反应均在 氛围中进行。
氛围中进行。
②加入pH已调至2.5的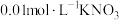 酸性溶液100mL,一段时间后铁屑部分溶解,溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现剩余固体表面有少量白色物质附着。
酸性溶液100mL,一段时间后铁屑部分溶解,溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现剩余固体表面有少量白色物质附着。
③连接好装置,并检查装置的气密性。
④检测到滤液中存在 、
、 和
和 。
。
⑤装好药品。
⑥过滤剩余固体时,表面的白色物质变为红褐色。
请回答下列问题:
(1)仪器a的名称是___________ 。
(2)通入 并保持后续反应均在
并保持后续反应均在 氛围中进行的实验目的是
氛围中进行的实验目的是___________ 。
(3)实验步骤的正确顺序是___________ 。
(4)白色物质是___________ ,白色物质变为红褐色的化学方程式为___________ :检验滤液中 所用的试剂是
所用的试剂是___________ 。
(5)某地下废水中 的含量测定。取VL废水,加入稀硫酸酸化,再加入
的含量测定。取VL废水,加入稀硫酸酸化,再加入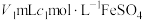 标准溶液(过量),充分反应后,用
标准溶液(过量),充分反应后,用 标准溶液滴定剩余的
标准溶液滴定剩余的 ,消耗
,消耗 标准溶液的体积为
标准溶液的体积为 ,终点时的现象是
,终点时的现象是___________ 。
 可脱除地下废水中硝酸盐”,某课外活动小组利用如下装置探究铁粉与
可脱除地下废水中硝酸盐”,某课外活动小组利用如下装置探究铁粉与 溶液的反应。实验步骤有如下五步:
溶液的反应。实验步骤有如下五步: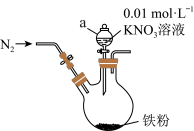
①打开弹簧夹,缓慢通入
 ,并保持后续反应均在
,并保持后续反应均在 氛围中进行。
氛围中进行。②加入pH已调至2.5的
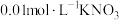 酸性溶液100mL,一段时间后铁屑部分溶解,溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现剩余固体表面有少量白色物质附着。
酸性溶液100mL,一段时间后铁屑部分溶解,溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现剩余固体表面有少量白色物质附着。③连接好装置,并检查装置的气密性。
④检测到滤液中存在
 、
、 和
和 。
。⑤装好药品。
⑥过滤剩余固体时,表面的白色物质变为红褐色。
请回答下列问题:
(1)仪器a的名称是
(2)通入
 并保持后续反应均在
并保持后续反应均在 氛围中进行的实验目的是
氛围中进行的实验目的是(3)实验步骤的正确顺序是
(4)白色物质是
 所用的试剂是
所用的试剂是(5)某地下废水中
 的含量测定。取VL废水,加入稀硫酸酸化,再加入
的含量测定。取VL废水,加入稀硫酸酸化,再加入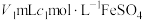 标准溶液(过量),充分反应后,用
标准溶液(过量),充分反应后,用 标准溶液滴定剩余的
标准溶液滴定剩余的 ,消耗
,消耗 标准溶液的体积为
标准溶液的体积为 ,终点时的现象是
,终点时的现象是
您最近一年使用:0次
名校
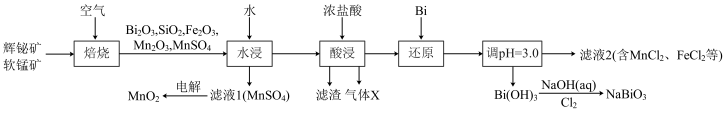
2 . 铋酸钠(NaBiO3)是常用的氧化剂,MnO2是活性电极。以辉铋矿(主要成分为Bi2S3,含FeS2、SiO2杂质)和软锰矿(主要成分是MnO2)为原料联合焙烧制备NaBiO3和MnO2,流程如下:
已知:①金属活动性:Fe>(H)>Bi>Cu。
②几种金属离子的氢氧化物沉淀pH如下:
回答下列问题:
(1)NaBiO3中Bi的化合价为_____ 。气体X是_____ (填化学式)。
(2)“焙烧”中Bi2S3和MnO2与空气反应生成Bi2O3和MnSO4,写出其反应的化学方程式:_____ 。被还原的元素是_____ (填元素符号)。
(3)“还原”中Bi的作用是_____ 。
(4)检验滤液2中是否有FeCl3的试剂是_____ (填化学式)。
(5)已知Bi(OH)3难溶于水,NaBiO3难溶于冷水,写出冷水中利用Bi(OH)3制备NaBiO3的离子方程式:_____ 。
(6)为探究Cl2和NaBiO3的氧化性相对强弱,设计如下实验:

实验中观察到试管B中溶液变蓝色。
由上述实验现象可知,氧化性:NaBiO3_____ Cl2(填“>”或“<”)。与根据第(5)小题得出的NaBiO3与Cl2氧化性强弱关系相反,其主要原因是_____ 。

已知:①金属活动性:Fe>(H)>Bi>Cu。
②几种金属离子的氢氧化物沉淀pH如下:
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.5 | 2.8 |
| Fe2+ | 6.3 | 8.3 |
| Mn2+ | 8.1 | 10.1 |
(1)NaBiO3中Bi的化合价为
(2)“焙烧”中Bi2S3和MnO2与空气反应生成Bi2O3和MnSO4,写出其反应的化学方程式:
(3)“还原”中Bi的作用是
(4)检验滤液2中是否有FeCl3的试剂是
(5)已知Bi(OH)3难溶于水,NaBiO3难溶于冷水,写出冷水中利用Bi(OH)3制备NaBiO3的离子方程式:
(6)为探究Cl2和NaBiO3的氧化性相对强弱,设计如下实验:

实验中观察到试管B中溶液变蓝色。
由上述实验现象可知,氧化性:NaBiO3
您最近一年使用:0次
3 . 向FeI2溶液中不断通入Cl2,体系中I-、I2、IO 、Fe2+、Fe3+等粒子的物质的量随
、Fe2+、Fe3+等粒子的物质的量随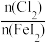 的变化可用如图简单表示,下列说法错误的是
的变化可用如图简单表示,下列说法错误的是

 、Fe2+、Fe3+等粒子的物质的量随
、Fe2+、Fe3+等粒子的物质的量随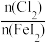 的变化可用如图简单表示,下列说法错误的是
的变化可用如图简单表示,下列说法错误的是
| A.A线表示n(I-)的变化 |
| B.D线对应的反应的离子方程式为2Fe2++Cl2=2Cl-+2Fe3+ |
C.形成IO 时,反应的离子方程式为5Cl2+I2+12OH-=2IO 时,反应的离子方程式为5Cl2+I2+12OH-=2IO +6H2O+10Cl- +6H2O+10Cl- |
D.当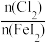 =1.2时,反应的离子方程式为2Fe2++10I-+6Cl2=5I2+2Fe3++12Cl- =1.2时,反应的离子方程式为2Fe2++10I-+6Cl2=5I2+2Fe3++12Cl- |
您最近一年使用:0次
名校
解题方法
4 . 一种利用低品位铜矿( 、CuS、FeO和
、CuS、FeO和 等)为原料制取CuCl的工艺流程如下:
等)为原料制取CuCl的工艺流程如下:
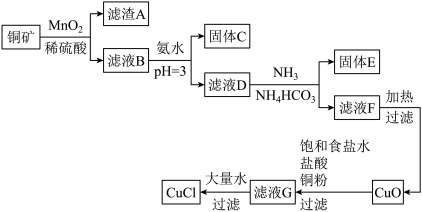
已知:i.水溶液中不存在碳酸铜,碳酸铜遇水立即水解为碱式碳酸铜和氢氧化铜。
ii.室温时, 的溶度积常数
的溶度积常数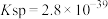 。
。
(1)铜矿中被 氧化的物质有
氧化的物质有_______ 。
(2)滤液D中铁离子的浓度约为_______ ,向滤液D中先通氨气的目的_______ 。
(3)固体E主要是 ,生成
,生成 的离子方程式是
的离子方程式是_______ 。
(4)滤液F加热生成 、
、 和CuO,反应的化学方程式是
和CuO,反应的化学方程式是_______ 。
(5)查阅资料:+1价Cu和 可以形成2种配离子
可以形成2种配离子 和
和 。滤液G加大量水析出CuCl沉淀,从平衡移动角度分析,滤液G中的配离子是哪种更有利于CuCl的生成
。滤液G加大量水析出CuCl沉淀,从平衡移动角度分析,滤液G中的配离子是哪种更有利于CuCl的生成_______ 。
(6)CuCl质量分数的测定
称取mg样品,溶于25mL过量的硫酸铁铵溶液( 将+1价Cu氧化),滴加2滴试亚铁灵指示剂(与
将+1价Cu氧化),滴加2滴试亚铁灵指示剂(与 发生特征反应,溶液呈红棕色),用含
发生特征反应,溶液呈红棕色),用含 的硫酸铁铈标准液滴定
的硫酸铁铈标准液滴定 ,共消耗硫酸铁铈标准液VmL,则CuCl质量分数的计算式
,共消耗硫酸铁铈标准液VmL,则CuCl质量分数的计算式_______ 。
 、CuS、FeO和
、CuS、FeO和 等)为原料制取CuCl的工艺流程如下:
等)为原料制取CuCl的工艺流程如下:
已知:i.水溶液中不存在碳酸铜,碳酸铜遇水立即水解为碱式碳酸铜和氢氧化铜。
ii.室温时,
 的溶度积常数
的溶度积常数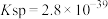 。
。(1)铜矿中被
 氧化的物质有
氧化的物质有(2)滤液D中铁离子的浓度约为
(3)固体E主要是
 ,生成
,生成 的离子方程式是
的离子方程式是(4)滤液F加热生成
 、
、 和CuO,反应的化学方程式是
和CuO,反应的化学方程式是(5)查阅资料:+1价Cu和
 可以形成2种配离子
可以形成2种配离子 和
和 。滤液G加大量水析出CuCl沉淀,从平衡移动角度分析,滤液G中的配离子是哪种更有利于CuCl的生成
。滤液G加大量水析出CuCl沉淀,从平衡移动角度分析,滤液G中的配离子是哪种更有利于CuCl的生成(6)CuCl质量分数的测定
称取mg样品,溶于25mL过量的硫酸铁铵溶液(
 将+1价Cu氧化),滴加2滴试亚铁灵指示剂(与
将+1价Cu氧化),滴加2滴试亚铁灵指示剂(与 发生特征反应,溶液呈红棕色),用含
发生特征反应,溶液呈红棕色),用含 的硫酸铁铈标准液滴定
的硫酸铁铈标准液滴定 ,共消耗硫酸铁铈标准液VmL,则CuCl质量分数的计算式
,共消耗硫酸铁铈标准液VmL,则CuCl质量分数的计算式
您最近一年使用:0次
2023-03-17更新
|
543次组卷
|
6卷引用:河南省湘豫名校2023届高三下学期第一次模拟化学试题变式题(工业流程题)
(已下线)河南省湘豫名校2023届高三下学期第一次模拟化学试题变式题(工业流程题)(已下线)专题20 工艺流程题北京市石景山区2022-2023学年高三下学期质量监控(零模)化学试题北京市石景山区2023-2024学年高三上学期一模考试化学试题北京市第一六一中学2023-2024学年高三下学期开学考化学试题北京市中国人民大学附属中学丰台学校2023-2024学年高三上学期12月月考化学试题
5 . 化学家克里斯特(Christe)制备F2的原理如下:
(1)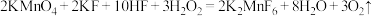
(2)
(3)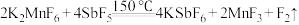
下列说法正确的是
(1)
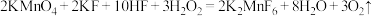
(2)

(3)
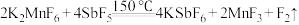
下列说法正确的是
| A.反应(1)中氧化剂、还原剂的物质的量之比为2∶3 |
| B.反应(2)的原理是“较强酸制备较弱酸” |
| C.反应(3)中氧化性:F2>K2MnF6 |
| D.上述3个反应都是氧化还原反应 |
您最近一年使用:0次
2022-12-23更新
|
140次组卷
|
3卷引用:河南省湘豫名校联考2022-2023学年高三上学期12月期末摸底考试变式汇编(9-16)
(已下线)河南省湘豫名校联考2022-2023学年高三上学期12月期末摸底考试变式汇编(9-16) 河南省湘豫名校联考2022-2023学年高三上学期12月期末摸底考试化学试题 河南省郑州市等3地2022-2023学年高三上学期12月月考化学试题
解题方法
6 . 已知:①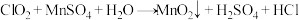
②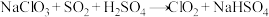
③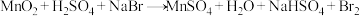
下列说法正确的是
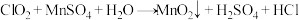
②
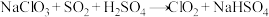
③
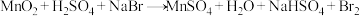
下列说法正确的是
A.氧化性: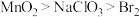 |
| B.反应①②中含氯的物质均被还原 |
C. 溶液与 溶液与 溶液不能发生反应 溶液不能发生反应 |
D.反应②③中转移等物质的量的电子时,消耗 的物质的量相等 的物质的量相等 |
您最近一年使用:0次
解题方法
7 . 已知:①ClO2+MnSO4+H2O→MnO2↓+H2SO4+HCl
②NaClO3+SO2+H2SO4→ClO2+NaHSO4
③MnO2+H2SO4+NaBr→MnSO4+H2O+NaHSO4+Br2
下列说法正确的是
②NaClO3+SO2+H2SO4→ClO2+NaHSO4
③MnO2+H2SO4+NaBr→MnSO4+H2O+NaHSO4+Br2
下列说法正确的是
| A.氧化性:MnO2>NaClO3>Br2 |
| B.反应①②中含氯的物质均被还原 |
| C.NaClO3溶液与MnSO4溶液不能发生反应 |
| D.反应②③中转移等物质的量的电子时,消耗H2SO4的物质的量相等 |
您最近一年使用:0次
8 . 已知下列实验事实:
①Cr2O3固体既能溶于KOH溶液得到KCrO2溶液,又能溶于硫酸得到Cr2(SO4)3溶液;
②向KCrO2溶液中滴加H2O2溶液,再酸化,可得K2Cr2O7溶液;
③将K2Cr2O7溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
下列判断不正确的是
①Cr2O3固体既能溶于KOH溶液得到KCrO2溶液,又能溶于硫酸得到Cr2(SO4)3溶液;
②向KCrO2溶液中滴加H2O2溶液,再酸化,可得K2Cr2O7溶液;
③将K2Cr2O7溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
下列判断不正确的是
| A.实验①证明Cr2O3是两性氧化物 |
B.实验③证明氧化性:I2 <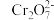 |
| C.化合物KCrO2中Cr元素为+6价 |
| D.实验②证明H2O2有氧化性 |
您最近一年使用:0次
名校
解题方法
9 . 已知:将H2S和O2的混合气体通入FeCl3、CuCl2的混合溶液中,部分有关物质转化如图所示。下列说法正确的是
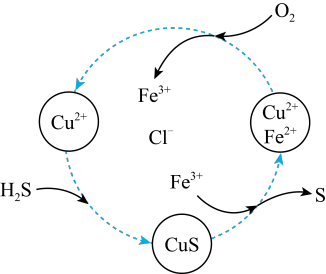
| A.CuCl2溶液和H2S反应的离子方程式为S2−+Cu2+=CuS↓ |
| B.FeCl3在转化过程中发生的反应为Fe3+ +CuS=Fe2++ Cu2++S |
| C.O2在转化过程中发生的反应为O2 +2Fe2+ +4H+=2Fe3++2H2O |
| D.反应过程中的总反应为2H2S+O2=2S↓+2H2O |
您最近一年使用:0次
2022-07-10更新
|
345次组卷
|
5卷引用:选择题11-16
名校
解题方法
10 . 下列过程中的化学反应,相应的离子方程式错误的是
A.将稀H2SO4加入NaIO3和NaI的混合溶液中:5I-+IO +6H+=3I2+3H2O +6H+=3I2+3H2O |
B.向稀HNO3中滴加Na2SO3溶液:3SO +2H++2NO +2H++2NO =3SO =3SO +2NO↑+H2O +2NO↑+H2O |
| C.将Na2O2加入CuSO4溶液中:2Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑ |
D.向NaHCO3溶液中加入足量Ba(OH)2溶液:2HCO +Ba2++2OH-=BaCO3↓+2H2O+CO +Ba2++2OH-=BaCO3↓+2H2O+CO |
您最近一年使用:0次
2022-03-15更新
|
1583次组卷
|
8卷引用:选择题11-16
(已下线)选择题11-16河南省开封市2022届高三第二次模拟考试理综化学试题(已下线)专题03离子反应-2022年高考真题+模拟题汇编(全国卷)(已下线)专题03离子反应-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题03离子反应-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题03 氧化还原反应-备战2023年高考化学母题题源解密(全国通用)(已下线)二轮专题强化练 专题3 离子方程式的书写及正误判断安徽省六安第一中学2023届高三下学期高考适应性考试理科综合化学试题



