安徽省六安第一中学2023届高三下学期高考适应性考试理科综合化学试题
安徽
高三
模拟预测
2023-07-13
472次
整体难度:
适中
考查范围:
认识化学科学、物质结构与性质、化学与STSE、化学实验基础、有机化学基础、常见无机物及其应用、化学反应原理
安徽省六安第一中学2023届高三下学期高考适应性考试理科综合化学试题
安徽
高三
模拟预测
2023-07-13
472次
整体难度:
适中
考查范围:
认识化学科学、物质结构与性质、化学与STSE、化学实验基础、有机化学基础、常见无机物及其应用、化学反应原理
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
解题方法
1. 国画、古诗词是我国传统文化的瑰宝。下列有关说法不正确的是
| A.墨的主要成分炭黑是一种无定形碳,与金刚石互为同素异形体 |
| B.我国古代绘画所用的“绢”是一种人工合成的高分子材料 |
| C.“朝坛雾卷,曙岭烟沉”,雾有丁达尔现象是因为胶体粒子对光有散射作用 |
| D.“章山之铜,所谓丹阳铜也。今有白铜,盖点化为之,非其本质”,白铜比纯铜硬度大,熔点低 |
您最近一年使用:0次
2023-06-06更新
|
322次组卷
|
2卷引用:安徽省六安第一中学2023届高三下学期高考适应性考试理科综合化学试题
单选题
|
较易(0.85)
名校
解题方法
2. 下列过程中的化学反应,相应的离子方程式错误的是
A.将稀H2SO4加入NaIO3和NaI的混合溶液中:5I-+IO +6H+=3I2+3H2O +6H+=3I2+3H2O |
B.向稀HNO3中滴加Na2SO3溶液:3SO +2H++2NO +2H++2NO =3SO =3SO +2NO↑+H2O +2NO↑+H2O |
| C.将Na2O2加入CuSO4溶液中:2Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑ |
D.向NaHCO3溶液中加入足量Ba(OH)2溶液:2HCO +Ba2++2OH-=BaCO3↓+2H2O+CO +Ba2++2OH-=BaCO3↓+2H2O+CO |
【知识点】 离子方程式的正误判断解读 氧化还原反应的规律解读
您最近一年使用:0次
2022-03-15更新
|
1583次组卷
|
8卷引用:河南省开封市2022届高三第二次模拟考试理综化学试题
河南省开封市2022届高三第二次模拟考试理综化学试题(已下线)专题03离子反应-2022年高考真题+模拟题汇编(全国卷)(已下线)专题03离子反应-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题03离子反应-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题03 氧化还原反应-备战2023年高考化学母题题源解密(全国通用)(已下线)二轮专题强化练 专题3 离子方程式的书写及正误判断安徽省六安第一中学2023届高三下学期高考适应性考试理科综合化学试题(已下线)选择题11-16
单选题
|
适中(0.65)
名校
解题方法
3. 我国自主发明的“钛战甲”——钛合金材料,为实现万米深潜的“奋斗者”号建造了世界最大、搭载人数最多的潜水器载人舱球壳。四氯化钛( )是生产钛合金的重要原料,某化学实验小组以
)是生产钛合金的重要原料,某化学实验小组以 和足量
和足量 为原料制取
为原料制取 ,装置如下图:
,装置如下图:

有关物质的性质如上表,下列说法错误的是
 )是生产钛合金的重要原料,某化学实验小组以
)是生产钛合金的重要原料,某化学实验小组以 和足量
和足量 为原料制取
为原料制取 ,装置如下图:
,装置如下图:
| 物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
 | -23 | 76.8 | 与 互溶 互溶 |
 | -25 | 136 | 遇潮湿空气产生白雾 |
A.B中 反应的化学方程式为 反应的化学方程式为 |
| B.实验开始时,点燃A处的酒精灯,再点燃B处 |
C.D中盛装的是碱石灰,防止生成的 遇到空气中的水溶解变质 遇到空气中的水溶解变质 |
D.欲分离C装置中的 ,应采用的实验操作为蒸发 ,应采用的实验操作为蒸发 |
您最近一年使用:0次
2023-02-12更新
|
656次组卷
|
3卷引用:吉林省吉林市普通高中2022-2023学年高三第二次调研测试化学试题
吉林省吉林市普通高中2022-2023学年高三第二次调研测试化学试题(已下线)先机卷 02 -【热题狂飙】2023年高考化学样卷(全国卷专用)安徽省六安第一中学2023届高三下学期高考适应性考试理科综合化学试题
单选题
|
适中(0.65)
名校
解题方法
4. 异黄酮类化合物是药用植物的有效成分。一种异黄酮Z的部分合成路线如下:
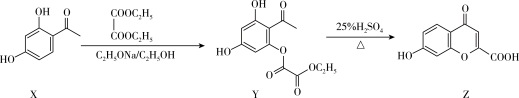
下列有关化合物X、Y和Z的说法正确的是

下列有关化合物X、Y和Z的说法正确的是
| A.X分子中碳原子杂化类型均为sp2 |
| B.Y在水中的溶解性比Z好 |
| C.Z与C2H5l8OH发生酯化反应,示踪原子18O在产物水中 |
| D.等物质的量的X、Y、Z,完全反应消耗NaOH的物质的量之比为1∶2∶1 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
5. 短周期元素X、Y、Z、W的原子序数依次增大。用表中信息判断下列说法不正确的是
| 元素 | X | Y | Z | W | |
| 最高价氧化物的水化物 | 分子式 | H3ZO4 | |||
| 25℃时,0.1mol·L-1溶液对应的pH | 1.00 | 13.00 | 1.57 | 0.70 | |
| A.YX3用于汽车防撞气囊,是离子晶体 |
B.简单氢化物分子内的键角: |
| C.足量的锌与W最高价氧化物的水化物的浓溶液充分反应,还原产物有2种 |
| D.31gZ4分子中含有1.5molσ键 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
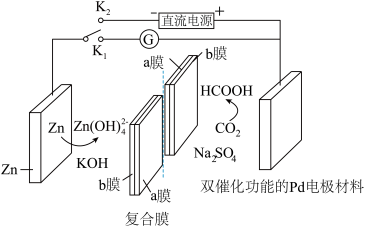
6. 水系可逆 电池在工作时,复合膜(由a、b膜复合而成,a膜只允许
电池在工作时,复合膜(由a、b膜复合而成,a膜只允许 通过,b膜只允许
通过,b膜只允许 通过)层间的
通过)层间的 解离成
解离成 和
和 ,在外加电场中可透过相应的离子膜定向移动。当闭合
,在外加电场中可透过相应的离子膜定向移动。当闭合 时,
时, 电池工作原理如图所示,下列说法正确的是
电池工作原理如图所示,下列说法正确的是
 电池在工作时,复合膜(由a、b膜复合而成,a膜只允许
电池在工作时,复合膜(由a、b膜复合而成,a膜只允许 通过,b膜只允许
通过,b膜只允许 通过)层间的
通过)层间的 解离成
解离成 和
和 ,在外加电场中可透过相应的离子膜定向移动。当闭合
,在外加电场中可透过相应的离子膜定向移动。当闭合 时,
时, 电池工作原理如图所示,下列说法正确的是
电池工作原理如图所示,下列说法正确的是
A.闭合 时,右侧电极反应为 时,右侧电极反应为 |
B.闭合 时,电池工作一段时间,复合膜两侧溶液的pH左侧升高右侧降低 时,电池工作一段时间,复合膜两侧溶液的pH左侧升高右侧降低 |
C.闭合 时, 时, 从复合膜流向Zn电极 从复合膜流向Zn电极 |
D.闭合 时,每生成65gZn,同时一定生成 时,每生成65gZn,同时一定生成 气体11.2L 气体11.2L |
您最近一年使用:0次
2023-03-11更新
|
1396次组卷
|
5卷引用:河北省唐山市2023届高三一模考试化学试题
单选题
|
较难(0.4)
名校
7. 25℃时,往 溶液中滴入
溶液中滴入 溶液,体系中
溶液,体系中 、
、 、
、 溶液的体积与溶液pH的关系如图所示。下列说法正确的是
溶液的体积与溶液pH的关系如图所示。下列说法正确的是

 溶液中滴入
溶液中滴入 溶液,体系中
溶液,体系中 、
、 、
、 溶液的体积与溶液pH的关系如图所示。下列说法正确的是
溶液的体积与溶液pH的关系如图所示。下列说法正确的是
A.曲线②表示 与溶液pH的关系 与溶液pH的关系 |
B.a点对应的溶液中: |
C.b点对应的溶液中: |
D.25℃时,HA的电离平衡常数的数量级为 |
您最近一年使用:0次
2023-01-12更新
|
649次组卷
|
4卷引用:湖南省长沙市2022-2023学年高三上学期1月期末考试化学试题
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
8. Ⅰ.硫脲的制备:硫脲[ ]是一种白色晶体,熔点180℃,易溶于水和乙醇,受热时部分发生异构化反应而生成硫氰化铵,可用于制造药物,也可用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题
]是一种白色晶体,熔点180℃,易溶于水和乙醇,受热时部分发生异构化反应而生成硫氰化铵,可用于制造药物,也可用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题
已知:将石灰氮( )和水的混合物加热至80℃时,通入硫化氢气体反应可生成硫脲溶液和石灰乳,实验装置如图所示。
)和水的混合物加热至80℃时,通入硫化氢气体反应可生成硫脲溶液和石灰乳,实验装置如图所示。
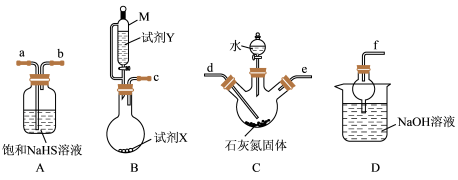
(1)装置B中的试剂X和试剂Y的最佳组合是___________ (填序号)。
A. 固体+浓硫酸 B.
固体+浓硫酸 B. 固体+稀硝酸 C.
固体+稀硝酸 C. 固体+稀盐酸
固体+稀盐酸
(2)按(1)中所选试剂组合,按气流从左到右的方向,上述装置的合理连接顺序为c→___________ (填仪器接口的小写字母)。
Ⅱ.实验室以苯甲酸和乙醇为原料制备苯甲酸乙酯,实验装置如图(加热及夹持装置已省略)。
反应原理: +CH3CH2OH
+CH3CH2OH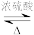
 +H2O
+H2O
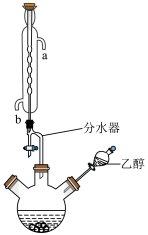
实验步骤如下:
步骤1:在三颈烧瓶中加入12.20g苯甲酸、20mL环己烷、5mL浓硫酸、沸石,并通过分液漏斗加入60mL(过量)乙醇,控制温度在65~70℃加热回流2h.反应时“环己烷-乙醇-水”会形成共沸物(沸点62.6℃)蒸馏出来,再利用分水器不断分离除去水,回流环己烷和乙醇。
步骤2:反应一段时间,打开旋塞放出分水器中液体,关闭旋塞,继续加热维持反应。
步骤3:将三颈烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性。
步骤4:用分液漏斗分离出有机层,水层用25mL乙醚萃取分液,然后合并至有机层。加入氯化钙,对粗产物进行蒸馏,低温蒸出乙醚后,继续升温,接收210~213℃的馏分,得到产品10.00mL。
请回答下列问题:
(3)加入环己烷的目的是___________ 。
(4)判断反应已完成的标志是___________ 。
(5)步骤4中对水层用乙醚再萃取后合并至有机层的目的是___________ 。下图关于步骤4中对水层的萃取分液的相关操作的正确顺序为___________ (用编号排序)。

(6)本实验中苯甲酸乙酯的产率为___________ 。
 ]是一种白色晶体,熔点180℃,易溶于水和乙醇,受热时部分发生异构化反应而生成硫氰化铵,可用于制造药物,也可用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题
]是一种白色晶体,熔点180℃,易溶于水和乙醇,受热时部分发生异构化反应而生成硫氰化铵,可用于制造药物,也可用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题已知:将石灰氮(
 )和水的混合物加热至80℃时,通入硫化氢气体反应可生成硫脲溶液和石灰乳,实验装置如图所示。
)和水的混合物加热至80℃时,通入硫化氢气体反应可生成硫脲溶液和石灰乳,实验装置如图所示。
(1)装置B中的试剂X和试剂Y的最佳组合是
A.
 固体+浓硫酸 B.
固体+浓硫酸 B. 固体+稀硝酸 C.
固体+稀硝酸 C. 固体+稀盐酸
固体+稀盐酸(2)按(1)中所选试剂组合,按气流从左到右的方向,上述装置的合理连接顺序为c→
Ⅱ.实验室以苯甲酸和乙醇为原料制备苯甲酸乙酯,实验装置如图(加热及夹持装置已省略)。
反应原理:
 +CH3CH2OH
+CH3CH2OH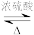
 +H2O
+H2O
| 物质 | 颜色、状态 | 沸点(℃) | 密度(g·cm-3) |
| 苯甲酸 | 无色晶体 | 249(100°C升华) | 1.27 |
| 苯甲酸乙酯 | 无色液体 | 212.6 | 1.05 |
| 乙醇 | 无色液体 | 78.3 | 0.79 |
| 环己烷 | 无色液体 | 80.8 | 0.73 |
步骤1:在三颈烧瓶中加入12.20g苯甲酸、20mL环己烷、5mL浓硫酸、沸石,并通过分液漏斗加入60mL(过量)乙醇,控制温度在65~70℃加热回流2h.反应时“环己烷-乙醇-水”会形成共沸物(沸点62.6℃)蒸馏出来,再利用分水器不断分离除去水,回流环己烷和乙醇。
步骤2:反应一段时间,打开旋塞放出分水器中液体,关闭旋塞,继续加热维持反应。
步骤3:将三颈烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性。
步骤4:用分液漏斗分离出有机层,水层用25mL乙醚萃取分液,然后合并至有机层。加入氯化钙,对粗产物进行蒸馏,低温蒸出乙醚后,继续升温,接收210~213℃的馏分,得到产品10.00mL。
请回答下列问题:
(3)加入环己烷的目的是
(4)判断反应已完成的标志是
(5)步骤4中对水层用乙醚再萃取后合并至有机层的目的是

(6)本实验中苯甲酸乙酯的产率为
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
名校
解题方法
9. NiCl2是一种重要催化剂。某科研小组以废弃催化剂(含Ni2+、Cu2+、Fe3+、Ca2+、Mg2+等)为原料,按如图流程回收NiCl2·6H2O晶体,回答下列问题。

已知:Ksp(CaF2)=4×10-11,Ksp(MgF2)=9×10-9
(1)滤渣1的成分主要是___________ 。
(2)X可以为Cl2或H2O2.若X为H2O2,试剂Y的使用量会减少,原因是___________ (用离子方程式加以说明)。
(3)氟化除杂时要保证完全除去Ca2+和Mg2+(离子浓度≤10-5mol/L),滤液3中c(F-)不小于___________ mol/L。
(4)操作A为___________ 、冷却结晶、过滤、洗涤。
(5)将所得NiCl2·6H2O与SOCl2混合加热可制备无水NiCl2并得到两种酸性气体,该反应的化学方程式为___________ 。
(6)废旧锂离子电池含LiNiO2的正极材料经预处理后,可采用如图原理富集Ni元素。
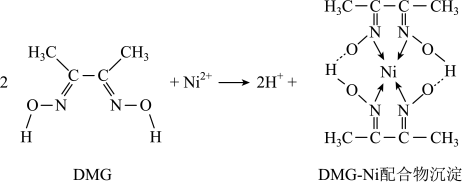
DMG-Ni配合物中存在的作用力有___________(填序号)。
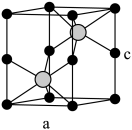
(7)红砷镍矿是一种六方晶体(底面为60°和120°的菱形),其晶胞如图所示,图中黑色小球为Ni,浅色大球为As
①晶胞中Ni周围距离最近且等距的As有___________ 个
②已知NiAs的晶胞边长分别为a pm和c pm,阿伏加德罗常数的值为NA,则红砷镍矿晶体的理论密度为ρ=___________ g·cm-3(写出表达式,需化简)

已知:Ksp(CaF2)=4×10-11,Ksp(MgF2)=9×10-9
(1)滤渣1的成分主要是
(2)X可以为Cl2或H2O2.若X为H2O2,试剂Y的使用量会减少,原因是
(3)氟化除杂时要保证完全除去Ca2+和Mg2+(离子浓度≤10-5mol/L),滤液3中c(F-)不小于
(4)操作A为
(5)将所得NiCl2·6H2O与SOCl2混合加热可制备无水NiCl2并得到两种酸性气体,该反应的化学方程式为
(6)废旧锂离子电池含LiNiO2的正极材料经预处理后,可采用如图原理富集Ni元素。

DMG-Ni配合物中存在的作用力有___________(填序号)。
| A.极性键 | B.非极性键 | C.氢键 | D.配位键 |
①晶胞中Ni周围距离最近且等距的As有
②已知NiAs的晶胞边长分别为a pm和c pm,阿伏加德罗常数的值为NA,则红砷镍矿晶体的理论密度为ρ=

您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
名校
解题方法
10. Ⅰ.甲醇(CH3OH)是结构最为简单的饱和一元醇,又称“木醇”或“木精”。常用于制造甲醛和农药等。CO2催化加氢制甲醇,极具前景。发生的主要反应如下:
① CO(g) +2H2(g) CH3OH(g) ΔH1= -90.6 kJ·mol-1
CH3OH(g) ΔH1= -90.6 kJ·mol-1
② CO2(g) +H2(g) CO(g)+ H2O(g) ΔH2=+41.2 kJ·mol-1
CO(g)+ H2O(g) ΔH2=+41.2 kJ·mol-1
③CO2(g) +3H2(g) CH3OH(g)+ H2O(g) ΔH3
CH3OH(g)+ H2O(g) ΔH3
回答下列问题:
(1)△H3=___________ kJ·mol-1。
(2)对于反应②,达平衡后,下列措施一定能提高H2转化率的是___________(填字母)。
(3)向盛有催化剂的刚性容器中通入n(CO2):n(H2)=1:3混合气体,发生③反应。在T1 K和T2 K时,CO2的转化率(α)与时间(t)的关系如图所示。

①温度:T1___________ (填“> ”或“<”)T2。
②T2K时,若平衡时体系的总压强为p0,则平衡常数Kp =_______ (用含有p0的代数式表示)。
Ⅱ.已二腈[NC(CH2)4CN]是合成尼龙-66的中间体,其制备方法如下。
(i)己二酸氨化法

(4)下列说法正确的是___________ (填字母)。
a.己二腈的分子中含有碳氮三键
b.反应②和④中均有H2O生成
c.H2O2分子中所有原子在同一平面
(ii)丙烯腈CH2=CHCN电解二聚法(两极均为惰性电极),电解原理如图,总反应为4CH2=CHCN+2H2O 2NC(CH2)4CN+O2↑,主要副产物为丙腈(C2H5CN)。
2NC(CH2)4CN+O2↑,主要副产物为丙腈(C2H5CN)。

(5)电极X为___________ (填“阴”或“阳”)极。
(6)写出i的电极反应式:___________ 。
① CO(g) +2H2(g)
 CH3OH(g) ΔH1= -90.6 kJ·mol-1
CH3OH(g) ΔH1= -90.6 kJ·mol-1② CO2(g) +H2(g)
 CO(g)+ H2O(g) ΔH2=+41.2 kJ·mol-1
CO(g)+ H2O(g) ΔH2=+41.2 kJ·mol-1③CO2(g) +3H2(g)
 CH3OH(g)+ H2O(g) ΔH3
CH3OH(g)+ H2O(g) ΔH3回答下列问题:
(1)△H3=
(2)对于反应②,达平衡后,下列措施一定能提高H2转化率的是___________(填字母)。
| A.加入适量氢气 | B.使用高效催化剂 | C.增大n(CO2) | D.升高温度 |

①温度:T1
②T2K时,若平衡时体系的总压强为p0,则平衡常数Kp =
Ⅱ.已二腈[NC(CH2)4CN]是合成尼龙-66的中间体,其制备方法如下。
(i)己二酸氨化法

(4)下列说法正确的是
a.己二腈的分子中含有碳氮三键
b.反应②和④中均有H2O生成
c.H2O2分子中所有原子在同一平面
(ii)丙烯腈CH2=CHCN电解二聚法(两极均为惰性电极),电解原理如图,总反应为4CH2=CHCN+2H2O
 2NC(CH2)4CN+O2↑,主要副产物为丙腈(C2H5CN)。
2NC(CH2)4CN+O2↑,主要副产物为丙腈(C2H5CN)。
(5)电极X为
(6)写出i的电极反应式:
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
名校
解题方法
11. 化合物G是一种药物合成中间体,其合成路线如下:

回答下列问题:
(1)A的名称是___________ ;C中的官能团名称是___________ 。
(2)②的反应类型是___________ ;写出D的结构简式并用星号(*)标出D中的手性碳原子___________ 。
(3)具有六元碳环结构、且环上只有1个取代基,并能与NaOH溶液发生反应的C的同分异构体有___________ 种;写出一种能发生银镜反应的同分异构体的结构简式___________ 。(不考虑立体异构)
(4)写出F到G第一步反应的离子方程式___________ 。
(5)参照化合物G合成线路,设计由甲苯和乙酰乙酸乙酯(CH3COCH2COOC2H5)制备 的合成路线
的合成路线___________ (无机试剂任选)。

回答下列问题:
(1)A的名称是
(2)②的反应类型是
(3)具有六元碳环结构、且环上只有1个取代基,并能与NaOH溶液发生反应的C的同分异构体有
(4)写出F到G第一步反应的离子方程式
(5)参照化合物G合成线路,设计由甲苯和乙酰乙酸乙酯(CH3COCH2COOC2H5)制备
 的合成路线
的合成路线
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、物质结构与性质、化学与STSE、化学实验基础、有机化学基础、常见无机物及其应用、化学反应原理
试卷题型(共 11题)
题型
数量
单选题
7
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 胶体的性质和应用 几组常见同素异形体 化学科学对人类文明发展的意义 金属与合金性能比较 | |
| 2 | 0.85 | 离子方程式的正误判断 氧化还原反应的规律 | |
| 3 | 0.65 | 氧化还原反应在生活、生产中的应用 蒸馏与分馏 物质制备的探究 | |
| 4 | 0.65 | 羧酸酯化反应 含酯基有机物水解消耗NaOH的量的计算 | |
| 5 | 0.65 | 结合物质结构基础知识与NA相关推算 硫酸 键能、键长、键角及应用 离子晶体 | |
| 6 | 0.65 | 原电池原理理解 原电池电极反应式书写 电解原理的应用 电解池有关计算 | |
| 7 | 0.4 | 酸碱混合时的定性判断及计算 弱电解质的电离平衡 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 二、解答题 | |||
| 8 | 0.65 | 基于酯化反应机理的相关计算 酯化反应的机理 物质分离、提纯综合应用 萃取和分液 | 实验探究题 |
| 9 | 0.65 | 氧化还原反应方程式的配平 溶度积常数相关计算 物质结构与性质综合考查 物质分离、提纯综合应用 | 工业流程题 |
| 10 | 0.65 | 盖斯定律与热化学方程式 与转化率变化有关图像的分析 电解池电极反应式及化学方程式的书写与判断 有机分子中原子共面的判断 | 原理综合题 |
| 11 | 0.4 | 根据要求书写同分异构体 根据题给物质选择合适合成路线 有机合成综合考查 有机推断综合考查 | 有机推断题 |



